8.6: Usos médicos de los radioisótopos
- Page ID
- 77320
El uso de la química nuclear en las tecnologías médicas va aumentando con el tiempo. Los usos médicos se pueden dividir en dos categorías:
- imágenes médicas de órganos o diagnóstico de cualquier mal funcionamiento y
- uso terapéutico, principalmente para matar células cancerosas.
Radioisótopos en imágenes médicas
- los que emiten\(\ce{\gamma}\) rayos, directa o indirectamente, durante su decadencia,
- puede administrarse al órgano de interés en forma pura o etiquetarse en un compuesto,
- son de corta duración o pueden ser excretados del cuerpo después de su uso.
En el Cuadro 8.6.1 se enumeran algunos radioisótopos comúnmente utilizados en imágenes médicas. Se administra una dosis baja del radioisótopo a un paciente. \(\ce{\gamma}\)Los rayos cruzan el cuerpo y se registran como rayos X. Una computadora finalmente convierte la grabación en una imagen útil. La imagen se compara con una imagen de un órgano sano para diagnosticar cualquier mal funcionamiento.
|
Radioisótopo |
Símbolo |
Modo de decaimiento |
Vida media |
Uso en imágenes médicas |
|---|---|---|---|---|
|
Carbono-11 |
\(\ce{_6^11C}\) |
β +, g |
20.3 m |
Gammagrafía cerebral para rastrear glucosa |
|
Fluorín-19 |
\(\ce{_9^18F}\) |
β +, g |
109m |
Gammagrafía cerebral para rastrear glucosa |
|
Cromio-51 |
\(\ce{_24^51Cr}\) |
E.C., g |
27.3 d |
Diagnosticar albinismo; imagen del bazo y vía gastrointestinal |
|
Galio-67 |
\(\ce{_31^67Ga}\) |
E.C., g |
78.3 h |
Exploración de todo el cuerpo para detectar tumores |
|
Selenio-75 |
\(\ce{_34^75Se}\) |
E.C., g |
118 d |
Escaneo de páncreas |
|
Kryptón-81m |
\(\ce{_36^{81m}Kr}\) |
g |
13.3 s |
Exploración de ventilación pulmonar |
|
Xenón-133 |
\(\ce{_54^133Xe}\) |
β |
5.24 d |
Exploración de ventilación pulmonar |
|
Estroncio-81 |
\(\ce{_38^81Sr}\) |
β |
22.2 m |
Escaneo para cáncer de hueso y enfermedades óseas |
|
Mercurio-197 |
\(\ce{_80^197Hg}\) |
E.C., g |
64.1 h |
Gammagrafía renal |
|
Hierro-59 |
\(\ce{_26^59Fe}\) |
β, g |
44.5 d |
Función de la médula ósea y anemias |
|
Yodo-131 |
\(\ce{_53^131I}\) |
β, g |
8.04 d |
Diagnóstico de mal funcionamiento tiroideo |
|
Yodo-123 |
\(\ce{_53^123I}\) |
E.C., g |
13.2 h |
Diagnóstico de mal funcionamiento tiroideo |
|
Tecnecio-99m |
\(\ce{_43^{99m}Te}\) |
g |
6.01 h |
Exploraciones cerebrales, hepáticas, renales, óseas y diagnóstico del músculo cardíaco dañado |
|
Fósforo-32 |
\(\ce{_15^32P}\) |
β |
14.3 d |
Detectar tumores oculares |
|
Talio-201 |
\(\ce{_81^201Tl}\) |
E.C., g |
3.05 d |
Escaneo cardíaco y prueba de esfuerzo por ejercicio |
Un ejemplo de imagen médica es la glándula tiroides en el cuello que produce la hormona tiroxina, que controla la tasa global de metabolismo en el cuerpo. Cada molécula de tiroxina contiene cuatro átomos de yodo. La administración de la sal radiactiva Na 131 I o Na 123 I acumula el yodo en la glándula tiroides en pocas horas. Decaimiento de 131 I y 123 I implica\(\ce{\gamma}\) -emisión.
\[\ce{_53^131I -> _54^131Xe + _{-1}^{0}{e}} + \gamma\nonumber\]
\[\ce{_53^123I + _{-1}^{0}{e} -> _52^123Xe} + \gamma\nonumber\]
Se registra la\(\ce{\gamma}\) -emisión del yodo localizado en la glándula tiroides, como se muestra en la Fig. 8.6.1. Una tiroides hiperactiva (hipertiroidismo) acumula más y la tiroides hipoactiva (hipotiroidismo) acumula menos yodo que una tiroides sana.

Otro ejemplo es la tomografía por emisión de positrones (PET). Los emisores de positrones como el carbono-11 y el fluor-18 incorporados en un compuesto adecuado como la glucosa permiten seguir la ruta metabólica del compuesto. Por ejemplo, 18-fluorodesoxiglucosa (18-FDG) es una molécula de glucosa en la que uno de los oxígeno es reemplazado por 18 F. La inyección intravenosa del 18-FDG finalmente da como resultado la acumulación de 18-FDG en el cerebro y otros órganos del cuerpo donde la glucosa se usa en el proceso metabólico. El 18 F emite un positrón, que al ser una antipartícula del electrón, reacciona con el electrón y produce dos\(\ce{\gamma}\) rayos g.
\[\ce{_9^18F -> _8^18O + _{1}^{0}{e}} + \gamma\nonumber\]
\[\ce{_{1}^{0}{e} + _{1}^{0}{e} ->} 2\gamma\nonumber\]
\(\ce{\gamma}\)Los rayos se utilizan para obtener una imagen del órgano. La imagen revela áreas problemáticas en forma de una concentración anormal de glucosa en la parte del órgano. Por ejemplo, la Fig. 8.6.2 compara la imagen PET de un cerebro sano versus un cerebro con enfermedad de Alzheimer.

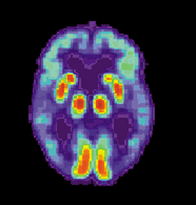
Dado que el metabolismo de la glucosa ocurre en todos los órganos, las TEP de todo el cuerpo se pueden usar para diagnosticar cánceres de pulmón, colorrectal, cabeza y cuello y esofágico, así como otras enfermedades que involucran un metabolismo anormal de la glucosa. Por ejemplo, los tumores tienen altas tasas metabólicas; para detectarlos se utilizan las exploraciones PET que utilizan 18-FDG, como se muestra en la Fig. 8.6.3.

Imágenes médicas sin usar radioisótopos
Los principales ejemplos de imágenes médicas que utilizan fuentes de radiación externa incluyen los siguientes.
- Los rayos X, que son fuente de radiación externa, se utilizan comúnmente para la obtención de imágenes médicas de órganos y huesos.
- La tomografía computarizada (TC) utiliza el procesamiento por computadora de muchas mediciones de rayos X, desde diferentes ángulos, para producir una vista transversal (cortes virtuales) del órgano.
- La imagen por resonancia magnética (MRI) es otra poderosa técnica de imagen médica que se basa en el hecho de que los átomos de hidrógeno se férula en dos estados de energía cuando se colocan en un campo magnético fuerte. Cuando se ilumina con radiación infrarroja (IR) de la energía que coincide con la brecha de energía entre los dos grupos, los átomos de hidrógeno se excitan desde el estado de energía inferior a superior. La decadencia del estado excitado emite las radiaciones IR que se registran para obtener la imagen de tejidos blandos que contienen muchos átomos de hidrógeno en forma de moléculas de agua. La Fig. 8.6.4 muestra algunos ejemplos.

Radioterapia
El propósito de la radioterapia es matar selectivamente las células o tejidos enfermos exponiéndolos a la radiación. Se requieren dosis de radiación más altas para la terapia que para la obtención de imágenes. La fuente de radiación puede ser externa o interna.
Radioterapia externa
En la irradiación externa, la radiación de la fuente, como la coba que a menudo se utilizan, se están desarrollando otras fuentes de radiación, como el haz de protones del ciclotrón, que se han utilizado para matar tumores inoperables cerca o en el ojo, la base del cráneo o la columna vertebral. La terapia de protones utiliza un haz de protones para administrar radiación directamente al tumor.
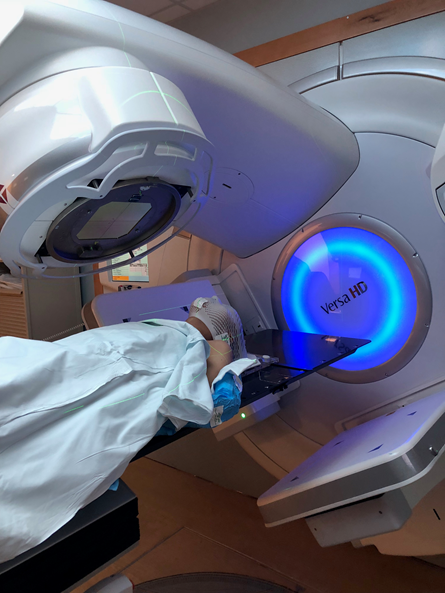
Radioterapia interna
La radioterapia interna se usa cuando se puede hacer que un radioisótopo de corta duración se concentre selectivamente en el órgano o tejido de interés. Por ejemplo, el yodo-131 es\(\ce{\beta}\) y\(\ce{\gamma}\) -emisor, se administra a un paciente, es recogido por la glándula tiroides, y se usa para tratar el hipertiroidismo. Otro ejemplo es el actinio-225, que es un\(\ce{\alpha}\) -emisor con una vida media de 10 días. El actinio-225 se instala en un anticuerpo monoclonal que se une a un antígeno prostático específico y se administra selectivamente para tratar tumores de próstata.
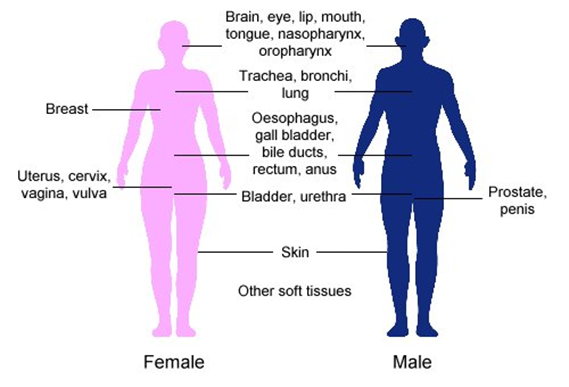
Braquiterapia
La braquiterapia o implantación de semillas es una forma de tratamiento de radiación interna que entrega una dosis alta por un corto período en comparación con el tratamiento de radiación externa. La Fig. 8.6.6 muestra los sitios en el cuerpo donde se puede usar braquiterapia para tratar el cáncer. Por ejemplo, se implantan 40 o más cápsulas de titanio, aproximadamente del tamaño de un grano de arroz (Fig. 8.6.7), para tratar el cáncer de próstata. La semilla contiene\(\ce{\gamma}\) -emisor como yodo-125 (vida media 60 días), paladio-103 (vida media 17 días), o cesio-131 (vida media 10 días). La semilla puede quedar en el cuerpo porque, debido a la corta vida media, ya no son significativamente radiactivas después del tratamiento.

Otra opción es la braquiterapia temporal, por ejemplo, se insertan agujas de iridio-192 que entregan dosis más altas de radiación para tratar el cáncer de próstata y se eliminan después de 5 a 10 min. Los alambres de iridio-192 también se utilizan como tratamiento de seguimiento después de la cirugía de cáncer de mama para matar cualquier célula cancerosa residual o recurrente. Los alambres de iridio-192 se insertan a través de un catéter implantado en el espacio desde donde se extrajo el tumor. Los cables se retiran después de entregar la dosis de radiación requerida. El proceso se repite dos veces al día durante cinco días. Se retira el catéter y no queda material radiactivo en el cuerpo después del tratamiento.


