7.5: Iones de metales de transición
- Page ID
- 70863
¿Qué tipo de moneda es esta?
La mayoría de nosotros estamos familiarizados con las monedas comunes: centavo, níquel, moneda de diez centavos, cuarto. En algunas zonas (como Las Vegas), es posible que veas grandes cantidades de dólares de plata (estos se ponen un poco pesados en tu bolsillo). Pero la mayoría de nosotros probablemente nunca hemos visto un águila platino, una moneda que representa el águila que está en poder principalmente de coleccionistas. Si llevaras un águila platino de una onza a una tienda para comprar artículos por valor de cien dólares, lo más probable es que el dueño de la tienda no te crea cuando afirmas que la moneda vale cien dólares. También sería incómodo y molesto si perdieras una de estas monedas de tu bolsillo. El platino es solo uno de varios metales de transición que vale mucho dinero (el oro es otro).
Los elementos del grupo 1 y 2 forman cationes a través de un proceso simple que implica la pérdida de uno o más electrones de la capa externa. Estos electrones provienen de la\(s\) órbita y se eliminan muy fácilmente.
Iones de metales de transición
La mayoría de los metales de transición difieren de los metales de los Grupos 1, 2 y 13 en que son capaces de formar más de un catión con diferentes cargas iónicas. Como ejemplo, el hierro comúnmente forma dos iones diferentes. A veces puede perder dos electrones para formar el\(\ce{Fe^{2+}}\) ion, mientras que en otras ocasiones pierde tres electrones para formar el\(\ce{Fe^{3+}}\) ion. El estaño y el plomo, aunque los miembros del\(p\) bloque en lugar del \(d\)bloque, también son capaces de formar múltiples iones.
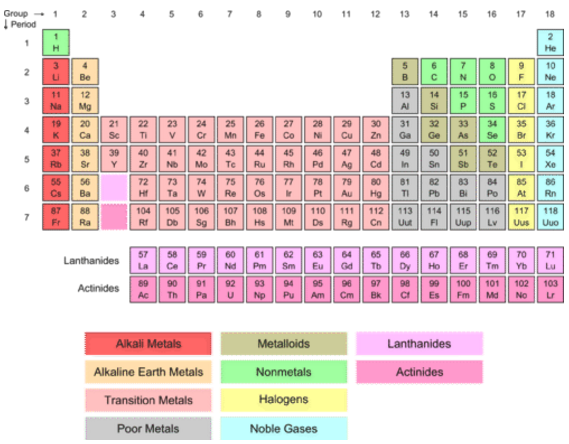
La formación iónica para los metales de transición se complica por el hecho de que estos elementos tienen\(d\) conchas internas sin llenar. Aunque los siguientes\(s\) orbitales superiores están en realidad a un nivel de energía más bajo que el\(d\) nivel, estos\(s\) electrones son los que se eliminan durante la ionización.
La siguiente tabla enumera los nombres y fórmulas de algunos de los iones comunes de metales de transición:
| Tabla\(\PageIndex{1}\): Iones comunes de metales de transición | |||
|---|---|---|---|
| \ (\ PageIndex {1}\): Iones comunes de metales de transición"> \(1+\) | \(2+\) | \(3+\) | \(4+\) |
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; ">copper (I),\(\ce{Cu^+}\) | cadmio,\(\ce{Cd^{2+}}\) | cromo (III),\(\ce{Cr^{3+}}\) | plomo (IV),\(\ce{Pb^{4+}}\) |
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; ">gold (I),\(\ce{Au^+}\) | cromo (II),\(\ce{Cr^{2+}}\) | cobalto (III),\(\ce{Co^{3+}}\) | estaño (IV),\(\ce{Sn^{4+}}\) |
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; ">mercury (I),\(\ce{Hg_2^{2+}}\) | cobalto (II),\(\ce{Co^{2+}}\) | oro (III),\(\ce{Au^{3+}}\) | |
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; ">silver,\(\ce{Ag^+}\) | cobre (II),\(\ce{Cu^{2+}}\) | hierro (III),\(\ce{Fe^{3+}}\) | |
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | hierro (II),\(\ce{Fe^{2+}}\) | ||
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | plomo (II),\(\ce{Pb^{2+}}\) | ||
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | manganeso (II),\(\ce{Mn^{2+}}\) | ||
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | mercurio (II),\(\ce{Hg^{2+}}\) | ||
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | níquel (II),\(\ce{Ni^{2+}}\) | ||
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | platino (II),\(\ce{Pt^{2+}}\) | ||
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | estaño (II),\(\ce{Sn^{2+}}\) | ||
| \ (\ PageIndex {1}\): Iones comunes de metales de transición” style="vertical-align:middle; "> | zinc,\(\ce{Zn^{2+}}\) | ||
Usos para metales de transición
Debido a que hay tantos metales en este grupo, hay una gran variedad de usos. Muchos de los metales se utilizan en la electrónica, mientras que otros (como el oro y la plata) se utilizan en sistemas monetarios. El hierro es un material estructural versátil. Cobalto, níquel, platino y otros metales se emplean como catalizadores en una serie de reacciones químicas. El zinc es un componente importante de las baterías.
Resumen
- Los metales de transición tienen capas internas de\(d\) electrones sin llenar.
- Los iones se forman principalmente a través de la pérdida de\(s\) electrones.
- Muchos metales de transición pueden formar más de un ion.
- Los metales de transición tienen una amplia variedad de aplicaciones.
Revisar
- ¿Qué tienen de único las configuraciones electrónicas de los metales de transición?
- ¿Qué electrones de elementos de metales de transición tienen más probabilidades de perderse durante la formación de iones?
- ¿Cuántos iones puede formar el hierro?
- ¿Qué metal de transición forma solo un ion?
- Enumere varios usos para los metales de transición.

