10.12: Determinación de fórmulas empíricas
- Page ID
- 71146

¿Qué ocurre en esta imagen?
En los primeros días de la química, había pocas herramientas disponibles para el estudio detallado de los compuestos. Gran parte de la información sobre la composición de los compuestos provino del análisis elemental de materiales inorgánicos. El “nuevo” campo de la química orgánica (el estudio de los compuestos de carbono) enfrentó el reto de no poder caracterizar un compuesto por completo. Se pudieron determinar las cantidades relativas de elementos, pero muchos de estos materiales tenían carbono, hidrógeno, oxígeno y posiblemente nitrógeno en proporciones simples. Los químicos no tenían forma de determinar las cantidades exactas de estos átomos que estaban contenidas en moléculas específicas.
Determinación de fórmulas empíricas
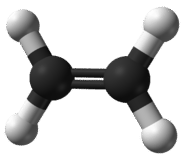
Una fórmula empírica es aquella que muestra la relación de número entero más baja de los elementos en un compuesto. Debido a que la estructura de los compuestos iónicos es una red tridimensional extendida de iones positivos y negativos, todas las fórmulas de compuestos iónicos son empíricas. Sin embargo, también podemos considerar la fórmula empírica de un compuesto molecular. El eteno es un pequeño compuesto hidrocarbonado con la fórmula\(\ce{C_2H_4}\) (ver figura a continuación). Si bien\(\ce{C_2H_4}\) es su fórmula molecular y representa su verdadera estructura molecular, tiene una fórmula empírica de\(\ce{CH_2}\). La relación más simple de carbono a hidrógeno en eteno es 1:2. Hay dos formas de ver esa relación. Considerando una molécula de eteno, la relación es de 1 átomo de carbono por cada 2 átomos de hidrógeno. Considerando un mol de eteno, la relación es de 1 mol de carbono por cada 2 moles de hidrógeno. Entonces, los subíndices en una fórmula representan la relación molar de los elementos en esa fórmula.
En un procedimiento denominado análisis elemental, un compuesto desconocido puede ser analizado en el laboratorio para determinar los porcentajes de cada elemento contenido dentro del mismo. Estos porcentajes pueden transformarse en la relación molar de los elementos, lo que lleva a la fórmula empírica. A continuación se detallan los pasos a seguir.
- Asumir una\(100 \: \text{g}\) muestra del compuesto, para que los porcentajes dados puedan convertirse directamente en gramos.
- Utilice la masa molar de cada elemento para convertir los gramos de cada elemento en moles.
- Para encontrar una relación de número entero, divida los moles de cada elemento por cualquiera de los moles del paso 2 que sea el más pequeño.
- Si todos los moles en este punto son números enteros (o muy cercanos), la fórmula empírica se puede escribir con los moles como subíndice de cada elemento.
- En algunos casos, uno o más de los moles calculados en el paso 3 no serán números enteros. Multiplica cada uno de los moles por el número entero más pequeño que convertirá cada uno en un número entero. Escribe la fórmula empírica.
Ejemplo\(\PageIndex{1}\): Determining the Empirical Formula of a Compound
Se analiza un compuesto de hierro y oxígeno y se encuentra que contiene\(69.94\%\) hierro y\(30.06\%\) oxígeno. Encuentra la fórmula empírica del compuesto.
Solución
Paso 1: Enumere las cantidades conocidas y planifique el problema.
Conocido
- \(\%\)de\(\ce{Fe} = 69.94\%\)
- \(\%\)de\(\ce{O} = 30.06\%\)
Desconocido
- Fórmula empírica = ¿Fe? O?
Los pasos a seguir se describen en el texto.
Paso 2: Calcular.
1. Asumir una\(100 \: \text{g}\) muestra.
\[69.94 \: \text{g} \: \ce{Fe}\nonumber \]
\[30.06 \: \text{g} \: \ce{O}\nonumber \]
2. Convertir a moles.
\[69.94 \: \text{g} \: \ce{Fe} \times \frac{1 \: \text{mol} \: \ce{Fe}}{55.85 \: \text{g} \: \ce{Fe}} = 1.252 \: \text{mol} \: \ce{Fe}\nonumber \]
\[30.06 \: \text{g} \: \ce{O} \times \frac{1 \: \text{mol} \: \ce{O}}{16.00 \: \text{g} \: \ce{O}} = 1.879 \: \text{mol} \: \ce{O}\nonumber \]
3. Divide ambos moles por el menor de los resultados.
\[\frac{1.252 \: \text{mol} \: \ce{Fe}}{1.252} = 1 \: \text{mol} \: \ce{Fe} \: \: \: \: \: \frac{1.879 \: \text{mol} \: \ce{O}}{1.252} = 1.501 \: \text{mol} \ce{O}\nonumber \]
4/5. Dado que los moles de todavía no\(\ce{O}\) es un número entero, ambos moles se pueden multiplicar por 2, mientras se redondean a un número entero.
\[1 \: \text{mol} \: \ce{Fe} \times 2 = 2 \: \text{mol} \: \ce{Fe} \: \: \: \: \: 1.501 \: \text{mol} \: \ce{O} \times 2 = 3 \: \text{mol} \: \ce{O}\nonumber \]
La fórmula empírica del compuesto es\(\ce{Fe_2O_3}\).
Paso 3: Piensa en tu resultado.
Los subíndices son números enteros y representan la relación molar de los elementos en el compuesto. El compuesto es el compuesto iónico óxido de hierro (III).
Resumen
- Se describe un proceso para el cálculo de la fórmula empírica para un compuesto basado en la composición porcentual de ese compuesto.
Revisar
- ¿Qué es una fórmula empírica?
- ¿Qué te dice una fórmula empírica?
- ¿Qué es lo que no te dice?

