12.2: Relaciones molares
- Page ID
- 70324
¿Qué necesita este porche?
Se quiere agregar algunas secciones al porche visto arriba. Antes de ir a la ferretería a comprar madera, es necesario determinar la composición de la unidad (el material entre dos montantes grandes). Cuenta cuántos postes, cuántas tablas, cuántos rieles; luego decide cuántas secciones desea agregar antes de calcular la cantidad de material de construcción necesario para la expansión de su porche.
Ratios Molares
Los problemas estequiométricos se pueden caracterizar por dos cosas: (1) la información dada en el problema, y (2) la información que se va a resolver, referida como la desconocida. Lo dado y lo desconocido pueden ser ambos reactivos, ambos son productos, o uno puede ser un reactivo mientras que el otro es un producto. Las cantidades de las sustancias pueden expresarse en moles. Sin embargo, en una situación de laboratorio, es común determinar la cantidad de una sustancia encontrando su masa en gramos. La cantidad de una sustancia gaseosa puede expresarse por su volumen. En este concepto, nos centraremos en el tipo de problema donde tanto las cantidades dadas como las desconocidas se expresan en moles.
Las ecuaciones químicas expresan las cantidades de reactivos y productos en una reacción. Los coeficientes de una ecuación equilibrada pueden representar el número de moléculas o el número de moles de cada sustancia. La producción de amoníaco\(\left( \ce{NH_3} \right)\) a partir de gases de nitrógeno e hidrógeno es una reacción industrial importante llamada proceso Haber, después del químico alemán Fritz Haber.
\[\ce{N_2} \left( g \right) + 3 \ce{H_2} \left( g \right) \rightarrow 2 \ce{NH_3} \left( g \right)\nonumber \]
La ecuación equilibrada se puede analizar de varias maneras, como se muestra en la siguiente figura.
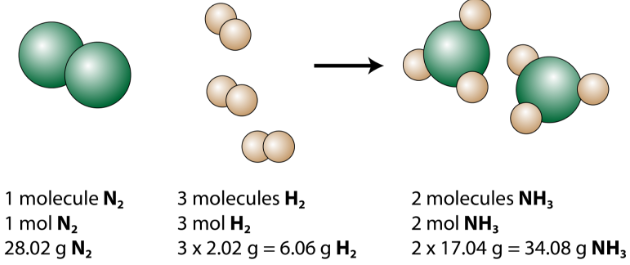
Vemos que 1 molécula de nitrógeno reacciona con 3 moléculas de hidrógeno para formar 2 moléculas de amoníaco. Esta es la cantidad relativa más pequeña posible de los reactivos y productos. Para considerar cantidades relativas mayores, cada coeficiente se puede multiplicar por el mismo número. Por ejemplo, 10 moléculas de nitrógeno reaccionarían con 30 moléculas de hidrógeno para producir 20 moléculas de amoníaco.
La cantidad más útil para contar partículas es el mol. Entonces, si cada coeficiente se multiplica por un mol, la ecuación química equilibrada nos dice que 1 mol de nitrógeno reacciona con 3 moles de hidrógeno para producir 2 moles de amoníaco. Esta es la forma convencional de interpretar cualquier ecuación química equilibrada.
Finalmente, si cada cantidad molar se convierte en gramos usando la masa molar, podemos ver que se sigue la ley de conservación de la masa. \(1 \: \ce{mol}\)de nitrógeno tiene una masa de\(28.02 \: \text{g}\), mientras que\(3 \: \text{mol}\) de hidrógeno tiene una masa de\(6.06 \: \text{g}\), y\(2 \: \text{mol}\) de amoníaco tiene una masa de\(34.08 \: \text{g}\).
\[28.02 \: \text{g} \: \ce{N_2} + 6.06 \: \text{g} \: \ce{H_2} \rightarrow 34.08 \: \text{g} \: \ce{NH_3}\nonumber \]
La masa y el número de átomos deben conservarse en cualquier reacción química. El número de moléculas no se conserva necesariamente.

Una relación molar es un factor de conversión que relaciona las cantidades en moles de dos sustancias cualesquiera en una reacción química. Los números en un factor de conversión provienen de los coeficientes de la ecuación química equilibrada. Se pueden escribir las siguientes seis relaciones molares para la reacción de formación de amoníaco anterior.
\[\begin{array}{ccc} \dfrac{1 \: \text{mol} \: \ce{N_2}}{3 \: \text{mol} \: \ce{H_2}} & or & \dfrac{3 \: \text{mol} \: \ce{H_2}}{1 \: \text{mol} \: \ce{N_2}} \\ \dfrac{1 \: \text{mol} \: \ce{N_2}}{2 \: \text{mol} \: \ce{NH_3}} & or & \dfrac{2 \: \text{mol} \: \ce{NH_3}}{1 \: \text{mol} \: \ce{N_2}} \\ \dfrac{3 \: \text{mol} \: \ce{H_2}}{2 \: \text{mol} \: \ce{NH_3}} & or & \dfrac{2 \: \text{mol} \: \ce{NH_3}}{3 \: \text{mol} \: \ce{H_2}} \end{array}\nonumber \]
En un problema de relación molar, la sustancia dada, expresada en moles, se escribe primero. Se elige el factor de conversión apropiado para convertir de moles de la sustancia dada a moles de lo desconocido.
Ejemplo\(\PageIndex{1}\): Mole Ratio
¿Cuántos moles de amoníaco se producen si se hacen reaccionar 4.20 moles de hidrógeno con un exceso de nitrógeno?
Solución
Paso 1: Enumere las cantidades conocidas y planifique el problema.
Conocido
- dado: H 2 = 4.20 mol
Desconocido
- mol de NH 3
La conversión es de\(\text{mol} \: \ce{H_2}\) a\(\text{mol} \: \ce{NH_3}\). El problema plantea que existe un exceso de nitrógeno, por lo que no necesitamos preocuparnos por ninguna relación molar que implique\(\ce{N_2}\). Elige el factor de conversión que tiene el\(\ce{NH_3}\) en el numerador y el\(\ce{H_2}\) en el denominador.
Paso 2: Resolver.
\[4.20 \: \text{mol} \: \ce{H_2} \times \dfrac{2 \: \text{mol} \: \ce{NH_3}}{3 \: \text{mol} \: \ce{H_2}} = 2.80 \: \text{mol} \: \ce{NH_3}\nonumber \]
La reacción\(4.20 \: \text{mol}\) de hidrógeno con exceso de nitrógeno produce\(2.80 \: \text{mol}\) de amoníaco.
Paso 3: Piensa en tu resultado.
El resultado corresponde a la relación 3:2 de hidrógeno a amoníaco de la ecuación equilibrada.
Resumen
- Las relaciones molares permiten comparar las cantidades de dos materiales cualesquiera en una ecuación equilibrada.
- Se pueden hacer cálculos para predecir cuánto producto se puede obtener de un número dado de moles de reactivo.
Revisar
- Si un reactivo está en exceso, ¿por qué no nos preocupamos por las relaciones molares que involucran a ese reactivo?
- ¿Cuál es la relación molar de H a N en la molécula de amoníaco?
- La fórmula para el etanol es CH 3 CH 2 OH. ¿Cuál es la relación molar de H a C en esta molécula?


