1.2: Definiciones básicas
- Page ID
- 75064
- Aprende los términos básicos utilizados para describir la materia
La definición de química —el estudio de las interacciones de la materia con otra materia y con la energía— utiliza algunos términos que también deben definirse. Iniciamos el estudio de la química definiendo términos básicos.
Materia
La materia es cualquier cosa que tenga masa y ocupe espacio. Un libro es materia, una computadora es materia, la comida es materia y la suciedad en el suelo es materia. A veces la materia puede ser difícil de identificar. Por ejemplo, el aire es materia, pero debido a que es tan delgado comparado con otra materia (por ejemplo, un libro, una computadora, comida y suciedad), a veces olvidamos que el aire tiene masa y ocupa espacio. Las cosas que no son materia incluyen pensamientos, ideas, emociones y esperanzas.
¿Cuál de los siguientes es materia y no materia?
- un hot dog
- amor
- un árbol
Solución
- Un hot dog tiene masa y ocupa espacio, por lo que es materia.
- El amor es una emoción, y las emociones no son materia.
- Un árbol tiene masa y ocupa espacio, por lo que es materia.
¿Cuál de los siguientes es materia y no materia?
- la luna
- una idea para un nuevo invento
- Contestar a
-
La luna es materia.
- Respuesta b
-
La invención en sí puede ser materia, pero la idea para ello no lo es.
Para entender la materia y cómo cambia, necesitamos ser capaces de describir la materia. Hay dos formas básicas de describir la materia: las propiedades físicas y las propiedades químicas.
Propiedades físicas
Las propiedades físicas son características que describen la materia tal como existe. Algunas características físicas de la materia son la forma, el color, el tamaño y la temperatura. Una propiedad física importante es la fase (o estado) de la materia. Las tres fases fundamentales de la materia son sólida, líquida y gaseosa (Figura\(\PageIndex{1}\)).

Propiedades Químicas
Las propiedades químicas son características de la materia que describen cómo se forman los cambios de la materia en presencia de otra materia. ¿Se quema una muestra de materia? La quema es una propiedad química. ¿Se comporta violentamente cuando se pone en el agua? Esta reacción también es una propiedad química (Figura\(\PageIndex{2}\)). En los siguientes capítulos, veremos cómo las descripciones de las propiedades físicas y químicas son aspectos importantes de la química.

Cambio Físico
Un cambio físico ocurre cuando una muestra de materia cambia una o más de sus propiedades físicas. Por ejemplo, un sólido puede fundirse (Figura\(\PageIndex{3}\)), o el alcohol en un termómetro puede cambiar de volumen a medida que cambia la temperatura. Un cambio físico no afecta la composición química de la materia.

Cambio Químico
El cambio químico es el proceso de demostrar una propiedad química, como el fósforo de combustión en la Figura\(\PageIndex{2}\) “Propiedades Químicas”. A medida que se quema la materia en el fósforo, su composición química cambia y se crean nuevas formas de materia con nuevas propiedades físicas. Tenga en cuenta que los cambios químicos suelen ir acompañados de cambios físicos, ya que la nueva materia probablemente tendrá diferentes propiedades físicas de la materia original.
Describir cada proceso como un cambio físico o un cambio químico.
- El agua en el aire se convierte en nieve.
- Se corta el pelo de una persona.
- La masa de pan se convierte en pan fresco en un horno.
Solución
- Debido a que el agua va de una fase gaseosa a una fase sólida, esto es un cambio físico.
- Tu cabello largo se está acortando. Esto es un cambio físico.
- Debido a la temperatura del horno, se están produciendo cambios químicos en la masa de pan para hacer pan fresco. Estos son cambios químicos. (De hecho, mucha cocción implica cambios químicos).
Identificar cada proceso como un cambio físico o un cambio químico.
- Un fuego está arrasando en una chimenea.
- El agua se calienta para hacer una taza de café.
- Contestar a
-
cambio químico
- Respuesta b
-
cambio físico
Sustancia
Una muestra de materia que tiene las mismas propiedades físicas y químicas en todo momento se llama sustancia. A veces se usa la frase sustancia pura, pero no se necesita la palabra pura. La definición del término sustancia es un ejemplo de cómo la química tiene una definición específica para una palabra que se usa en el lenguaje cotidiano con una definición diferente, más vaga. Aquí, usaremos el término sustancia con su estricta definición química.
La química reconoce dos tipos diferentes de sustancias: elementos y compuestos.
Elemento
Un elemento es el tipo de sustancia química más simple; no se puede descomponer en sustancias químicas más simples por medios químicos ordinarios. Hay 118 elementos conocidos por la ciencia, de los cuales 80 son estables. (Los demás elementos son radiactivos, condición que consideraremos en el Capítulo 15.) Cada elemento tiene su propio conjunto único de propiedades físicas y químicas. Ejemplos de elementos incluyen hierro, carbono y oro.
Compuesto
Un compuesto es una combinación de más de un elemento. Las propiedades físicas y químicas de un compuesto son distintas de las propiedades físicas y químicas de sus elementos constituyentes; es decir, se comporta como una sustancia completamente diferente. Se conocen más de 50 millones de compuestos, y a diario se descubren más. Los ejemplos de compuestos incluyen agua, penicilina y cloruro de sodio (el nombre químico de la sal común de mesa).
Mezclas
Las combinaciones físicas de más de una sustancia se denominan mezclas. Elementos y compuestos no son las únicas formas en que la materia puede estar presente. Frecuentemente encontramos objetos que son combinaciones físicas de más de un elemento o mezclas compuestas. Hay dos tipos de mezclas.
Mezcla heterogénea
Una mezcla heterogénea es una mezcla compuesta por dos o más sustancias. Es fácil decir, a veces a simple vista, que hay más de una sustancia presente.
Mezcla/Solución Homogénea
Una mezcla homogénea es una combinación de dos o más sustancias que está tan íntimamente mezclada, que la mezcla se comporta como una sola sustancia. Otra palabra para una mezcla homogénea es una solución. Así, una combinación de sal y lana de acero es una mezcla heterogénea porque es fácil ver qué partículas de la materia son cristales de sal y cuáles son lana de acero. Por otro lado, si tomas cristales de sal y los disuelves en agua, es muy difícil saber que tienes más de una sustancia presente con solo mirar—aunque uses un microscopio potente. La sal disuelta en agua es una mezcla homogénea, o una solución (Figura\(\PageIndex{3}\)).

Identificar las siguientes combinaciones como mezclas heterogéneas o mezclas homogéneas.
- agua de soda (el dióxido de carbono se disuelve en agua)
- una mezcla de limaduras metálicas de hierro y polvo de azufre (tanto el hierro como el azufre son elementos)
Solución
- Debido a que el dióxido de carbono se disuelve en agua, podemos inferir del comportamiento de los cristales de sal disueltos en agua que el dióxido de carbono disuelto en agua es (también) una mezcla homogénea.
- Suponiendo que el hierro y el azufre simplemente se mezclan entre sí, debería ser fácil ver qué es hierro y qué es azufre, por lo que esta es una mezcla heterogénea.
- el cuerpo humano
- una amalgama, una combinación de algunos otros metales disueltos en una pequeña cantidad de mercurio
- Contestar a
-
mezcla heterogénea
- Respuesta b
-
mezcla homogénea
Hay otros descriptores que podemos usar para describir la materia, especialmente los elementos. Por lo general, podemos dividir elementos en metales y no metales, y cada conjunto comparte ciertas propiedades (pero no siempre todas).
Metal
Un metal es un elemento que conduce bien la electricidad y el calor y es brillante, plateado, sólido, dúctil y maleable. A temperatura ambiente, los metales son sólidos (aunque el mercurio es una excepción bien conocida). Un metal es dúctil porque puede ser dibujado en alambres delgados (una propiedad llamada ductilidad); y maleable porque puede ser machacado en láminas delgadas (una propiedad llamada maleabilidad).
No metálico
Un no metal es un elemento que es quebradizo cuando es sólido, y no conduce muy bien la electricidad ni el calor. Los no metales no se pueden convertir en láminas delgadas o alambres (Figura\(\PageIndex{4}\)). Los no metales también existen en una variedad de fases y colores a temperatura ambiente.
Semimetales
Algunos elementos tienen propiedades tanto de metales como de no metales y se denominan semimetales (o metaloides). Veremos más adelante cómo estas descripciones se pueden asignar con bastante facilidad a diversos elementos.

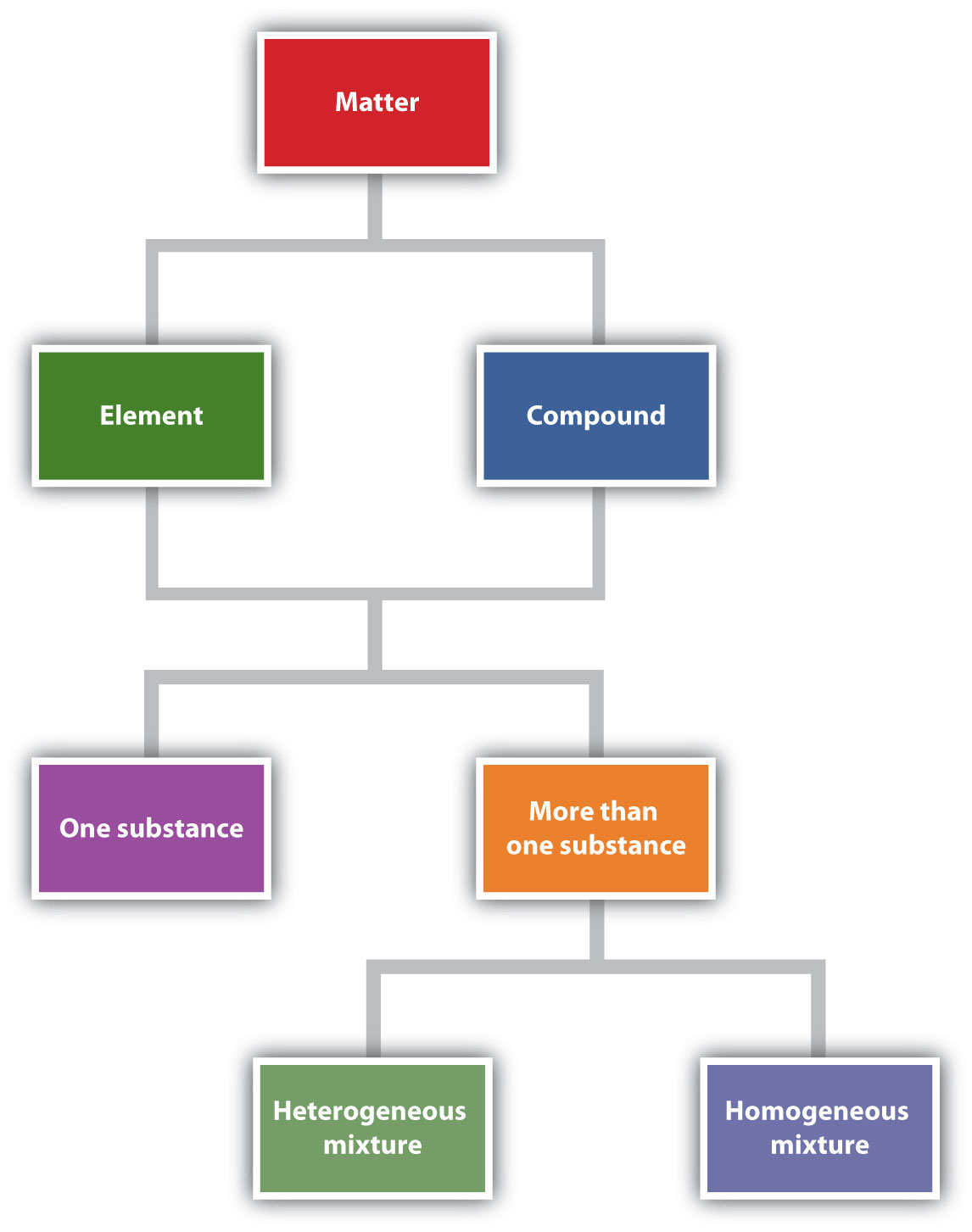
Diagrama de flujo de descripción
“Describiendo la materia” es un diagrama de flujo de las relaciones entre las diferentes formas de describir la materia.
La mayoría de las personas tienen un ritual matutino, un proceso por el que pasan todas las mañanas para prepararse para el día. La química aparece en muchas de estas actividades.
- Si te das una ducha o un baño por la mañana, probablemente uses jabón, champú, o ambos. Estos artículos contienen químicos que interactúan con el aceite y la suciedad de tu cuerpo y pelo para eliminarlos y lavarlos. Muchos de estos productos también contienen químicos que te hacen oler bien; se llaman fragancias.
- Cuando te cepillas los dientes por la mañana, usualmente usas pasta de dientes, una forma de jabón, para limpiarte los dientes. Las pastas dentales suelen contener partículas diminutas y duras llamadas abrasivos que frotan físicamente los dientes. Muchas pastas dentales también contienen flúor, una sustancia que interactúa químicamente con la superficie de los dientes para ayudar a prevenir las caries.
- Quizás tomes vitaminas, suplementos o medicamentos todas las mañanas. Las vitaminas y otros suplementos contienen los químicos que su cuerpo necesita en pequeñas cantidades para funcionar correctamente. Los medicamentos son químicos que ayudan a combatir enfermedades y promover la salud.
- A lo mejor haces algunos huevos fritos para el desayuno. Freír los huevos implica calentarlos lo suficiente para que se produzca una reacción química para cocinar los huevos.
- Después de comer, la comida en su estómago reacciona químicamente para que el cuerpo (principalmente los intestinos) pueda absorber alimentos, agua y otros nutrientes.
- Si conduces o tomas el autobús a la escuela o al trabajo, estás usando un vehículo que probablemente quema gasolina, un material que se quema con bastante facilidad y proporciona energía para alimentar el vehículo. Recordemos que la quema es un cambio químico.
Estos son solo algunos ejemplos de cómo la química impacta tu vida cotidiana. ¡Y aún no hemos llegado a almorzar!

Claves para llevar
- La química es el estudio de la materia y sus interacciones con otra materia y energía.
- La materia es cualquier cosa que tenga masa y ocupe espacio.
- La materia puede describirse en términos de propiedades físicas y químicas.
- Las propiedades físicas y químicas de la materia pueden cambiar.
- La materia se compone de elementos y compuestos.
- Las combinaciones de diferentes sustancias se llaman mezclas.
- Los elementos pueden describirse como metales, no metales y semimetales.


