6.2: Nucleofilicidad de\(\mathrm{ROH}\), \(\mathrm{RSH}\), and \(\mathrm{RNH}_{2}\)
- Page ID
- 76995
Anteriormente (Capítulos\(1\) y\(4\)), discutimos (en gran profundidad) que los tres grupos funcionales (\({}^{-}\mathrm{OH}\)\({}^{-}\mathrm{NH}\),, y\({}^{-}\mathrm{SH}\)) son nucleofílicos: es decir, reaccionarán en el centro de carbono que es deficiente en electrones. Para los grupos funcionales que contienen centros nucleofílicos de la misma fila de la tabla periódica, las tendencias en la nucleofilia son paralelas a la basicidad de Bronsted: las aminas son más nucleofílicas (y básicas) que las alcoholes. Sin embargo, en los grupos funcionales que contienen centros nucleofílicos del mismo grupo de la tabla periódica (la nucleofilia aumenta a lo largo del grupo, mientras que la basicidad disminuye), los tioles son más nucleofílicos que los alcoholes. Tanto las aminas como los tioles son muy nucleofílicos. Los tres grupos participan en sustituciones nucleofílicas como se discute en Capítulos\(1\) y\(4\).
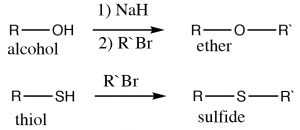
Ejemplos de este tipo de sustituciones nucleofílicas son las reacciones de alcoholes, tioles y aminas con haluros de alquilo para dar los correspondientes éteres, sulfuros y aminas (secundarias, terciarias o cuaternarias). Los alcoholes no son tan nucleofílicos como los tioles y las aminas, por lo que normalmente se debe usar el alcóxido correspondiente (porque es más reactivo), para la síntesis de éteres.
En el caso de las aminas, el nitrógeno puede reaccionar varias veces con el electrófilo (haluro de alquilo), y en la práctica es difícil detener la reacción en cualquier etapa intermedia (en el laboratorio).
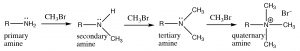
Las aminas reaccionan típicamente con electrófilos para dar aminas polialquiladas


