13.10: Curvas de Presión de Vapor
- Page ID
- 70418
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)¿Cuál es la forma más rápida de hervir agua?
Una de las primeras lecciones de cocina es cómo hervir el agua. Sí, suena simple, pero hay un par de pistas que aceleran las cosas. Un indicio es poner una tapa en la olla. La imagen de arriba tiene agua hirviendo descubierta con el vapor escapando a la atmósfera. Si la tapa está en la olla, se hervirá menos agua y el agua hervirá más rápido. La acumulación de presión dentro de la olla ayuda a acelerar el proceso de ebullición.
Curvas de presión de vapor
Los puntos de ebullición de varios líquidos se pueden ilustrar en una curva de presión de vapor (figura a continuación). Una curva de presión de vapor es una gráfica de la presión de vapor en función de la temperatura. Para encontrar el punto de ebullición normal del líquido, se dibuja una línea horizontal desde el eje y a una presión igual a la presión estándar. Se puede trazar una línea vertical que comienza en el eje x conectada al punto en el que se cruzan la presión estándar y la curva de presión de vapor de un líquido, la temperatura correspondiente es el punto de ebullición de ese líquido.
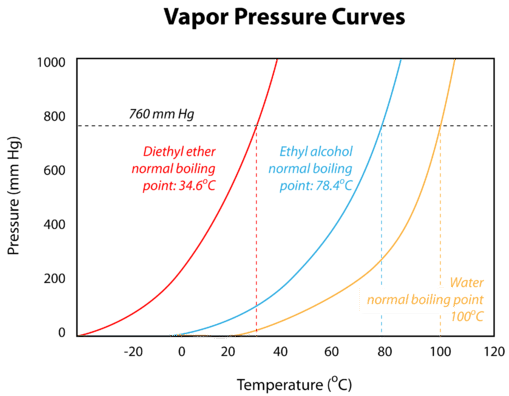
El punto de ebullición de un líquido también se correlaciona con la fuerza de sus fuerzas intermoleculares. Recordemos que el éter dietílico tiene fuerzas de dispersión débiles, lo que significa que el líquido tiene una alta presión de vapor. Las fuerzas débiles también significan que no requiere un gran aporte de energía para hacer hervir el éter dietílico, por lo que tiene un punto de ebullición normal relativamente bajo de\(34.6^\text{o} \text{C}\). El agua, con su enlace de hidrógeno mucho más fuerte, tiene una baja presión de vapor y un punto de ebullición normal más alto de\(100^\text{o} \text{C}\).
Como se indicó anteriormente, los puntos de ebullición se ven afectados por la presión externa. A mayores altitudes, la presión atmosférica es menor. Con menos presión empujando hacia abajo sobre la superficie del líquido, hierve a una temperatura más baja. Esto también se puede ver a partir de las curvas de presión de vapor. Si se dibuja una línea horizontal a una presión de vapor más baja, se cruza con cada curva a una temperatura más baja. El punto de ebullición del agua está\(100^\text{o} \text{C}\) al nivel del mar, donde la presión atmosférica es estándar. En Denver, Colorado\(1600 \: \text{m}\) sobre el nivel del mar, la presión atmosférica es de aproximadamente\(640 \: \text{mm} \: \ce{Hg}\) y el agua hierve a aproximadamente\(95^\text{o} \text{C}\). En la cima del monte. Everest, la presión atmosférica es de aproximadamente\(255 \: \text{mm} \: \ce{Hg}\), y el agua hierve solo en\(70^\text{o} \text{C}\). Por otro lado, el agua hierve a mayor que\(100^\text{o} \text{C}\) si la presión externa es superior a la estándar. Las ollas a presión no permiten que el vapor escape y la presión de vapor aumenta. Dado que el agua en una olla a presión hierve a una temperatura superior\(100^\text{o} \text{C}\), la comida se cocina más rápidamente.

El efecto de la disminución de la presión de aire se puede demostrar colocando un vaso de precipitados de agua en una cámara de vacío. A una presión lo suficientemente baja, aproximadamente\(20 \: \text{mm} \: \ce{Hg}\), el agua hervirá a temperatura ambiente.
Resumen
- Una curva de presión de vapor es una gráfica de la presión de vapor en función de la temperatura.
- Los puntos de ebullición se ven afectados por la presión externa.
Revisar
- ¿Qué muestra una curva de presión de vapor?
- ¿Por qué el éter dietílico tiene un punto de ebullición bajo?
- ¿Qué fuerzas intermoleculares mantienen unidas las moléculas de agua?
- ¿Por qué hierve el agua a una temperatura más baja cuando se encuentra a gran altitud?
Explora más
Utilice el siguiente recurso para responder a las preguntas que siguen.
- ¿Qué hace una bomba de vacío?
- ¿Cuál es el papel de la junta tórica?
- ¿Qué sucede cuando se enciende la bomba de vacío?
- ¿Qué pasó cuando se encendió la bomba de vacío?
- ¿Cuál era la temperatura de esta agua hirviendo?


