19.2: Músculo Cardíaco y Actividad Eléctrica
- Page ID
- 123118
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Objetivos de aprendizaje
- Describir la estructura del músculo cardíaco
- Identificar y describir los componentes del sistema de conducción que distribuye los impulsos eléctricos a través del corazón
- Comparar el efecto del movimiento iónico sobre el potencial de membrana de las células conductoras y contráctiles cardíacas
- Relacionar características de un electrocardiograma con eventos en el ciclo cardíaco
- Identificar bloqueos que pueden interrumpir el ciclo cardíaco
Recordemos que el músculo cardíaco comparte algunas características tanto con el músculo esquelético como con el músculo liso, pero tiene algunas propiedades únicas propias. No menos importante de estas propiedades excepcionales es su capacidad para iniciar un potencial eléctrico a una velocidad fija que se propaga rápidamente de célula a celda para activar el mecanismo contráctil. Esta propiedad se conoce como autorritmicidad. Ni el músculo liso ni el esquelético pueden hacer esto. A pesar de que el músculo cardíaco tiene autorritmicidad, la frecuencia cardíaca es modulada por los sistemas endocrino y nervioso.
Hay dos tipos principales de células del músculo cardíaco: las células contráctiles miocárdicas y las células conductoras del miocardio. Las células contráctiles miocárdicas constituyen la masa (99 por ciento) de las células en las aurículas y los ventrículos. Las células contráctiles conducen impulsos y son responsables de las contracciones que bombean sangre a través del cuerpo. Las células conductoras miocárdicas (1 por ciento de las células) forman el sistema de conducción del corazón. A excepción de las células de Purkinje, generalmente son mucho más pequeñas que las células contráctiles y tienen pocas de las miofibrillas o filamentos necesarios para la contracción. Su función es similar en muchos aspectos a las neuronas, aunque son células musculares especializadas. Las células de conducción miocárdica inician y propagan el potencial de acción (el impulso eléctrico) que viaja por todo el corazón y desencadena las contracciones que impulsan la sangre.
Estructura del Músculo Cardíaco
En comparación con los cilindros gigantes del músculo esquelético, las células del músculo cardíaco o los cardiomiocitos, son considerablemente más cortas con diámetros mucho más pequeños. El músculo cardíaco también demuestra estrías, el patrón alterno de bandas A oscuras y bandas I claras atribuidas a la disposición precisa de los mifilamentos y fibrillas que se organizan en sarcómeros a lo largo de la célula (Figura\(\PageIndex{1}\) .a). Estos elementos contráctiles son prácticamente idénticos al músculo esquelético. Los túbulos T (transversales) penetran desde la membrana plasmática superficial, el sarcolema, hasta el interior de la célula, permitiendo que el impulso eléctrico llegue al interior. Los túbulos T solo se encuentran en los discos Z, mientras que en el músculo esquelético, se encuentran en la unión de las bandas A e I. Por lo tanto, hay la mitad de túbulos T en el músculo cardíaco que en el músculo esquelético. Además, el retículo sarcoplásmico almacena pocos iones de calcio, por lo que la mayoría de los iones de calcio deben provenir de fuera de las células. El resultado es un inicio más lento de la contracción. Las mitocondrias son abundantes, proporcionando energía para las contracciones del corazón. Por lo general, los cardiomiocitos tienen un solo núcleo central, pero en algunas células se pueden encontrar dos o más núcleos.
Las células del músculo cardíaco se ramifican libremente. Una unión entre dos células colindantes está marcada por una estructura crítica llamada disco intercalado, que ayuda a soportar la contracción sincronizada del músculo (Figura\(\PageIndex{1}\) .b). Los sarcolemas de las células adyacentes se unen en los discos intercalados. Consisten en desmosomas, proteoglicanos de enlace especializados, uniones estrechas y grandes cantidades de uniones gap que permiten el paso de iones entre las células y ayudan a sincronizar la contracción (Figura\(\PageIndex{1}\) .c). El tejido conectivo intercelular también ayuda a unir las células. La importancia de unir fuertemente estas células entre sí es necesaria por las fuerzas ejercidas por la contracción.
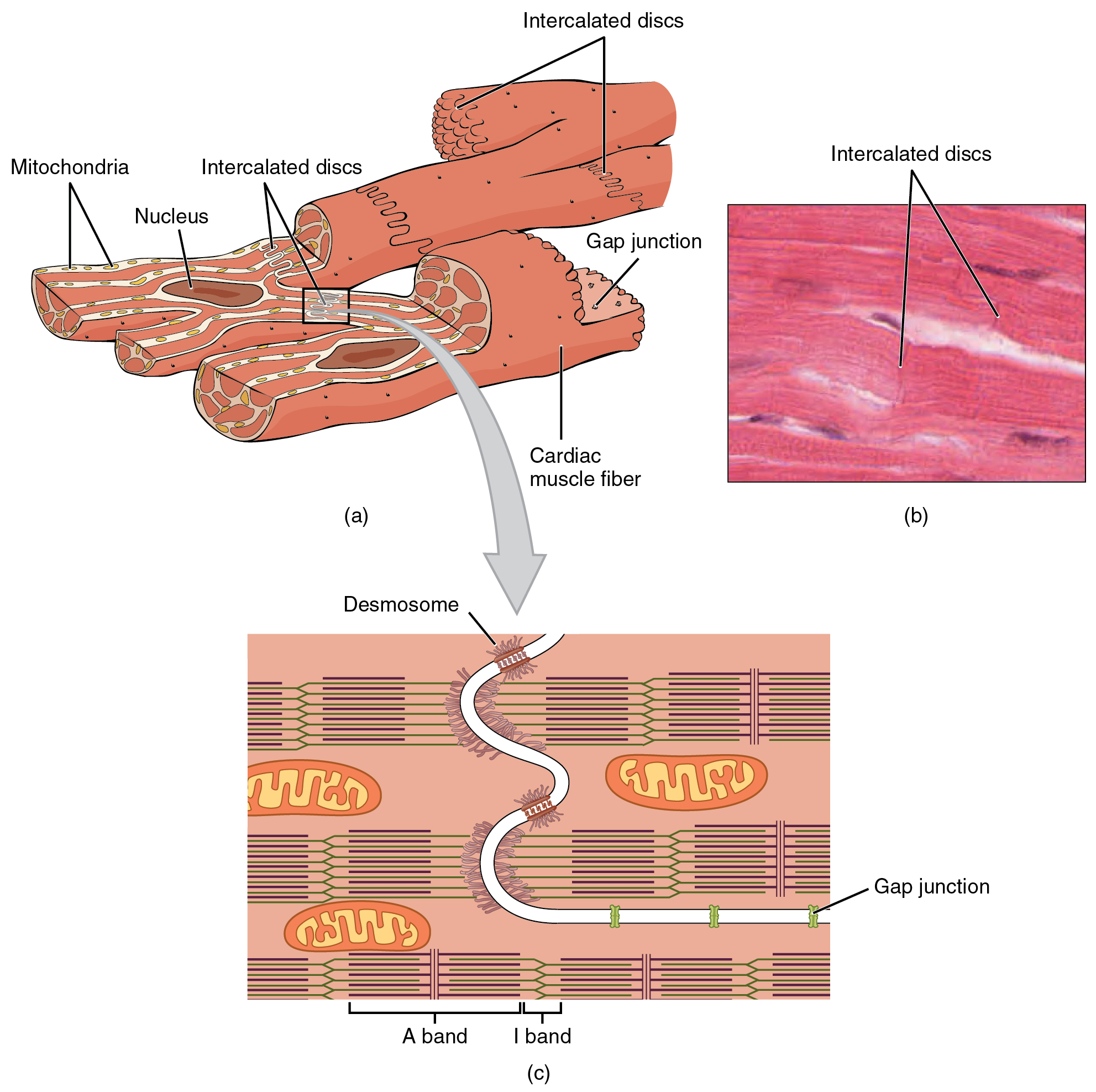
El músculo cardíaco experimenta patrones de respiración aeróbica, principalmente metabolizando lípidos e hidratos de carbono. La mioglobina, los lípidos y el glucógeno se almacenan dentro del citoplasma. Las células del músculo cardíaco sufren contracciones tipo contracciones con largos períodos refractarios seguidos de breves períodos de relajación. La relajación es esencial para que el corazón pueda llenarse de sangre para el siguiente ciclo. El periodo refractario es muy largo para evitar la posibilidad de tetanía, condición en la que el músculo permanece contraído involuntariamente. En el corazón, la tetanía no es compatible con la vida, ya que evitaría que el corazón bombee sangre.
CONEXIÓN DIARIA
Reparación y Repuesto
Las células del músculo cardíaco dañadas tienen capacidades extremadamente limitadas para repararse o reemplazar las células muertas a través de la mitosis. Evidencias recientes indican que al menos algunas células madre permanecen dentro del corazón que continúan dividiéndose y al menos potencialmente reemplazando a estas células muertas. Sin embargo, las células recién formadas o reparadas rara vez son tan funcionales como las células originales, y la función cardíaca se reduce. En caso de un ataque al corazón o IM, las células muertas a menudo son reemplazadas por parches de tejido cicatricial. Las autopsias realizadas en individuos que habían recibido exitosamente trasplantes de corazón muestran cierta proliferación de células originales. Si los investigadores pueden desbloquear el mecanismo que genera nuevas células y restaurar las capacidades mitóticas completas al músculo cardíaco, el pronóstico para los sobrevivientes de un ataque cardíaco se verá enormemente mejorado. Hasta la fecha, las células miocárdicas producidas dentro del paciente (in situ) por las células madre cardíacas parecen no funcionales, aunque las cultivadas en cajas de Petri (in vitro) sí latieron. Quizás pronto se resuelva este misterio, y los nuevos avances en el tratamiento serán comunes.
Sistema de Conducción del Corazón
Si las células cardíacas embrionarias se separan en una placa de Petri y se mantienen vivas, cada una es capaz de generar su propio impulso eléctrico seguido de contracción. Cuando se colocan juntas dos células embrionarias del músculo cardíaco que late independientemente, la célula con la tasa inherente más alta marca el ritmo, y el impulso se propaga de la célula más rápida a la más lenta para desencadenar una contracción. A medida que se unen más celdas, la celda más rápida continúa asumiendo el control de la velocidad. Un corazón adulto completamente desarrollado mantiene la capacidad de generar su propio impulso eléctrico, desencadenado por las células más rápidas, como parte del sistema de conducción cardíaca. Los componentes del sistema de conducción cardíaca incluyen el nódulo sinoauricular, el nódulo auriculoventricular, el haz auriculoventricular, las ramas del haz auriculoventricular y las células de Purkinje (Figura\(\PageIndex{2}\)).
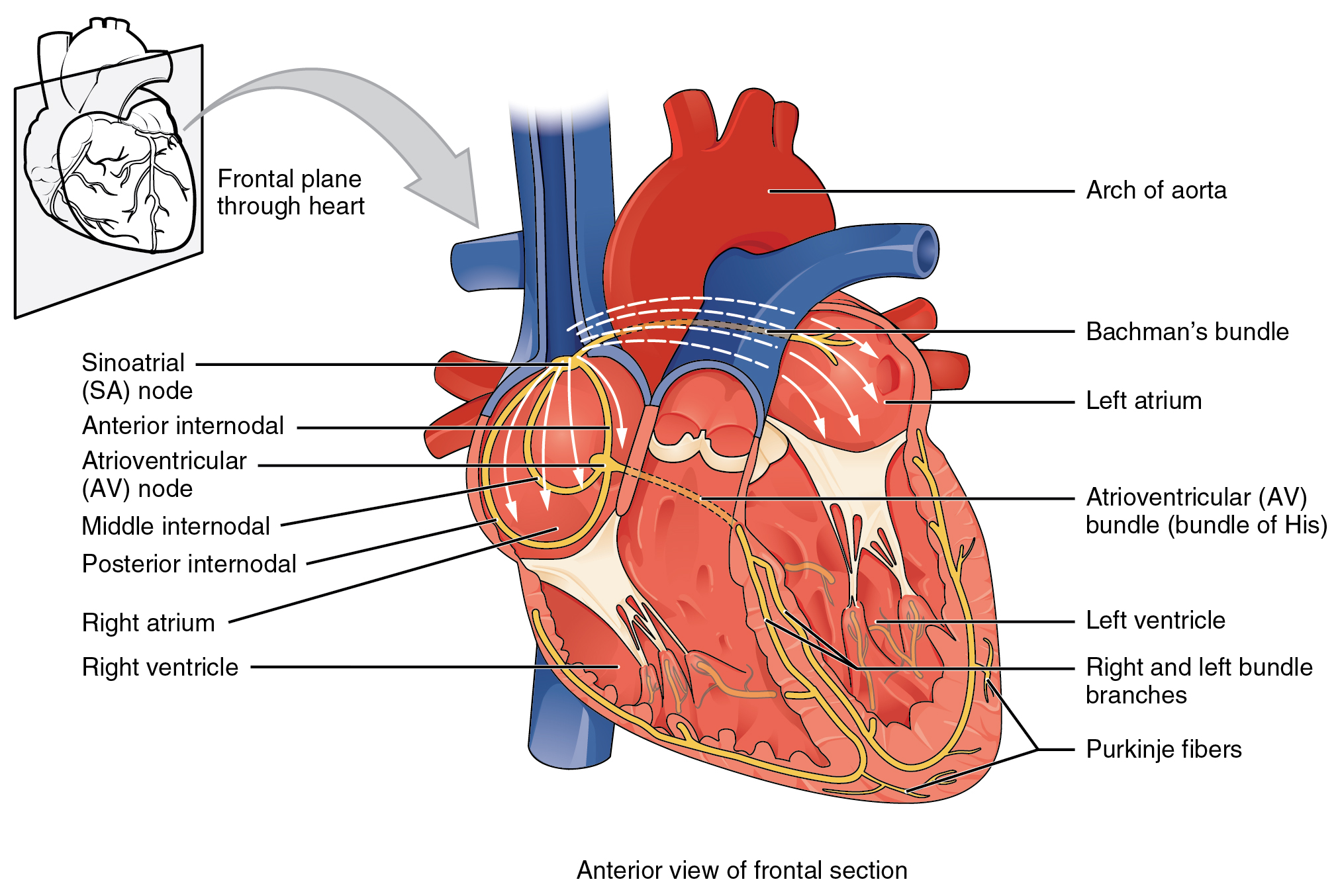
Nodo sinoauricular (SA)
El ritmo cardíaco normal es establecido por el nódulo sinoauricular (SA), un grupo especializado de células conductoras miocárdicas localizadas en las paredes superior y posterior de la aurícula derecha muy cerca del orificio de la vena cava superior. El nodo SA tiene la mayor tasa inherente de despolarización y es conocido como el marcapasos del corazón. Inicia el ritmo sinusal, o patrón eléctrico normal seguido de contracción del corazón.
Este impulso se propaga desde su inicio en el nódulo SA a lo largo de las aurículas a través de vías internodales especializadas, hasta las células contráctiles miocárdicas auriculares y el nódulo auriculoventricular. Las vías internodales constan de tres bandas (anterior, media y posterior) que conducen directamente desde el nódulo SA hasta el siguiente nodo en el sistema de conducción, el nódulo auriculoventricular (ver Figura\(\PageIndex{2}\)). El impulso tarda aproximadamente 50 ms (milisegundos) en viajar entre estos dos nodos. La importancia relativa de esta vía se ha debatido ya que el impulso alcanzaría el nódulo auriculoventricular simplemente siguiendo la vía célula por célula a través de las células contráctiles del miocardio en las aurículas. Además, existe una vía especializada llamada haz de Bachmann o banda interauricular que conduce el impulso directamente desde la aurícula derecha a la aurícula izquierda. Independientemente de la vía, a medida que el impulso llega al tabique auriculoventricular, el tejido conectivo del esqueleto cardíaco evita que el impulso se extienda a las células miocárdicas en los ventrículos excepto en el nódulo auriculoventricular. La figura\(\PageIndex{3}\) ilustra el inicio del impulso en el nódulo SA que luego extiende el impulso a lo largo de las aurículas hasta el nódulo auriculoventricular.
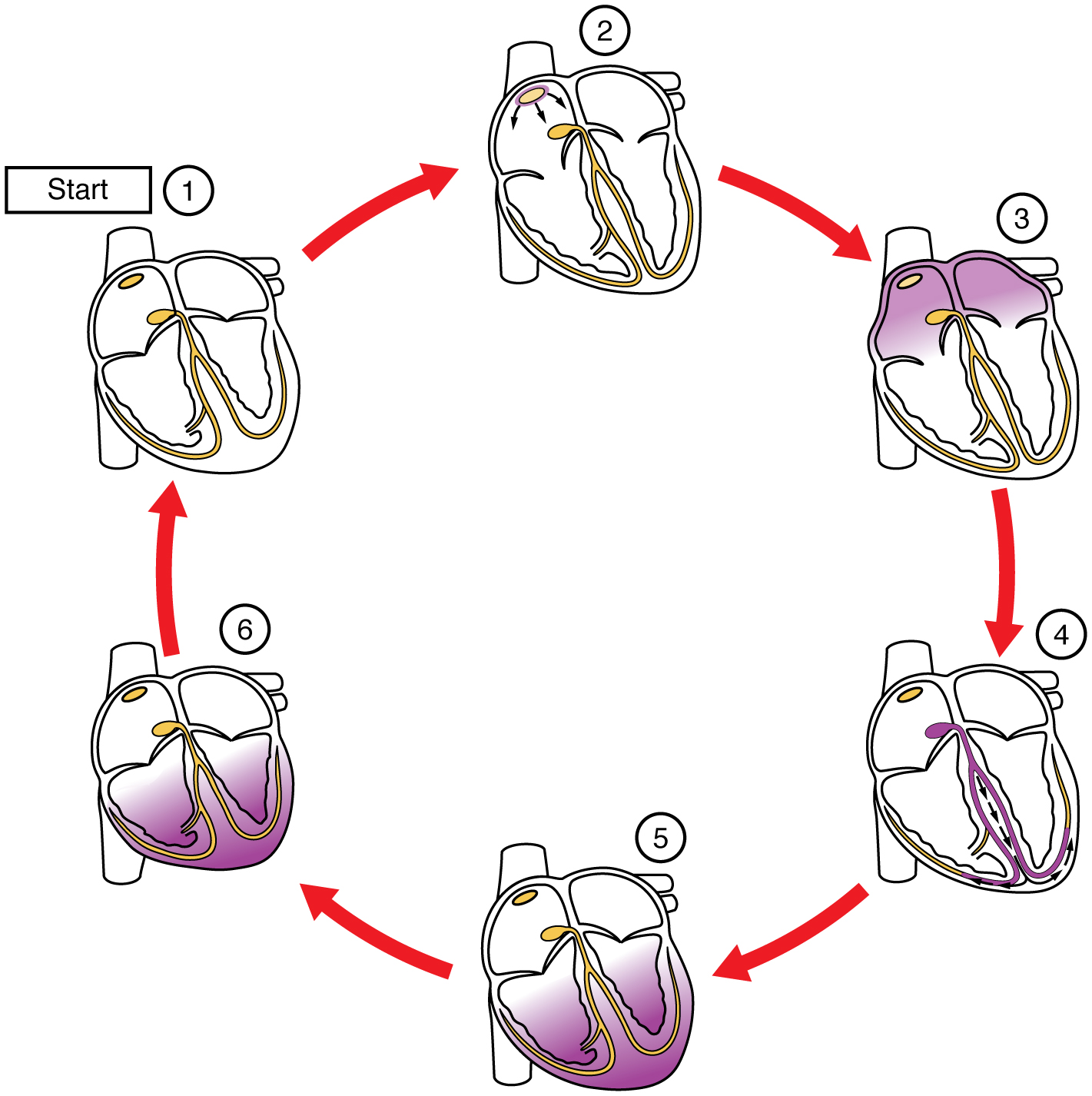
El evento eléctrico, la onda de despolarización, es el detonante de la contracción muscular. La onda de despolarización comienza en la aurícula derecha, y el impulso se extiende a través de las porciones superiores de ambas aurículas y luego hacia abajo a través de las células contráctiles. Luego, las células contráctiles comienzan a contraerse desde las porciones superiores a las inferiores de las aurículas, bombeando sangre de manera eficiente hacia los ventrículos.
Nodo auriculoventricular (AV)
El nódulo auriculoventricular (AV) es un segundo grupo de células conductoras miocárdicas especializadas, ubicadas en la porción inferior de la aurícula derecha dentro del tabique auriculoventricular. El tabique evita que el impulso se extienda directamente a los ventrículos sin pasar por el nódulo AV. Hay una pausa crítica antes de que el nodo AV se despolarice y transmita el impulso al haz auriculoventricular (ver Figura\(\PageIndex{3}\), paso 3). Este retraso en la transmisión es parcialmente atribuible al pequeño diámetro de las celdas del nodo, que ralentizan el impulso. Además, la conducción entre células nodales es menos eficiente que entre células conductoras. Estos factores significan que el impulso tarda aproximadamente 100 ms en pasar por el nodo. Esta pausa es crítica para la función cardíaca, ya que permite que los cardiomiocitos auriculares completen su contracción que bombea sangre hacia los ventrículos antes de que el impulso se transmita a las células del ventrículo mismo. Con estimulación extrema por el nodo SA, el nodo AV puede transmitir impulsos al máximo a 220 por minuto. Esto establece la frecuencia cardíaca máxima típica en un individuo joven y sano. Los corazones dañados o los estimulados por las drogas pueden contraerse a tasas más altas, pero a estos ritmos, el corazón ya no puede bombear sangre de manera efectiva.
Paquete auriculoventricular (haz de His), ramas de haz y fibras de Purkinje
Surgido del nódulo AV, el haz auriculoventricular, o haz de His, procede a través del tabique interventricular antes de dividirse en dos ramas del haz auriculoventricular, comúnmente llamadas ramas izquierda y derecha del haz. La rama izquierda del haz tiene dos fascículos. La rama izquierda del haz abastece el ventrículo izquierdo, y el haz derecho ramifica el ventrículo derecho. Dado que el ventrículo izquierdo es mucho más grande que el derecho, la rama del haz izquierdo también es considerablemente más grande que la derecha. Porciones de la rama derecha del haz se encuentran en la banda moderadora y abastecen los músculos papilares derechos. Debido a esta conexión, cada músculo papilar recibe el impulso aproximadamente al mismo tiempo, por lo que comienzan a contraerse simultáneamente justo antes del resto de las células contráctiles miocárdicas de los ventrículos. Se cree que esto permite que se desarrolle tensión en las cuerdas tendinosas antes de la contracción ventricular derecha. No hay banda de moderadores correspondiente a la izquierda. Ambas ramas del haz descienden y alcanzan el ápice del corazón donde se conectan con las fibras de Purkinje (ver Figura\(\PageIndex{3}\), paso 4). Este pasaje toma aproximadamente 25 ms.
Las fibras de Purkinje son fibras conductoras miocárdicas adicionales que propagan el impulso a las células contráctiles miocárdicas en los ventrículos. Se extienden por todo el miocardio desde el ápice del corazón hacia el tabique auriculoventricular y la base del corazón. Las fibras de Purkinje tienen una velocidad de conducción inherente rápida, y el impulso eléctrico alcanza todas las células musculares ventriculares en aproximadamente 75 ms (ver Figura\(\PageIndex{3}\), paso 5). Dado que el estímulo eléctrico comienza en el ápice, la contracción también comienza en el ápice y viaja hacia la base del corazón, similar a apretar un tubo de pasta de dientes desde el fondo. Esto permite que la sangre sea bombeada fuera de los ventrículos y hacia la aorta y el tronco pulmonar. El tiempo total transcurrido desde el inicio del impulso en el nodo SA hasta la despolarización de los ventrículos es de aproximadamente 225 ms.
Potenciales de membrana y movimiento iónico en células conductoras cardíacas
Los potenciales de acción son considerablemente diferentes entre las células conductoras cardíacas y las células contractivas cardíacas. Mientras que Na + y K + desempeñan papeles esenciales, Ca 2 + también es crítico para ambos tipos de células. A diferencia de los músculos esqueléticos y las neuronas, las células conductoras cardíacas no tienen un potencial de reposo estable. Las células conductoras contienen una serie de canales iónicos de sodio que permiten una afluencia normal y lenta de iones de sodio que hace que el potencial de la membrana aumente lentamente desde un valor inicial de −60 mV hasta aproximadamente —40 mV. El movimiento resultante de los iones de sodio crea una despolarización espontánea (o despolarización prepotencial). En este punto, los canales de iones calcio se abren y Ca 2 + ingresa a la célula, despolarizándola aún más a una velocidad más rápida hasta alcanzar un valor de aproximadamente +5 mV. En este punto, los canales de iones calcio se cierran y los canales K + se abren, permitiendo el flujo de salida de K + y dando como resultado una repolarización. Cuando el potencial de membrana alcanza aproximadamente −60 mV, los canales K + se cierran y los canales de Na + se abren, y la fase prepotencial comienza de nuevo. Este fenómeno explica las propiedades de autorritmicidad del músculo cardíaco (Figura\(\PageIndex{4}\)).

Potenciales de membrana y movimiento iónico en células contráctiles cardíacas
Hay un patrón eléctrico claramente diferente que involucra las células contráctiles. En este caso, hay una rápida despolarización, seguida de una fase de meseta y luego repolarización. Este fenómeno explica los largos períodos refractarios requeridos para que las células del músculo cardíaco bombean sangre de manera efectiva antes de que sean capaces de disparar por segunda vez. Estos miocitos cardíacos normalmente no inician su propio potencial eléctrico, aunque son capaces de hacerlo, sino que esperan un impulso para alcanzarlos.
Las células contráctiles demuestran una fase de reposo mucho más estable que las células conductoras a aproximadamente −80 mV para las células en las aurículas y −90 mV para las células en los ventrículos. A pesar de esta diferencia inicial, los demás componentes de sus potenciales de acción son prácticamente idénticos. En ambos casos, cuando son estimulados por un potencial de acción, los canales regulados por voltaje se abren rápidamente, iniciando el mecanismo de realimentación positiva de despolarización. Esta rápida afluencia de iones cargados positivamente eleva el potencial de membrana a aproximadamente +30 mV, momento en el que se cierran los canales de sodio. El período de despolarización rápida suele durar 3—5 ms. A la despolarización le sigue la fase de meseta, en la que el potencial de membrana disminuye relativamente lentamente. Esto se debe en gran parte a la apertura de los canales lentos de Ca 2 +, permitiendo que Ca 2 + ingrese a la celda mientras pocos canales K + están abiertos, permitiendo que K + salga de la celda. La fase de meseta relativamente larga dura aproximadamente 175 ms. Una vez que el potencial de membrana alcanza aproximadamente cero, los canales Ca 2 + se cierran y los canales K + se abren, permitiendo que K + salga de la célula. La repolarización dura aproximadamente 75 ms. En este punto, el potencial de membrana disminuye hasta alcanzar niveles de reposo una vez más y el ciclo se repite. Todo el evento dura entre 250 y 300 ms (Figura\(\PageIndex{5}\)).
El período refractario absoluto para el músculo contráctil cardíaco dura aproximadamente 200 ms, y el período refractario relativo dura aproximadamente 50 ms, para un total de 250 ms. Este periodo prolongado es crítico, ya que el músculo cardíaco debe contraerse para bombear sangre de manera efectiva y la contracción debe seguir los eventos eléctricos. Sin periodos refractarios prolongados, se producirían contracciones prematuras en el corazón y no serían compatibles con la vida.

Iones de calcio
Los iones de calcio juegan dos papeles críticos en la fisiología del músculo cardíaco. Su afluencia a través de canales lentos de calcio explica la fase de meseta prolongada y el período refractario absoluto que permiten que el músculo cardíaco funcione correctamente. Los iones de calcio también se combinan con la proteína reguladora troponina en el complejo troponina-tropomiosina; este complejo elimina la inhibición que impide que las cabezas de las moléculas de miosina formen puentes transversales con los sitios activos en la actina que proporcionan el golpe de potencia de contracción. Este mecanismo es prácticamente idéntico al del músculo esquelético. Aproximadamente el 20 por ciento del calcio requerido para la contracción es suministrado por la afluencia de Ca 2 + durante la fase de meseta. El Ca 2 + restante para la contracción se libera del almacenamiento en el retículo sarcoplásmico.
Tasas comparativas de disparo del sistema de conducción
El patrón de despolarización prepotencial o espontánea, seguido de una rápida despolarización y repolarización recién descrita, se observa en el nodo SA y algunas otras células conductoras en el corazón. Dado que el nodo SA es el marcapasos, alcanza el umbral más rápido que cualquier otro componente del sistema de conducción. Iniciará que los impulsos se propaguen a las otras células conductoras. El nódulo SA, sin control nervioso o endocrino, iniciaría un impulso cardíaco aproximadamente 80—100 veces por minuto. Si bien cada componente del sistema de conducción es capaz de generar su propio impulso, la velocidad se ralentiza progresivamente a medida que avanza desde el nodo SA hasta las fibras de Purkinje. Sin el nodo SA, el nodo AV generaría una frecuencia cardíaca de 40—60 latidos por minuto. Si se bloqueara el nódulo AV, el haz auriculoventricular se dispararía a una velocidad aproximada de 30—40 impulsos por minuto. Las ramas del haz tendrían una tasa inherente de 20—30 impulsos por minuto, y las fibras de Purkinje dispararían a 15—20 impulsos por minuto. Si bien algunos atletas aeróbicos excepcionalmente entrenados demuestran frecuencias cardíacas en reposo en el rango de 30—40 latidos por minuto (la cifra más baja registrada es de 28 latidos por minuto para Miguel Indurain, un ciclista), para la mayoría de los individuos, tasas inferiores a 50 latidos por minuto indicarían una condición llamada bradicardia. Dependiendo del individuo específico, ya que las tasas caen muy por debajo de este nivel, el corazón sería incapaz de mantener un flujo adecuado de sangre a los tejidos vitales, inicialmente resultando en una disminución de la pérdida de función a través de los sistemas, inconsciencia y finalmente la muerte.
Electrocardiograma
Mediante la colocación cuidadosa de los electrodos superficiales en el cuerpo, es posible registrar la señal eléctrica compleja y compuesta del corazón. Este trazado de la señal eléctrica es el electrocardiograma (ECG), también comúnmente abreviado EKG (K viniendo kardiología, del término alemán para cardiología). El análisis cuidadoso del ECG revela una imagen detallada de la función cardíaca normal y anormal, y es una herramienta de diagnóstico clínico indispensable. El electrocardiógrafo estándar (el instrumento que genera un ECG) utiliza 3, 5 o 12 derivaciones. Cuanto mayor sea el número de derivaciones que utiliza un electrocardiógrafo, más información proporciona el ECG. El término “plomo” puede usarse para referirse al cable desde el electrodo hasta el registrador eléctrico, pero típicamente describe la diferencia de voltaje entre dos de los electrodos. El electrocardiógrafo de 12 derivaciones utiliza 10 electrodos colocados en ubicaciones estándar en la piel del paciente (Figura\(\PageIndex{6}\)). En electrocardiógrafos ambulatorios continuos, el paciente lleva un pequeño dispositivo portátil que funciona con baterías conocido como monitor Holter, o simplemente un Holter, que monitorea continuamente la actividad eléctrica cardíaca, típicamente por un periodo de 24 horas durante la rutina normal del paciente.
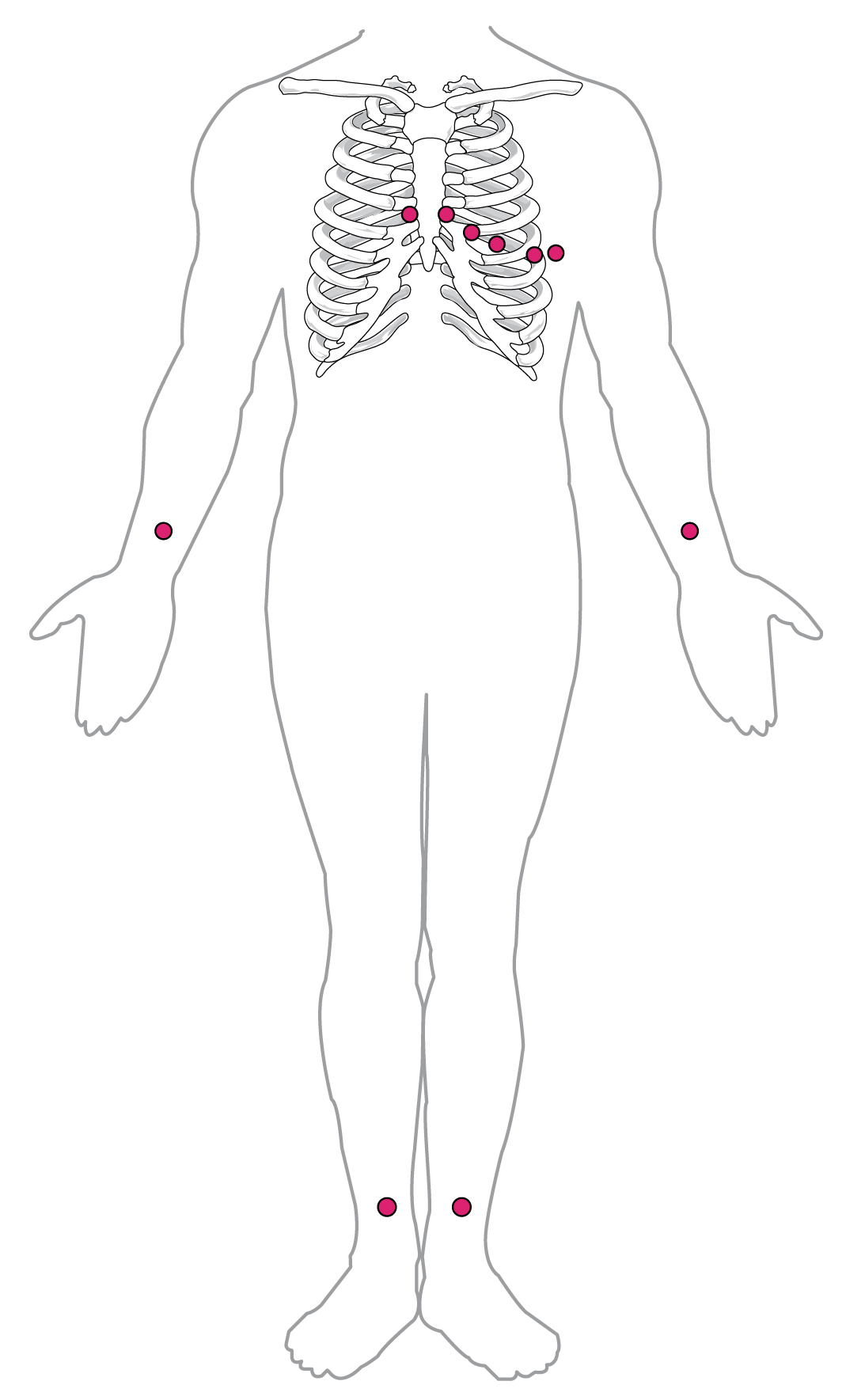
Visite este sitio para un análisis más detallado de los ECG.

Figura\(\PageIndex{8}\): Rastreo ECG Correlacionado con el Ciclo Cardíaco. Este diagrama correlaciona un rastreo de ECG con los eventos eléctricos y mecánicos de una contracción cardíaca. Cada segmento de un rastreo de ECG corresponde a un evento en el ciclo cardíaco.
Anomalías ECG
Ocasionalmente, una zona del corazón distinta del nódulo SA iniciará un impulso que será seguido por una contracción prematura. Tal área, que en realidad puede ser un componente del sistema de conducción o de algunas otras células contráctiles, se conoce como foco ectópico o marcapasos ectópico. Un foco ectópico puede ser estimulado por isquemia localizada; exposición a ciertos fármacos, incluyendo cafeína, digital o acetilcolina; estimulación elevada por divisiones simpáticas o parasimpáticas del sistema nervioso autónomo; o una serie de enfermedades o afecciones patológicas. Las incidencias ocasionales son generalmente transitorias y no amenazantes para la vida, pero si la afección se vuelve crónica, puede llevar a una arritmia, una desviación del patrón normal de conducción y contracción del impulso, o a fibrilación, un latido descoordinado del corazón.
Si bien la interpretación de un ECG es posible y extremadamente valiosa después de algún entrenamiento, una comprensión completa de las complejidades y complejidades generalmente requiere varios años de experiencia. En general, el tamaño de las variaciones eléctricas, la duración de los eventos y el análisis vectorial detallado proporcionan la imagen más completa de la función cardíaca. Por ejemplo, una onda P amplificada puede indicar agrandamiento de las aurículas, una onda Q agrandada puede indicar un MI y una onda Q suprimida o invertida agrandada a menudo indica ventrículos agrandados. Las ondas T a menudo aparecen más planas cuando se está suministrando oxígeno insuficiente al miocardio. A menudo se observa una elevación del segmento ST por encima de la línea basal en pacientes con IM agudo, y puede aparecer deprimido por debajo de la línea basal cuando ocurre hipoxia.
Tan útil como puede ser analizar estas grabaciones eléctricas, existen limitaciones. Por ejemplo, no todas las áreas que sufren un IM pueden ser obvias en el ECG. Adicionalmente, no revelará la efectividad del bombeo, lo que requiere más pruebas, como una prueba de ultrasonido llamada ecocardiograma o imágenes de medicina nuclear. También es posible que haya actividad eléctrica sin pulso, que aparecerá en un rastreo de ECG, aunque no existe una acción de bombeo correspondiente. Las anomalías comunes que pueden ser detectadas por los ECG se muestran en la Figura\(\PageIndex{9}\).
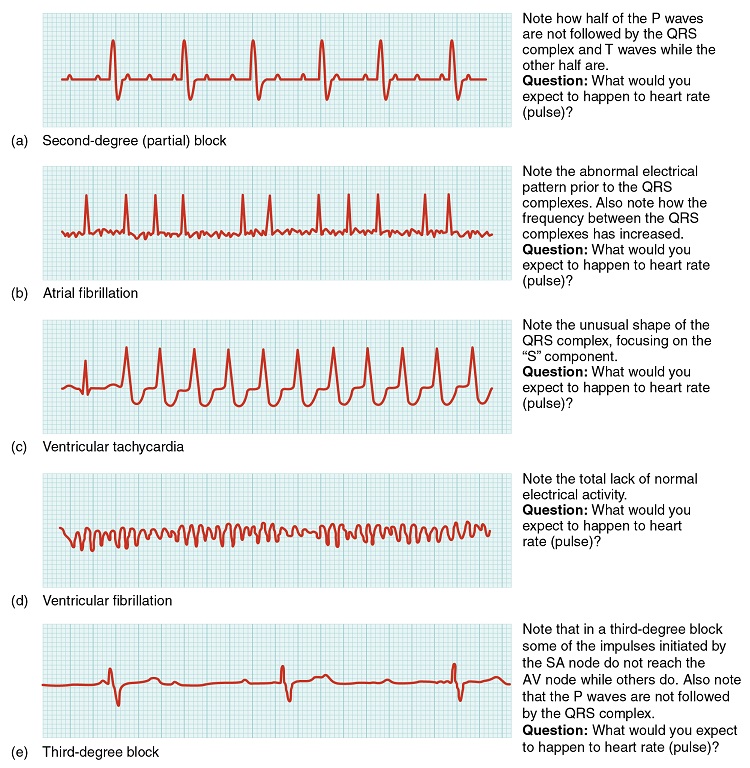
Figura\(\PageIndex{9}\): Anomalías comunes del ECG. (a) En un bloque de segundo grado o parcial, la mitad de las ondas P no son seguidas por el complejo QRS y las ondas T mientras que la otra mitad lo son. (b) En la fibrilación auricular, el patrón eléctrico es anormal previo al complejo QRS y la frecuencia entre los complejos QRS ha aumentado. (c) En la taquicardia ventricular, la forma del complejo QRS es anormal. d) En la fibrilación ventricular, no hay actividad eléctrica normal. (e) En un bloqueo de tercer grado, no existe correlación entre la actividad auricular (la onda P) y la actividad ventricular (el complejo QRS).
Visite este sitio para obtener una biblioteca más completa de ECG anormales.
Desfibriladores Automatizados Externos
En el caso de que la actividad eléctrica del corazón se vea gravemente alterada, se puede producir el cese de la actividad eléctrica o fibrilación. En la fibrilación, el corazón late de manera salvaje, incontrolada, lo que impide que pueda bombear de manera efectiva. La fibrilación auricular (ver Figura 19.2.9.b) es un padecimiento grave, pero mientras los ventrículos continúen bombeando sangre, la vida del paciente puede no estar en peligro inmediato. La fibrilación ventricular (ver Figura 19.2.9.d) es una emergencia médica que requiere soporte vital, debido a que los ventrículos no están bombeando sangre de manera efectiva. En un entorno hospitalario, a menudo se lo describe como “código azul”. Si no se trata por tan solo unos minutos, la fibrilación ventricular puede provocar la muerte cerebral. El tratamiento más común es la desfibrilación, que utiliza paletas especiales para aplicar una carga al corazón desde una fuente eléctrica externa en un intento de establecer un ritmo sinusal normal (Figura\(\PageIndex{10}\)). Un desfibrilador detiene efectivamente el corazón para que el nódulo SA pueda desencadenar un ciclo de conducción normal. Debido a su efectividad para restablecer un ritmo sinusal normal, se están colocando desfibriladores automatizados externos (EAD) en áreas frecuentadas por un gran número de personas, como escuelas, restaurantes y aeropuertos. Estos dispositivos contienen instrucciones verbales simples y directas que pueden ser seguidas por personal no médico en un intento de salvar una vida.

Un bloqueo cardíaco se refiere a una interrupción en la vía de conducción normal. La nomenclatura para estos es muy sencilla. Los bloques nodales SA ocurren dentro del nodo SA. Los bloques nodales AV ocurren dentro del nodo AV. Los bloques infra-hisianos involucran el manojo de His. Los bloqueos de rama ocurren dentro de las ramas del haz auriculoventricular izquierda o derecha. Los hemibloqueos son parciales y ocurren dentro de uno o más fascículos de la rama del haz auriculoventricular. Clínicamente, los tipos más comunes son los bloqueos nodales AV e infra-hisianos.
Los bloques AV a menudo se describen por grados. Un bloqueo de primer grado o parcial indica un retraso en la conducción entre los nodos SA y AV. Esto se puede reconocer en el ECG como un intervalo PR anormalmente largo. Un bloqueo de segundo grado o incompleto ocurre cuando algunos impulsos del nodo SA llegan al nodo AV y continúan, mientras que otros no. En esta instancia, el ECG revelaría algunas ondas P no seguidas de un complejo QRS, mientras que otras parecerían normales. En el bloqueo de tercer grado o completo, no existe correlación entre la actividad auricular (la onda P) y la actividad ventricular (el complejo QRS). Incluso en el caso de un bloqueo total de SA, el nodo AV asumirá el papel de marcapasos y continuará iniciando contracciones a 40—60 contracciones por minuto, lo que es adecuado para mantener la conciencia. Los bloqueos de segundo y tercer grado se demuestran en el ECG presentado en la Figura\(\PageIndex{9}\).
Cuando las arritmias se convierten en un problema crónico, el corazón mantiene un ritmo de unión, el cual se origina en el nodo AV. Para acelerar la frecuencia cardíaca y restaurar el ritmo sinusal completo, un cardiólogo puede implantar un marcapasos artificial, que entrega impulsos eléctricos al músculo cardíaco para asegurar que el corazón continúe contrayéndose y bombeando sangre de manera efectiva. Estos marcapasos artificiales son programables por los cardiólogos y pueden proporcionar estimulación temporalmente bajo demanda o de forma continua. Algunos dispositivos también contienen desfibriladores incorporados.
Metabolismo del músculo cardíaco
Normalmente, el metabolismo del músculo cardíaco es completamente aeróbico. El oxígeno de los pulmones se lleva al corazón, y a cualquier otro órgano, unido a las moléculas de hemoglobina dentro de los eritrocitos. Las células cardíacas también almacenan cantidades apreciables de oxígeno en la mioglobina. Normalmente, estos dos mecanismos, oxígeno circulante y oxígeno unido a la mioglobina, pueden suministrar suficiente oxígeno al corazón, incluso durante el máximo rendimiento.
Los ácidos grasos y la glucosa de la circulación se descomponen dentro de las mitocondrias para liberar energía en forma de ATP. Tanto las gotitas de ácidos grasos como el glucógeno se almacenan dentro del sarcoplasma y proporcionan un aporte adicional de nutrientes. (Busca contenido adicional para más detalles sobre el metabolismo.)
Revisión del Capítulo
El corazón está regulado tanto por el control neural como endocrino, pero es capaz de iniciar su propio potencial de acción seguido de contracción muscular. Las células conductoras dentro del corazón establecen la frecuencia cardíaca y la transmiten a través del miocardio. Las células contráctiles se contraen e impulsan la sangre. La vía normal de transmisión para las células conductoras es el nódulo sinoauricular (SA), las vías internodales, el nódulo auriculoventricular (AV), el haz auriculoventricular (AV) de His, las ramas del haz y las fibras de Purkinje. El potencial de acción para las células conductoras consiste en una fase prepotencial con una afluencia lenta de Na + seguida de una afluencia rápida de Ca 2 + y salida de K +. Las células contráctiles tienen un potencial de acción con una fase de meseta extendida que da como resultado un período refractario prolongado para permitir una contracción completa para que el corazón bombee sangre de manera efectiva. Los puntos reconocibles en el ECG incluyen la onda P que corresponde a la despolarización auricular, el complejo QRS que corresponde a la despolarización ventricular y la onda T que corresponde a la repolarización ventricular.
Preguntas de revisión
P. ¿Cuál de las siguientes características es exclusiva de las células del músculo cardíaco?
A. Solo el músculo cardíaco contiene un retículo sarcoplásmico.
B. Solo el músculo cardíaco tiene uniones gap.
C. Solo el músculo cardíaco es capaz de autorritmicidad
D. Solo el músculo cardíaco tiene una alta concentración de mitocondrias.
Respuesta: C
P. ¿La afluencia de qué ion representa la fase de meseta?
A. sodio
B. potasio
C. cloruro
D. calcio
Respuesta: D
P. ¿Qué porción del ECG corresponde a la repolarización de las aurículas?
A. onda P
B. Complejo QRS
C. Onda T
D. ninguno de los anteriores: la repolarización auricular está enmascarada por despolarización ventricular
Respuesta: D
P: ¿Qué componente del sistema de conducción cardíaca tendría la frecuencia de disparo más lenta?
A. nódulo auriculoventricular
B. haz auriculoventricular
C. ramales de haz
D. Fibras de Purkinje
Respuesta: D
Preguntas de Pensamiento Crítico
P. ¿Por qué la fase de meseta es tan crítica para la función del músculo cardíaco?
A. Evita que los impulsos adicionales se propaguen prematuramente por el corazón, permitiendo así al músculo tiempo suficiente para contraerse y bombear sangre de manera efectiva.
P. ¿Cómo contribuye el retraso del impulso en el nódulo auriculoventricular a la función cardíaca?
A. Asegura tiempo suficiente para que el músculo auricular se contraiga y bombee sangre a los ventrículos antes de que el impulso sea conducido a las cámaras inferiores.
P. ¿Cómo ayudan las uniones de brecha y los discos intercalados a la contracción del corazón?
A. Las uniones de brecha dentro de los discos intercalados permiten que los impulsos se propaguen de una célula del músculo cardíaco a otra, permitiendo que los iones de sodio, potasio y calcio fluyan entre las células adyacentes, propagando el potencial de acción y asegurando contracciones coordinadas.
P. ¿Por qué las células de los músculos cardíacos demuestran autorritmicidad?
A. Sin un verdadero potencial de reposo, hay una afluencia lenta de iones de sodio a través de canales lentos que produce un prepotencial que gradualmente alcanza el umbral.
Glosario
- marcapasos artificiales
- dispositivo médico que transmite señales eléctricas al corazón para asegurar que se contrae y bombea sangre al cuerpo
- haz auriculoventricular
- (también, haz de His) grupo de células conductiles miocárdicas especializadas que transmiten el impulso desde el nódulo AV a través del tabique interventricular; forman las ramas del haz auriculoventricular izquierdo y derecho
- ramas de haz auriculoventricular
- (también, ramas del haz izquierdo o derecho) células conductiles miocárdicas especializadas que surgen de la bifurcación del haz auriculoventricular y pasan por el tabique interventricular; conducen a las fibras de Purkinje y también al músculo papilar derecho a través de la banda moderadora
- nódulo auriculoventricular (AV)
- grupo de células miocárdicas localizadas en la porción inferior de la aurícula derecha dentro del tabique auriculoventricular; recibe el impulso del nódulo SA, hace una pausa y luego lo transmite a células conductoras especializadas dentro del tabique interventricular
- autorritmicidad
- capacidad del músculo cardíaco para iniciar su propio impulso eléctrico que desencadena la contracción mecánica que bombea sangre a un ritmo fijo sin control nervioso o endocrino
- Paquete de Bachmann
- (también, banda interauricular) grupo de células conductoras especializadas que transmiten el impulso directamente desde el nodo SA en la aurícula derecha a la aurícula izquierda
- manojo de Su
- (también, haz auriculoventricular) grupo de células conductiles miocárdicas especializadas que transmiten el impulso desde el nódulo AV a través del tabique interventricular; forman las ramas del haz auriculoventricular izquierdo y derecho
- electrocardiograma (ECG)
- registro superficial de la actividad eléctrica del corazón que puede ser utilizado para el diagnóstico de la función cardíaca irregular; también abreviado como EKG
- bloqueo de corazón
- interrupción en la vía de conducción normal
- banda interauricular
- (también, haz de Bachmann) grupo de células conductoras especializadas que transmiten el impulso directamente desde el nodo SA en la aurícula derecha a la aurícula izquierda
- disco intercalado
- unión física entre células adyacentes del músculo cardíaco; que consiste en desmosomas, proteoglicanos de enlace especializados y uniones gap que permiten el paso de iones entre las dos células
- vías internodales
- células conductiles especializadas dentro de las aurículas que transmiten el impulso desde el nodo SA a través de las células miocárdicas de la aurícula y al nodo AV
- células conductoras del miocardio
- células especializadas que transmiten impulsos eléctricos por todo el corazón y desencadenan la contracción de las células contráctiles miocárdicas
- células contráctiles miocárdicas
- mayor parte de las células del músculo cardíaco en las aurículas y ventrículos que conducen impulsos y se contraen para propulsar la sangre
- Onda P
- componente del electrocardiograma que representa la despolarización de las aurículas
- marcapasos
- grupo de células miocárdicas especializadas conocidas como el nódulo SA que inicia el ritmo sinusal
- despolarización prepotencial
- (también, despolarización espontánea) mecanismo que da cuenta de la propiedad autorrítmica del músculo cardíaco; el potencial de membrana aumenta a medida que los iones de sodio se difunden a través de los canales iónicos de sodio siempre abiertos y hace que el potencial eléctrico aumente
- Fibras de Purkinje
- fibras de conducción miocárdica especializadas que surgen de las ramas del haz y extienden el impulso a las fibras de contracción miocárdica de los ventrículos
- Complejo QRS
- componente del electrocardiograma que representa la despolarización de los ventrículos e incluye, como componente, la repolarización de las aurículas
- nódulo sinoauricular (SA)
- conocido como el marcapasos, un grupo especializado de células conductoras miocárdicas localizadas en la porción superior de la aurícula derecha que tiene la mayor tasa inherente de despolarización que luego se extiende por todo el corazón
- ritmo sinusal
- patrón contráctil normal del corazón
- despolarización espontánea
- (también, despolarización prepotencial) el mecanismo que da cuenta de la propiedad autorrítmica del músculo cardíaco; el potencial de membrana aumenta a medida que los iones de sodio se difunden a través de los canales iónicos de sodio siempre abiertos y hace que el potencial eléctrico aumente
- Onda T
- componente del electrocardiograma que representa la repolarización de los ventrículos


