6.4: Contracción muscular
- Page ID
- 120969
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Objetivos de aprendizaje
- Describir los pasos involucrados en la contracción muscular
Modelo de contracción de filamento deslizante
Para que una célula muscular se contraiga, el sarcómero debe acortarse. Sin embargo, los filamentos gruesos y delgados, los componentes de los sarcómeres, no se acortan. En cambio, se deslizan uno al otro, haciendo que el sarcómero se acorte mientras que los filamentos permanecen de la misma longitud. La teoría de la contracción muscular del filamento deslizante se desarrolló para ajustarse a las diferencias observadas en las bandas nombradas en el sarcómero en diferentes grados de contracción muscular y relajación. El mecanismo de contracción es la unión de la miosina a la actina, formando puentes transversales que generan movimiento de filamentos (Figura 6.7).
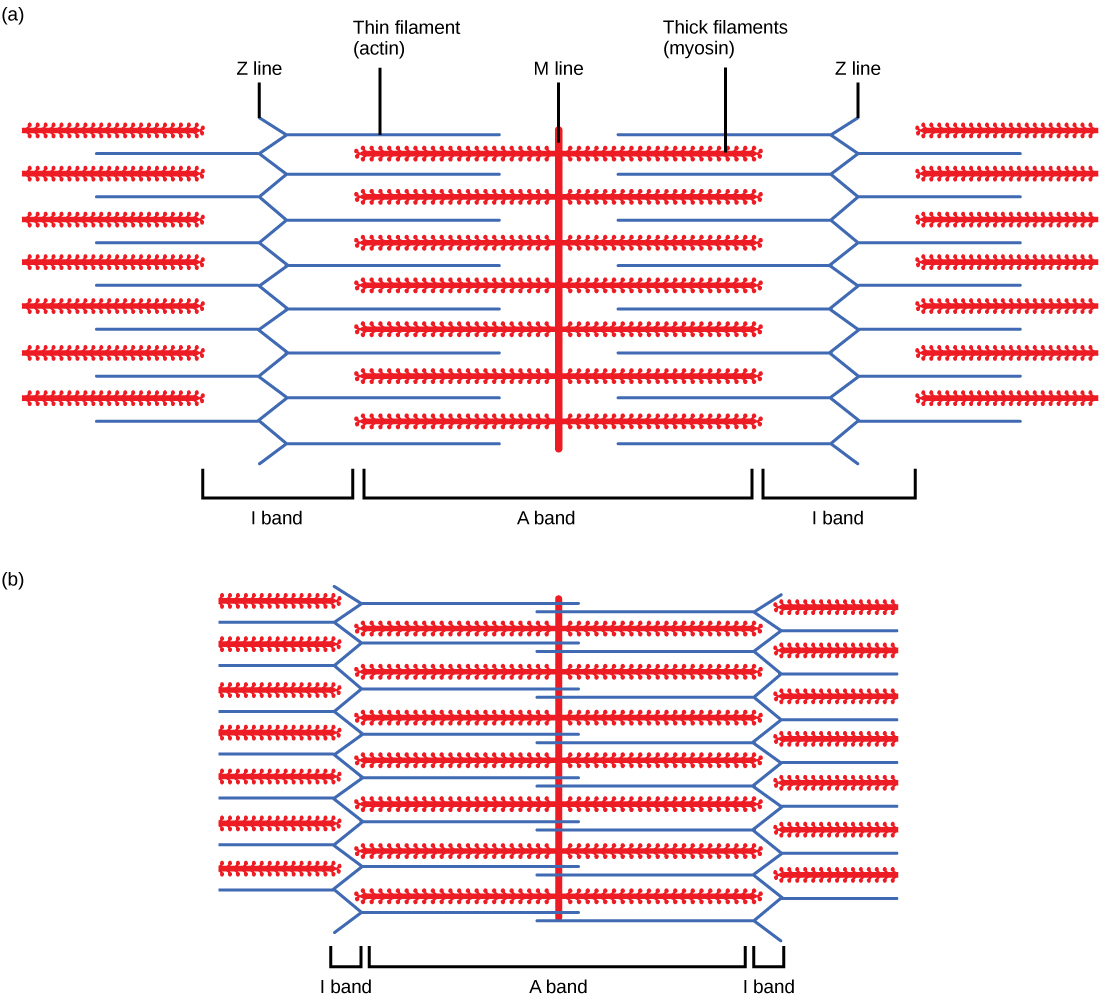
Figura 6.7. Cuando (a) un sarcómero (b) se contrae, las líneas Z se acercan y la banda I se hace más pequeña. La banda A mantiene el mismo ancho y, en plena contracción, los filamentos delgados se superponen.
Cuando un sarcómero se acorta, algunas regiones se acortan mientras que otras permanecen de la misma longitud. Un sarcómero se define como la distancia entre dos discos Z consecutivos o líneas Z; cuando un músculo se contrae, la distancia entre los discos Z se reduce. La zona H, la región central de la zona A, contiene solo filamentos gruesos y se acorta durante la contracción. La banda I contiene sólo filamentos finos y además acorta. La banda A no se acorta —sigue siendo la misma longitud— pero bandas A de diferentes sarcómeros se acercan durante la contracción, desapareciendo eventualmente. Los filamentos gruesos arrastran los filamentos delgados hacia el centro del sarcómero hasta que los discos Z se acercan a los filamentos gruesos. La zona de solapamiento, en la que los filamentos delgados y los filamentos gruesos ocupan la misma área, aumenta a medida que los filamentos delgados se mueven hacia adentro.
ATP y contracción muscular
El movimiento del acortamiento muscular ocurre cuando las cabezas de miosina se unen a la actina y tiran de la actina hacia adentro. Esta acción requiere de energía, la cual es proporcionada por el ATP. La miosina se une a la actina en un sitio de unión en la proteína actina globular. La miosina tiene otro sitio de unión para ATP en el que la actividad enzimática hidroliza ATP a ADP, liberando una molécula de fosfato inorgánico y energía.
La unión a ATP hace que la miosina libere actina, permitiendo que la actina y la miosina se separen entre sí. Después de que esto suceda, el ATP recién unido se convierte en ADP y fosfato inorgánico, Pi. La enzima en el sitio de unión de la miosina se llama ATPasa. La energía liberada durante la hidrólisis de ATP cambia el ángulo de la cabeza de la miosina a una posición “amarrada”. La cabeza de miosina se encuentra entonces en una posición para un mayor movimiento, poseyendo energía potencial, pero ADP y Pi todavía están unidos. Si los sitios de unión a actina están cubiertos y no disponibles, la miosina permanecerá en la configuración de alta energía con ATP hidrolizado pero aún unido.
Si se descubren los sitios de unión a actina, se formará un puente cruzado; es decir, la cabeza de miosina abarca la distancia entre las moléculas de actina y miosina. Luego se libera Pi, permitiendo que la miosina gaste la energía almacenada como un cambio conformacional. La cabeza de miosina se mueve hacia la línea M, tirando de la actina junto con ella. A medida que se tira de la actina, los filamentos se mueven aproximadamente 10 nm hacia la línea M. A este movimiento se le llama golpe de potencia, ya que es el paso en el que se produce la fuerza. A medida que se tira de la actina hacia la línea M, el sarcómero se acorta y el músculo se contrae.
Cuando la cabeza de miosina está “amarrada”, contiene energía y se encuentra en una configuración de alta energía. Esta energía se gasta a medida que la cabeza de miosina se mueve a través del golpe de potencia; al final de la carrera de potencia, la cabeza de miosina se encuentra en una posición de baja energía. Después de la carrera de potencia, se libera ADP; sin embargo, el puente transversal formado todavía está en su lugar, y actina y miosina se unen entre sí. El ATP puede entonces unirse a la miosina, lo que permite que el ciclo de puente cruzado comience de nuevo y se pueda producir una mayor contracción muscular (Figura 6.8).
Mira este video explicando cómo se señala una contracción muscular.
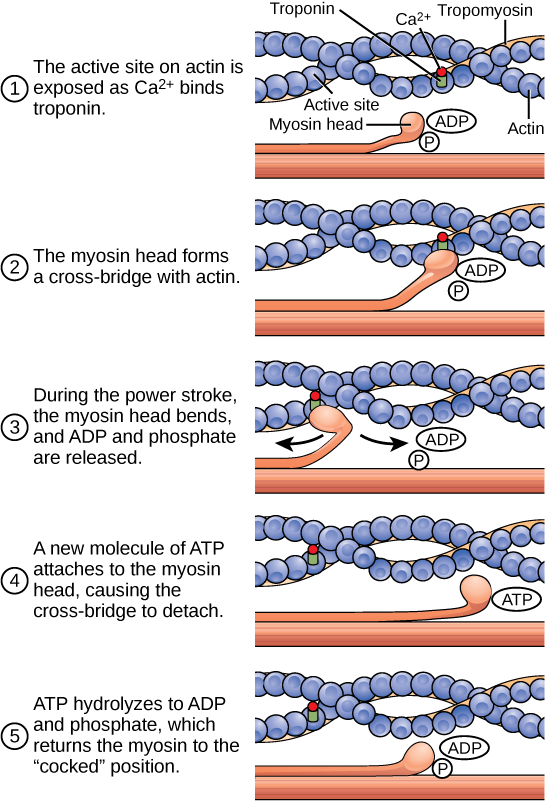
Figura 6.8. Se muestra el ciclo de contracción muscular en puente cruzado, que se desencadena por la unión de Ca2+ al sitio activo de la actina. Con cada ciclo de contracción, la actina se mueve en relación con la miosina.
Ejercicio\(\PageIndex{1}\)
¿Cuál de las siguientes afirmaciones sobre la contracción muscular es cierta?
- La carrera de potencia ocurre cuando el ATP se hidroliza a ADP y fosfato.
- El golpe de potencia ocurre cuando ADP y fosfato se disocian de la cabeza de miosina.
- La carrera de potencia ocurre cuando ADP y fosfato se disocian del sitio activo de actina.
- El golpe de poder ocurre cuando el Ca2+ se une a la cabeza de calcio.
Mira este video de animación de la contracción muscular en puente cruzado.
Proteínas reguladoras
Cuando un músculo está en estado de reposo, la actina y la miosina se separan. Para evitar que la actina se una al sitio activo de la miosina, las proteínas reguladoras bloquean los sitios de unión molecular. La tropomiosina bloquea los sitios de unión de miosina en las moléculas de actina, evitando la formación de puentes cruzados y evitando la contracción en un músculo sin entrada nerviosa. La troponina se une a la tropomiosina y ayuda a posicionarla sobre la molécula de actina; también se une a los iones de calcio.
Para permitir una contracción muscular, la tropomiosina debe cambiar la conformación, descubriendo el sitio de unión a la miosina en una molécula de actina y permitiendo la formación de puentes cruzados. Esto sólo puede ocurrir en presencia de calcio, que se mantiene en concentraciones extremadamente bajas en el sarcoplasma. Si están presentes, los iones de calcio se unen a la troponina, provocando cambios conformacionales en la troponina que permiten que la tropomiosina se aleje de los sitios de unión a la miosina en la actina. Una vez que se elimina la tropomiosina, se puede formar un puente transversal entre la actina y la miosina, desencadenando la contracción. El ciclo de puente cruzado continúa hasta que los iones Ca2+ y ATP ya no están disponibles y la tropomiosina vuelve a cubrir los sitios de unión en la actina.
Acoplamiento excitación-contracción
El acoplamiento excitación-contracción es el vínculo (transducción) entre el potencial de acción generado en el sarcolema y el inicio de una contracción muscular. El desencadenante de la liberación de calcio desde el retículo sarcoplásmico hacia el sarcoplasma es una señal neural. Cada fibra del músculo esquelético es controlada por una neurona motora, que conduce señales desde el cerebro o la médula espinal hasta el músculo. El área del sarcolema en la fibra muscular que interactúa con la neurona se llama placa terminal motora. El extremo del axón de la neurona se llama terminal sináptica, y en realidad no entra en contacto con la placa terminal motora. Un pequeño espacio llamado hendidura sináptica separa el terminal sináptico de la placa terminal del motor. Las señales eléctricas viajan a lo largo del axón de la neurona, que se ramifica a través del músculo y se conecta a fibras musculares individuales en una unión neuromuscular.
La capacidad de las células para comunicarse eléctricamente requiere que las células gasten energía para crear un gradiente eléctrico a través de sus membranas celulares. Este gradiente de carga es transportado por iones, los cuales se distribuyen diferencialmente a través de la membrana. Cada ion ejerce una influencia eléctrica y una influencia de concentración. Así como la leche eventualmente se mezclará con el café sin necesidad de revolver, los iones también se distribuyen uniformemente, si se les permite hacerlo. En este caso, no se les permite regresar a un estado uniformemente mixto.
La ATPasa sodio-potasio utiliza energía celular para mover los iones K+ dentro de la célula y los iones Na+ afuera. Esto por sí solo acumula una pequeña carga eléctrica, pero un gran gradiente de concentración. Hay mucho K+ en la celda y mucho Na+ fuera de la celda. El potasio es capaz de salir de la célula a través de canales de K+ que están abiertos el 90% del tiempo, y lo hace. Sin embargo, los canales de Na+ rara vez están abiertos, por lo que Na+ permanece fuera de la celda. Cuando K+ sale de la célula, obedeciendo su gradiente de concentración, eso efectivamente deja atrás una carga negativa. Entonces, en reposo, hay un gran gradiente de concentración para que Na+ ingrese a la célula, y hay una acumulación de cargas negativas dejadas atrás en la celda. Este es el potencial de membrana en reposo. El potencial en este contexto significa una separación de carga eléctrica que es capaz de hacer trabajo. Se mide en voltios, al igual que una batería. Sin embargo, el potencial transmembrana es considerablemente menor (0.07 V); por lo tanto, el valor pequeño se expresa como milivoltios (mV) o 70 mV. Debido a que el interior de una celda es negativo comparado con el exterior, un signo menos significa el exceso de cargas negativas dentro de la celda, −70 mV.
Si un evento cambia la permeabilidad de la membrana a iones Na+, ingresarán a la célula. Eso va a cambiar el voltaje. Se trata de un evento eléctrico, llamado potencial de acción, que puede ser utilizado como señal celular. La comunicación ocurre entre nervios y músculos a través de neurotransmisores. Los potenciales de acción neuronal causan la liberación de neurotransmisores desde el terminal sináptico hacia la hendidura sináptica, donde luego pueden difundirse a través de la hendidura sináptica y unirse a una molécula receptora en la placa terminal motora. La placa terminal motora posee pliegues de unión, pliegues en el sarcolema que crean una gran área de superficie para que el neurotransmisor se una a los receptores. Los receptores son en realidad canales de sodio que se abren para permitir el paso de Na+ a la célula cuando reciben la señal del neurotransmisor.
La acetilcolina (ACh) es un neurotransmisor liberado por las neuronas motoras que se une a los receptores en la placa terminal motora. La liberación de neurotransmisores ocurre cuando un potencial de acción viaja por el axón de la neurona motora, lo que resulta en una permeabilidad alterada de la membrana terminal sináptica y una afluencia de calcio. Los iones Ca2+ permiten que las vesículas sinápticas se muevan y se unan a la membrana presináptica (en la neurona) y liberen neurotransmisores de las vesículas hacia la hendidura sináptica. Una vez liberado por el terminal sináptico, ACh se difunde a través de la hendidura sináptica hasta la placa terminal motora, donde se une con los receptores ACh. A medida que un neurotransmisor se une, estos canales iónicos se abren y los iones Na+ cruzan la membrana hacia la célula muscular. Esto reduce la diferencia de voltaje entre el interior y el exterior de la celda, lo que se denomina despolarización. Como ACh se une en la placa de extremo del motor, esta despolarización se denomina potencial de placa final. La despolarización luego se extiende a lo largo del sarcolema, creando un potencial de acción ya que los canales de sodio adyacentes al sitio de despolarización inicial detectan el cambio de voltaje y se abren. El potencial de acción se mueve a través de toda la célula, creando una onda de despolarización.
La ACh es descompuesta por la enzima acetilcolinesterasa (AChE) en acetilo y colina. La AChE reside en la hendidura sináptica, descomponiendo la ACh para que no quede unida a los receptores de ACh, lo que provocaría una contracción muscular extendida no deseada (Figura 6.9).

Figura 6.9. Este diagrama muestra el acoplamiento excitación-contracción en una contracción del músculo esquelético. El retículo sarcoplásmico es un retículo endoplásmico especializado que se encuentra en las células musculares.
Ejercicio\(\PageIndex{1}\)
El gas nervioso mortal Sarin inhibe irreversiblemente la acetilcolinesterasa. ¿Qué efecto tendría el Sarin en la contracción muscular?
Después de la despolarización, la membrana vuelve a su estado de reposo. Esto se llama repolarización, durante la cual se cierran los canales de sodio regulados por voltaje. Los canales de potasio continúan a 90% de conductancia. Debido a que la ATPasa sodio-potasio de la membrana plasmática siempre transporta iones, se restablece el estado de reposo (cargado negativamente en el interior con respecto al exterior). El periodo inmediatamente posterior a la transmisión de un impulso en un nervio o músculo, en el que una neurona o célula muscular recupera su capacidad de transmitir otro impulso, se denomina periodo refractario. Durante el periodo refractario, la membrana no puede generar otro potencial de acción. El periodo refractario permite que los canales iónicos sensibles al voltaje vuelvan a sus configuraciones de reposo. La ATPasa de sodio-potasio mueve continuamente Na+ de nuevo fuera de la celda y K+ de vuelta a la celda, y el K+ se filtra dejando atrás la carga negativa. Muy rápidamente, la membrana se repolariza, para que pueda volver a ser despolarizada.
Control de la tensión muscular
El control neural inicia la formación de puentes cruzados actina-miosina, lo que lleva al acortamiento del sarcómero involucrado en la contracción muscular. Estas contracciones se extienden desde la fibra muscular a través del tejido conectivo para tirar de los huesos, provocando el movimiento esquelético. El tirón ejercido por un músculo se llama tensión, y la cantidad de fuerza creada por esta tensión puede variar. Esto permite que los mismos músculos muevan objetos muy ligeros y objetos muy pesados. En las fibras musculares individuales, la cantidad de tensión producida depende del área transversal de la fibra muscular y de la frecuencia de estimulación neural.
El número de puentes transversales formados entre la actina y la miosina determina la cantidad de tensión que puede producir una fibra muscular. Solo se pueden formar puentes cruzados donde los filamentos gruesos y delgados se superponen, permitiendo que la miosina se una a la actina. Si se forman más puentes transversales, más miosina tirará de actina, y se producirá más tensión.
La longitud ideal de un sarcómero durante la producción de tensión máxima ocurre cuando los filamentos gruesos y delgados se superponen en el mayor grado. Si un sarcómero en reposo se estira más allá de una longitud ideal de reposo, los filamentos gruesos y delgados no se superponen en el mayor grado, y se pueden formar menos puentes transversales. Esto da como resultado menos cabezas de miosina que tiran de actina, y se produce menos tensión. A medida que se acorta un sarcómero, la zona de solapamiento se reduce a medida que los filamentos delgados alcanzan la zona H, que está compuesta por colas de miosina. Debido a que son las cabezas de miosina las que forman puentes transversales, la actina no se unirá a la miosina en esta zona, reduciendo la tensión producida por esta miofibra. Si el sarcómero se acorta, aún más, los filamentos delgados comienzan a solaparse entre sí, reduciendo aún más la formación de puentes transversales y produciendo aún menos tensión. Por el contrario, si el sarcómero se estira hasta el punto en el que los filamentos gruesos y delgados no se superponen en absoluto, no se forman puentes transversales y no se produce tensión. Esta cantidad de estiramiento no suele ocurrir porque las proteínas accesorias, los nervios sensoriales internos y el tejido conectivo se oponen al estiramiento extremo.
La variable primaria que determina la producción de fuerza es el número de miofibras dentro del músculo que reciben un potencial de acción de la neurona que controla esa fibra. Al usar los bíceps para coger un lápiz, la corteza motora del cerebro solo señala unas pocas neuronas del bíceps, y solo unas pocas miofibras responden. En vertebrados, cada miofibra responde plenamente si se estimula. Al levantar un piano, la corteza motora señala a todas las neuronas del bíceps y cada miofibra participa. Esto está cerca de la fuerza máxima que puede producir el músculo. Como se mencionó anteriormente, aumentar la frecuencia de los potenciales de acción (el número de señales por segundo) puede aumentar un poco más la fuerza, debido a que la tropomiosina está inundada de calcio.
Ejercicio\(\PageIndex{1}\)
Enséñele a su compañero sobre los eventos durante la contracción muscular, desde la llegada de la señal neural hasta la generación de movimiento impulsado por el músculo. Cuando termines, pregúntale a tu compañero qué términos o pasos te perdiste o no te explicaste bien. Deja que tu compañero llene los vacíos. Si no hubo brechas, tu compañero puede desafiarte con algunas preguntas sobre tu explicación. Recuerda que una forma en la que puedes probar si estás aprendiendo es poder transmitir tus conocimientos a otra persona.

