15.5A: Riñones Humanos
- Page ID
- 56982
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Los riñones humanos son dos órganos en forma de frijol, uno a cada lado de la columna vertebral. Representan alrededor de 0.5% del peso total del cuerpo, pero reciben 20-25% de la sangre arterial total bombeada por el corazón. Cada uno contiene de uno a dos millones de nefronas.

La nefrona

El nefrón es un tubo cerrado en un extremo y abierto en el otro. Consta de:
- Cápsula de Bowman. Ubicada en el extremo cerrado, la pared de la nefrona es empujada formando una cámara de doble pared.
- Glomérulo. Una red capilar dentro de la cápsula de Bowman. La sangre que sale del glomérulo pasa a una segunda red capilar que rodea el túbulo proximal.
- Túbulo contorneado proximal. Enroscada y forrada con células alfombradas con microvellosidades y rellenas de mitocondrias.
- Bucle de Henle. Hace un giro en horquilla y regresa al túbulo enrevesado distal.
- Túbulo contorneado distal, que también está muy enrollado y rodeado de capilares.
- Conducto colector. Conduce a un cáliz, una de las muchas cámaras pequeñas de las que drena la orina hacia la pelvis del riñón desde donde fluye a través de un uréter hasta la vejiga y, periódicamente, hacia el mundo exterior.
Las cápsulas de Bowman se empaquetan en la corteza del riñón, los túbulos y los conductos colectores descienden a la médula.
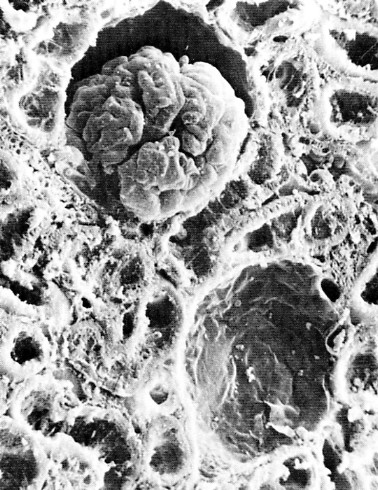
La imagen de arriba muestra una sección cortada de la corteza de un riñón de ratón como se ve bajo el microscopio electrónico de barrido. Cerca de la parte superior (centro) se puede observar una cápsula de Bowman con su glomérulo. Directamente debajo se encuentra otra cápsula de Bowman con su glomérulo eliminado. El resto del campo muestra los lúmenes de los túbulos proximales y distales ya que han sido cortados en varios ángulos.
Formación de Orina
La nefrona produce orina filtrando la sangre de sus pequeñas moléculas e iones y luego recuperando las cantidades necesarias de materiales útiles. Las moléculas excedentes o residuales y los iones se dejan fluir como orina. En 24 horas los riñones reclaman: ~1,300 g de NaCl, ~400 g NaHCO 3, ~180 g de glucosa y casi todos los 180 litros de agua que ingresaron a los túbulos. La sangre ingresa al glomérulo bajo presión. Esto hace que el agua, las moléculas pequeñas (pero no macromoléculas como las proteínas) y los iones se filtren a través de las paredes capilares hacia la cápsula de Bowman. Este fluido se llama filtrado nefrico. Como muestra la tabla, es simplemente plasma sanguíneo menos casi todas las proteínas plasmáticas. Esencialmente no es diferente del líquido intersticial.
| Componente | Plasma | filtrado nefríco | Orina | Concentración | % Reclaimado |
|---|---|---|---|---|---|
| Urea | 0.03 | 0.03 | 1.8 | 60X | 50% |
| Ácido úrico | 0.004 | 0.004 | 0.05 | 12X | 91% |
| Glucosa | 0.10 | 0.10 | Ninguno | - | 100% |
| Aminoácidos | 0.05 | 0.05 | Ninguno | - | 100% |
| Sales inorgánicas totales | 0.9 | 0.9 | <0.9—3.6 | <1—4X | 99.5% |
| Proteínas y otras macromoléculas | 8.0 | Ninguno | Ninguno | - | - |
Figura 15.5.1.4 Proceso de formación de orina
- El filtrado nefríco se acumula dentro de la cápsula de Bowman y luego fluye hacia el túbulo proximal.
- Aquí toda la glucosa y aminoácidos, > 90% del ácido úrico, y ~ 60% de las sales inorgánicas son reabsorbidas por transporte activo.
- El transporte activo de Na + fuera del túbulo proximal está controlado por angiotensina II.
- El transporte activo de fosfato (PO 4 3-) de regreso a la sangre está regulado (suprimido) tanto por la hormona paratiroidea como por el factor de crecimiento de fibroblastos 23 (FGF-23).
- A medida que estos solutos se eliminan del filtrado nefrico, un gran volumen del agua los sigue por ósmosis (80-85% de los 180 litros depositados en las cápsulas de Bowman en 24 horas).
- A medida que el fluido fluye hacia el segmento descendente del bucle de Henle, el agua continúa saliendo por ósmosis debido a que el líquido intersticial es muy hipertónico. Esto es causado por el transporte activo de Na + fuera del fluido tubular a medida que se mueve hacia arriba por el segmento ascendente del bucle de Henle.
- En los túbulos distales, se recupera más sodio por transporte activo, y aún más agua sigue por ósmosis.
- El ajuste final del contenido de sodio y agua del cuerpo ocurre en los conductos colectores.
Sodio
A pesar de que ya se ha eliminado 97% del sodio, es el último 3% que determina el balance final del sodio y de ahí el contenido de agua y la presión arterial en el organismo. La reabsorción de sodio en el túbulo distal y los conductos colectores está estrechamente regulada por la acción sinérgica de las hormonas vasopresina y aldosterona.
Agua
- El líquido intersticial hipertónico que rodea los conductos colectores proporciona una alta presión osmótica para la eliminación del agua.
- Los canales transmembrana hechos de proteínas llamadas acuaporinas se insertan en la membrana plasmática aumentando en gran medida su permeabilidad al agua. Cuando está abierto, un canal de acuaporina permite que 3 mil millones de moléculas de agua pasen por cada segundo.
- La inserción de los canales de acuaporina-2 requiere señalización por vasopresina (también conocida como arginina vasopresina [AVP] o la hormona antidiurética [ADH]).
- La vasopresina se une a receptores (llamados receptores V2) en la superficie basolateral de las células de los conductos colectores.
- La unión de la hormona desencadena un nivel creciente de AMPc dentro de la célula.
- Este “segundo mensajero” inicia una cadena de eventos que culminan con la inserción de canales de acuaporina-2 en la superficie apical de la célula.
- La liberación de vasopresina (desde el lóbulo posterior de la glándula pituitaria) está regulada por la presión osmótica de la sangre.
- Cualquier cosa que deshidrata el cuerpo, como transpirar fuertemente,
- aumenta la presión osmótica de la sangre
- activa la vasopresina → receptores V2 → vía acuaporina-2.
- Tan poco como 0.5 litros/día de orina pueden quedar de los 180 litros/día originales de filtrado nefrico.
- La concentración de sales en la orina puede ser hasta cuatro veces mayor que la de la sangre. (Pero no lo suficientemente alto como para permitir que los humanos se beneficien de beber agua de mar, que aún es más salada).
- Si la sangre se diluyera demasiado (como ocurriría después de beber una gran cantidad de agua),
- Se inhibe la secreción de vasopresina.
- Los canales de acuaporina-2 son llevados de vuelta a la célula por endocitosis.
- El resultado: se forma un gran volumen de orina acuosa (con una concentración de sal tan pequeña como una cuarta parte de la de la sangre).
Diabetes insípida
Este trastorno se caracteriza por la excreción de grandes cantidades de una orina acuosa (tanto como 30 litros - alrededor de 8 galones cada día y sed incesante.
Puede tener varias causas:
- Secreción insuficiente de vasopresina.
- Herencia de dos genes mutantes para el receptor de vasopresina (V2) [en hembras; debido a que el gen está ligado al X, solo uno lo hace para los machos].
- Herencia de uno (para mutaciones dominantes) o dos (para versiones recesivas) genes mutantes para acuaporina-2.
Síndrome de Liddle
El efecto más obvio de este raro trastorno hereditario es la presión arterial extremadamente alta (hipertensión). Es causada por un solo alelo mutante (por lo tanto, el síndrome se hereda como rasgo dominante) que codifica el canal de sodio activado por aldosterona en los conductos colectores. El canal defectuoso siempre está “encendido” así que se reabsorbe demasiado Na + y se excreta muy poco. La presión osmótica elevada resultante de la sangre produce hipertensión arterial.
Secreción Tubular
Aunque la formación de orina ocurre principalmente por el mecanismo de filtración-reabsorción descrito anteriormente, también está involucrado un mecanismo auxiliar, llamado secreción tubular. Las células de los túbulos eliminan ciertas moléculas e iones de la sangre y los depositan en el fluido dentro de los túbulos.
Ejemplo: Los iones de hidrógeno en exceso (H +) se combinan con amoníaco (NH 3) para formar iones amonio (NH 4 +) y se transportan a las celdas de los conductos colectores. Aquí el NH 4 + se disocia de nuevo en amoníaco y H +. Ambos son entonces secretados en el fluido dentro de los conductos colectores (los protones por transporte activo).
La secreción tubular de H + es importante para mantener el control del pH de la sangre. Cuando el pH de la sangre comienza a bajar, se secretan más iones de hidrógeno. Si la sangre se vuelve demasiado alcalina, se reduce la secreción de H +. Al mantener el pH de la sangre dentro de sus límites normales de 7.3—7.4, el riñón puede producir una orina con un pH tan bajo como 4.5 o tan alto como 8.5. El exceso de iones de potasio (K +) también se eliminan por secreción tubular.
El riñón y la homeostasis
Si bien pensamos en el riñón como un órgano de excreción, es más que eso. Elimina los desechos, pero también elimina los componentes normales de la sangre que están presentes en concentraciones mayores de lo normal. Cuando hay exceso de agua, iones de sodio, iones de calcio, iones de potasio, etc., el exceso se desmaya rápidamente en la orina. Por otro lado, los riñones incrementan su recuperación de estas mismas sustancias cuando están presentes en la sangre en cantidades inferiores a lo normal. Así, el riñón regula continuamente la composición química de la sangre dentro de límites estrechos. El riñón es uno de los principales dispositivos homeostáticos del cuerpo.
Hormonas de los Riñones
El riñón humano es también una glándula endocrina que secreta dos hormonas:
- Eritropoyetina (EPO)
- Calcitriol (1,25 [OH] 2 Vitamina D 3), la forma activa de la vitamina D
así como la enzima renina.
El riñón artificial
El riñón artificial utiliza el principio de diálisis para purificar la sangre de pacientes cuyos propios riñones han fallado.
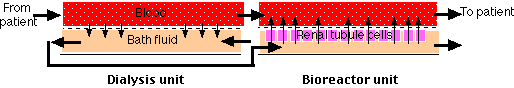
La porción izquierda de la figura (“Unidad de diálisis”) muestra el mecanismo utilizado hoy en día en los riñones artificiales. Las moléculas pequeñas como la urea se eliminan de la sangre porque son libres de difundirse entre la sangre y el líquido del baño, mientras que las moléculas grandes (por ejemplo, proteínas plasmáticas) y las células permanecen confinadas a la sangre. Al líquido del baño ya se le deben haber agregado sales esenciales para evitar la peligrosa pérdida de estos iones de la sangre. Observe que la sangre y el líquido del baño fluyen en direcciones opuestas a través de la membrana de diálisis Este intercambio de “contracorriente” mantiene un gradiente de difusión a lo largo de toda la longitud del sistema. Se agrega un anticoagulante a la sangre para que no se coagule mientras pasa por la máquina. El anticoagulante se neutraliza a medida que se devuelve la sangre al paciente.
Los riñones artificiales han demostrado ser de gran beneficio para ayudar a pacientes de mal funcionamiento renal agudo a sobrevivir a la crisis hasta que sus propios riñones reanuden la operación. También han permitido que las personas que sufren de insuficiencia renal crónica permanezcan con vida, aunque a un gasto enorme de tiempo (a menudo tres sesiones de 6 o más horas a la semana), dinero y bienestar psicológico. Además, aunque la diálisis hace un buen trabajo en la eliminación de desechos, no puede realizar las otras funciones del riñón:
- proporcionando un control homeostático preciso sobre la concentración de ingredientes vitales como glucosa y Na +
- secretar sus hormonas
¿Un riñón artificial del futuro?
En un intento de resolver estos problemas, un equipo de investigación de la Universidad de Michigan está experimentando con la adición de una “unidad biorreactor” (arriba) a la unidad de diálisis. El biorreactor consta de muchos tubos huecos porosos en cuya pared interna se une una monocapa de células de túbulos proximales (derivadas de cerdos). El fluido del baño de diálisis pasa a través del lumen de los tubos donde las moléculas y los iones pueden ser captados por la superficie apical de las células. La descarga de moléculas esenciales e iones (así como hormonas) en la superficie basolateral de las células coloca estos materiales de nuevo en la sangre (tal como lo hacen normalmente las células del túbulo proximal en la nefrona). Hasta el momento, todas las pruebas se han hecho usando perros, pero los resultados parecen prometedores.
Trasplantes de Riñón

La alternativa ideal a la diálisis a largo plazo es el trasplante de un nuevo riñón. La operación es técnicamente bastante fácil. Los riñones enfermos del receptor generalmente se dejan en su lugar, pero las arterias y venas renales están atadas a excepción de las ramas que abastecen a las glándulas suprarrenales. El principal problema es la escasez de donantes adecuadamente emparejados para moléculas de histocompatibilidad para evitar el problema del rechazo del injerto por parte del sistema inmune del receptor -que a menos que el donante y el receptor sean gemelos idénticos- “ve” al riñón como “extraño”.


