7.4: Fosforilación Oxidativa
- Page ID
- 59410
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Habilidades para Desarrollar
- Describir cómo los electrones se mueven a través de la cadena de transporte de electrones y qué sucede con sus niveles de energía
- Explicar cómo un gradiente de protones (H +) es establecido y mantenido por la cadena de transporte de electrones
Acabas de leer sobre dos vías en el catabolismo de la glucosa, la glucólisis y el ciclo del ácido cítrico, que generan ATP. La mayor parte del ATP generado durante el catabolismo aeróbico de la glucosa, sin embargo, no se genera directamente a partir de estas vías. Más bien, se deriva de un proceso que comienza con el movimiento de electrones a través de una serie de transportadores de electrones que experimentan reacciones redox. Esto hace que los iones de hidrógeno se acumulen dentro del espacio de la matriz. Por lo tanto, se forma un gradiente de concentración en el que los iones de hidrógeno se difunden fuera del espacio matriz al pasar a través de ATP sintasa La corriente de iones hidrógeno potencia la acción catalítica de la ATP sintasa, la cual fosforila ADP, produciendo ATP.
Cadena de transporte de electrones
La cadena de transporte de electrones (Figura\(\PageIndex{1}\)) es el último componente de la respiración aeróbica y es la única parte del metabolismo de la glucosa que utiliza oxígeno atmosférico. El oxígeno se difunde continuamente en las plantas; en los animales, ingresa al cuerpo a través del sistema respiratorio. El transporte de electrones es una serie de reacciones redox que se asemejan a una carrera de relevos o brigada de baldes en que los electrones pasan rápidamente de un componente al siguiente, al punto final de la cadena donde los electrones reducen el oxígeno molecular, produciendo agua. Hay cuatro complejos compuestos por proteínas, etiquetados del I al IV en la Figura\(\PageIndex{1}\), y la agregación de estos cuatro complejos, junto con los portadores de electrones móviles asociados, se llama la cadena de transporte de electrones. La cadena de transporte de electrones está presente en múltiples copias en la membrana mitocondrial interna de eucariotas y la membrana plasmática de procariotas.
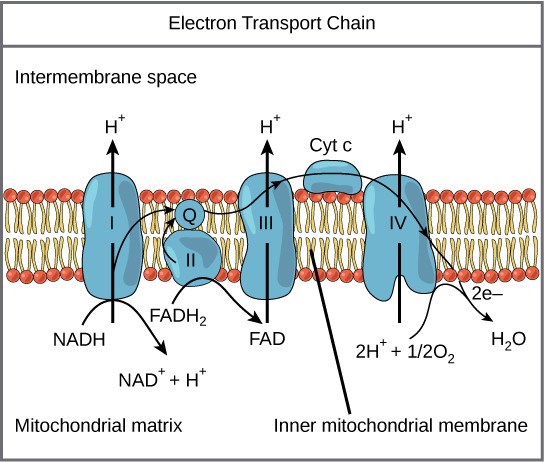
Complejo I
Para comenzar, dos electrones son transportados al primer complejo a bordo del NADH. Este complejo, marcado con I, está compuesto por mononucleótido de flavina (FMN) y una proteína que contiene hierro-azufre (Fe-S). La FMN, que se deriva de la vitamina B 2, también llamada riboflavina, es uno de varios grupos protésicos o cofactores en la cadena de transporte de electrones. Un grupo protésico es una molécula no proteica requerida para la actividad de una proteína. Los grupos protésicos son moléculas orgánicas o inorgánicas, no peptídicas unidas a una proteína que facilita su función; los grupos protésicos incluyen coenzimas, que son los grupos protésicos de enzimas. La enzima en el complejo I es NADH deshidrogenasa y es una proteína muy grande, que contiene 45 cadenas de aminoácidos. El complejo I puede bombear cuatro iones de hidrógeno a través de la membrana desde la matriz hacia el espacio intermembrana, y es de esta manera que el gradiente de iones de hidrógeno se establece y mantiene entre los dos compartimentos separados por la membrana mitocondrial interna.
Q y Complejo II
El complejo II recibe directamente FADH 2, que no pasa a través del complejo I. El compuesto que conecta el primer y segundo complejos con el tercero es ubiquinona (Q). La molécula Q es soluble en lípidos y se mueve libremente a través del núcleo hidrófobo de la membrana. Una vez que se reduce, (QH 2), la ubiquinona entrega sus electrones al siguiente complejo en la cadena de transporte de electrones. Q recibe los electrones derivados del NADH del complejo I y los electrones derivados del FADH 2 del complejo II, incluyendo la succinato deshidrogenasa. Esta enzima y FADH 2 forman un pequeño complejo que entrega electrones directamente a la cadena de transporte de electrones, evitando el primer complejo. Dado que estos electrones se desvían y por lo tanto no energizan la bomba de protones en el primer complejo, se hacen menos moléculas de ATP a partir de los electrones FADH 2. El número de moléculas de ATP finalmente obtenidas es directamente proporcional al número de protones bombeados a través de la membrana mitocondrial interna.
Complejo III
El tercer complejo está compuesto por citocromo b, otra proteína Fe-S, centro Rieske (centro 2Fe-2S) y proteínas citocromo c; este complejo también se llama citocromo oxidorreductasa. Las proteínas del citocromo tienen un grupo protésico de hemo. La molécula hemo es similar al hemo en la hemoglobina, pero transporta electrones, no oxígeno. Como resultado, el ion hierro en su núcleo se reduce y oxida a medida que pasa los electrones, fluctuando entre diferentes estados de oxidación: Fe ++ (reducido) y Fe +++ (oxidado). Las moléculas hemo en los citocromos tienen características ligeramente diferentes debido a los efectos de las diferentes proteínas que las unen, dando características ligeramente diferentes a cada complejo. El complejo III bombea protones a través de la membrana y pasa sus electrones al citocromo c para transportarlos al cuarto complejo de proteínas y enzimas (el citocromo c es el aceptor de electrones de Q; sin embargo, mientras que Q lleva pares de electrones, el citocromo c puede aceptar solo uno a la vez).
Complejo IV
El cuarto complejo está compuesto por las proteínas del citocromo c, a y a 3. Este complejo contiene dos grupos hemo (uno en cada uno de los dos citocromos, a y a 3) y tres iones de cobre (un par de Cu A y un Cu B en el citocromo a 3). Los citocromos mantienen una molécula de oxígeno muy apretada entre los iones hierro y cobre hasta que el oxígeno se reduce por completo. El oxígeno reducido luego recoge dos iones hidrógeno del medio circundante para hacer agua (H 2 O). La eliminación de los iones hidrógeno del sistema contribuye al gradiente iónico utilizado en el proceso de quimioósmosis.
Quimósmosis
En la quimiósmosis, la energía libre de la serie de reacciones redox que se acaban de describir se utiliza para bombear iones de hidrógeno (protones) a través de la membrana. La distribución desigual de iones H + a través de la membrana establece gradientes tanto de concentración como eléctricos (por lo tanto, un gradiente electroquímico), debido a la carga positiva de los iones de hidrógeno y su agregación en un lado de la membrana.
Si la membrana estuviera abierta a la difusión por los iones hidrógeno, los iones tenderían a difundirse de nuevo a través de la matriz, impulsados por su gradiente electroquímico. Recordemos que muchos iones no pueden difundirse a través de las regiones no polares de las membranas de fosfolípidos sin la ayuda de canales iónicos. De manera similar, los iones hidrógeno en el espacio de la matriz solo pueden pasar a través de la membrana mitocondrial interna a través de una proteína de membrana integral llamada ATP sintasa (Figura\(\PageIndex{2}\)). Esta compleja proteína actúa como un pequeño generador, girado por la fuerza de los iones de hidrógeno que se difunden a través de ella, bajando por su gradiente electroquímico. El giro de partes de esta máquina molecular facilita la adición de un fosfato al ADP, formando ATP, utilizando la energía potencial del gradiente de iones hidrógeno.
Conexión de arte
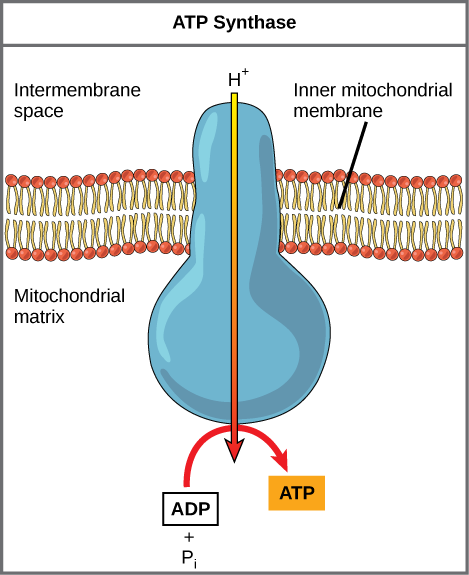
El dinitrofenol (DNP) es un desacoplador que hace que la membrana mitocondrial interna tenga fugas a los protones. Se utilizó hasta 1938 como medicamento para bajar de peso. ¿Qué efecto esperarías que tuviera la DNP en el cambio de pH a través de la membrana mitocondrial interna? ¿Por qué crees que este podría ser un medicamento eficaz para bajar de peso?
La quimiósmosis (Figura\(\PageIndex{3}\)) se utiliza para generar 90 por ciento del ATP producido durante el catabolismo aeróbico de glucosa; también es el método utilizado en las reacciones lumínicas de la fotosíntesis para aprovechar la energía de la luz solar en el proceso de fotofosforilación. Recordemos que la producción de ATP utilizando el proceso de quimioósmosis en las mitocondrias se denomina fosforilación oxidativa. El resultado global de estas reacciones es la producción de ATP a partir de la energía de los electrones retirados de los átomos de hidrógeno. Estos átomos eran originalmente parte de una molécula de glucosa. Al final de la ruta, los electrones se utilizan para reducir una molécula de oxígeno a iones de oxígeno. Los electrones adicionales en el oxígeno atraen iones de hidrógeno (protones) del medio circundante, y se forma agua.
Conexión de arte
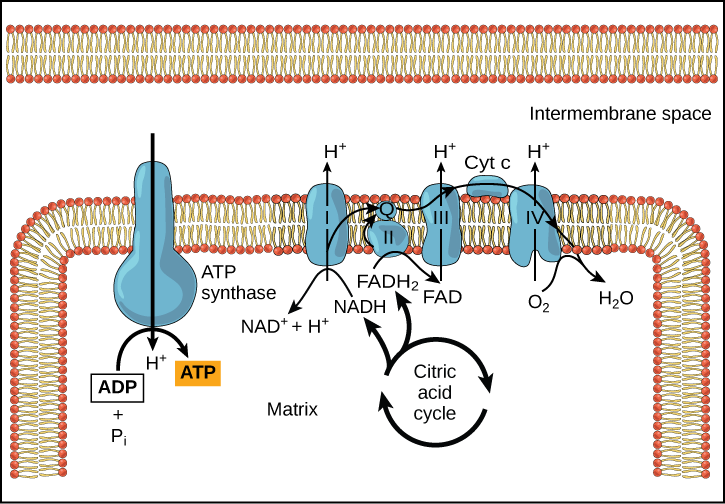
El cianuro inhibe la citocromo c oxidasa, un componente de la cadena de transporte de electrones. Si se produce envenenamiento por cianuro, ¿esperaría que el pH del espacio intermembrana aumente o disminuya? ¿Qué efecto tendría el cianuro en la síntesis de ATP?
Rendimiento ATP
El número de moléculas de ATP generadas a partir del catabolismo de la glucosa varía. Por ejemplo, el número de iones hidrógeno que los complejos de la cadena de transporte de electrones pueden bombear a través de la membrana varía entre especies. Otra fuente de varianza proviene de la lanzadera de electrones a través de las membranas de las mitocondrias. (El NADH generado a partir de la glucólisis no puede ingresar fácilmente a las mitocondrias). Así, los electrones son captados en el interior de las mitocondrias por NAD + o FAD +. Como ya has aprendido anteriormente, estas moléculas FAD + pueden transportar menos iones; en consecuencia, se generan menos moléculas de ATP cuando FAD + actúa como portador. NAD + se utiliza como transportador de electrones en el hígado y FAD + actúa en el cerebro.
Otro factor que afecta el rendimiento de las moléculas de ATP generadas a partir de la glucosa es el hecho de que los compuestos intermedios en estas vías se utilizan para otros fines. El catabolismo de la glucosa se conecta con las vías que construyen o descomponen todos los demás compuestos bioquímicos en las células, y el resultado es algo más desmesurado que las situaciones ideales descritas hasta ahora. Por ejemplo, los azúcares distintos de la glucosa se alimentan en la vía glucolítica para la extracción de energía. Además, los azúcares de cinco carbonos que forman ácidos nucleicos están hechos de intermedios en la glucólisis. Ciertos aminoácidos no esenciales pueden elaborarse a partir de intermedios tanto de la glucólisis como del ciclo del ácido cítrico. Los lípidos, como el colesterol y los triglicéridos, también se elaboran a partir de intermedios en estas vías, y tanto los aminoácidos como los triglicéridos se descomponen para obtener energía a través de estas vías. En general, en los sistemas vivos, estas vías del catabolismo de la glucosa extraen alrededor del 34 por ciento de la energía contenida en la glucosa.
Resumen
La cadena de transporte de electrones es la porción de respiración aeróbica que utiliza oxígeno libre como aceptor final de electrones de los electrones eliminados de los compuestos intermedios en el catabolismo de glucosa. La cadena de transporte de electrones está compuesta por cuatro grandes complejos multiproteicos incrustados en la membrana mitocondrial interna y dos pequeños portadores de electrones difusibles que transportan electrones entre ellos. Los electrones pasan a través de una serie de reacciones redox, con una pequeña cantidad de energía libre utilizada en tres puntos para transportar iones de hidrógeno a través de una membrana. Este proceso contribuye al gradiente utilizado en la quimioósmosis. Los electrones que pasan a través de la cadena de transporte de electrones pierden energía gradualmente, los electrones de alta energía donados a la cadena por NADH o FADH 2 completan la cadena, ya que los electrones de baja energía reducen las moléculas de oxígeno y forman agua. El nivel de energía libre de los electrones cae de aproximadamente 60 kcal/mol en NADH o 45 kcal/mol en FADH 2 a aproximadamente 0 kcal/mol en agua. Los productos finales de la cadena de transporte de electrones son el agua y el ATP. Varios compuestos intermedios del ciclo del ácido cítrico pueden desviarse hacia el anabolismo de otras moléculas bioquímicas, como aminoácidos no esenciales, azúcares y lípidos. Estas mismas moléculas pueden servir como fuentes de energía para las vías de la glucosa.
Conexiones de arte
Figura\(\PageIndex{2}\): El dinitrofenol (DNP) es un desacoplador que hace que la membrana mitocondrial interna gotee a los protones. Se utilizó hasta 1938 como medicamento para bajar de peso. ¿Qué efecto esperarías que tuviera la DNP en el cambio de pH a través de la membrana mitocondrial interna? ¿Por qué crees que este podría ser un medicamento eficaz para bajar de peso?
- Contestar
-
Después del envenenamiento por DNP, la cadena de transporte de electrones ya no puede formar un gradiente de protones, y la ATP sintasa ya no puede producir ATP. El DNP es un medicamento dietético eficaz porque desempareja la síntesis de ATP; es decir, después de tomarlo, una persona obtiene menos energía de los alimentos que come. Curiosamente, uno de los peores efectos secundarios de este medicamento es la hipertermia, o sobrecalentamiento del cuerpo. Dado que no se puede formar ATP, la energía del transporte de electrones se pierde como calor.
Figura\(\PageIndex{3}\): El cianuro inhibe la citocromo c oxidasa, un componente de la cadena de transporte de electrones. Si se produce envenenamiento por cianuro, ¿esperaría que el pH del espacio intermembrana aumente o disminuya? ¿Qué efecto tendría el cianuro en la síntesis de ATP?
- Contestar
-
Después del envenenamiento por cianuro, la cadena de transporte de electrones ya no puede bombear electrones al espacio intermembrana. El pH del espacio intermembrana aumentaría, el gradiente de pH disminuiría y la síntesis de ATP se detendría.
Glosario
- ATP sintasa
- (también, F1F0 ATP sintasa) complejo proteico embebido en la membrana que agrega un fosfato al ADP con energía de protones que se difunden a través de él
- grupo protésico
- (también, cofactor protésico) molécula unida a una proteína que facilita la función de la proteína
- ubiquinona
- transportador de electrones soluble en la cadena de transporte de electrones que conecta el primer o segundo complejo con el tercero


