2.4: Átomos, Isótopos, Iones y Moléculas - La Tabla Periódica
- Page ID
- 57610
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
- Discutir la organización de la tabla periódica
Materia y Elementos
La materia comprende todos los objetos físicos del universo, aquellos que ocupan el espacio y tienen masa. Toda la materia está compuesta por átomos de uno o más elementos, sustancias puras con propiedades químicas y físicas específicas. Hay 98 elementos que ocurren naturalmente en la tierra, sin embargo, los sistemas vivos utilizan un número relativamente pequeño de estos. Las criaturas vivientes están compuestas principalmente por solo cuatro elementos: carbono, hidrógeno, oxígeno y nitrógeno (a menudo recordados por las siglas CHON). A medida que los elementos se unen, forman compuestos que a menudo tienen nuevas propiedades emergentes que son diferentes de las propiedades de los elementos individuales. La vida es un ejemplo de una propiedad emergente que surge de la colección específica de moléculas que se encuentran en las células.

Elementos del cuerpo humano dispuestos por porcentaje de la masa total: Se cree que 25 elementos juegan un papel activo en la salud humana. El carbono, el hidrógeno, el oxígeno y el nitrógeno constituyen aproximadamente el 96% de la masa en un cuerpo humano.
La Tabla Periódica
Los diferentes elementos se organizan y muestran en la tabla periódica. Ideada por el químico ruso Dmitri Mendeleev (1834—1907) en 1869, la tabla agrupa elementos que, aunque únicos, comparten ciertas propiedades químicas con otros elementos. En la tabla periódica los elementos se organizan y muestran de acuerdo a su número atómico y se organizan en una serie de filas (periodos) y columnas (grupos) basados en propiedades químicas y físicas compartidas. Si miras una tabla periódica, verás los grupos numerados en la parte superior de cada columna de izquierda a derecha comenzando con 1 y terminando con 18. Además de proporcionar el número atómico para cada elemento, la tabla periódica también muestra la masa atómica del elemento. Mirando al carbono, por ejemplo, aparecen su símbolo (C) y nombre, así como su número atómico de seis (en la esquina superior izquierda) y su masa atómica de 12.11.

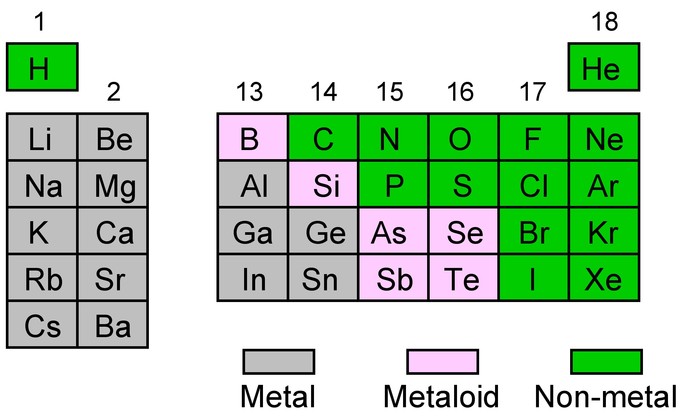
La disposición de la tabla periódica permite agrupar los elementos de acuerdo a sus propiedades químicas. Dentro de los elementos principales del grupo (Grupos 1-2, 13-18), hay algunas tendencias generales que podemos observar. Cuanto más abajo de un grupo dado, los elementos tienen un carácter metálico aumentado: son buenos conductores tanto de calor como de electricidad, sólidos a temperatura ambiente y aspecto brillante. Al moverse de izquierda a derecha a lo largo de un período, los elementos tienen mayor carácter no metálico. Estos elementos son aislantes, malos conductores de calor y pueden existir en diferentes fases a temperatura ambiente (sólido quebradizo, líquido o gas). Los elementos en el límite entre los elementos metálicos (elementos grises) y los elementos no metálicos (elementos verdes) son de carácter metaloide (elementos rosados). Tienen baja conductividad eléctrica que aumenta con la temperatura. También comparten propiedades tanto con los metales como con los no metales.
Hoy en día, la tabla periódica continúa expandiéndose a medida que se sintetizan elementos cada vez más pesados en los laboratorios. Estos grandes elementos son extremadamente inestables y, como tales, son muy difíciles de detectar; pero su creación continua es un desafío continuo emprendido por científicos de todo el mundo.
Puntos Clave
- Toda la materia está hecha de átomos de uno o más elementos. Las criaturas vivientes consisten principalmente en carbono, hidrógeno, oxígeno y nitrógeno (CHON).
- La combinación de elementos crea compuestos que pueden tener propiedades emergentes.
- La tabla periódica es una lista de los elementos según el número atómico creciente que se organiza además en columnas basadas en propiedades físicas y químicas similares y configuración electrónica.
- A medida que uno se mueve hacia abajo por una columna o a través de una fila, hay algunas tendencias generales para las propiedades de los elementos.
- La tabla periódica continúa expandiéndose hoy en día a medida que se crean elementos cada vez más pesados en laboratorios de todo el mundo.
Términos Clave
- Elemento: Sustancias químicas puras que consisten en un solo tipo de átomo con un conjunto definido de propiedades químicas y físicas.
- propiedades emergentes: Propiedades encontradas en estructuras compuestas que son diferentes a las de los componentes individuales y que no se predecirían en base a las propiedades de los componentes individuales.
- tabla periódica: Una tabla tabular de los elementos químicos según sus números atómicos para que los elementos con propiedades similares estén en la misma columna.


