3.7: Día 24- Enzimas y Catálisis Enzimática
- Page ID
- 78851
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)22
Día 24: Enzimas y Catálisis Enzimática
Enzimas D24.1
Millones de reacciones químicas ocurren dentro de cada una de nuestras células cada minuto. Sin catalizadores, muchas de estas reacciones proceden a una velocidad extremadamente lenta. Por ejemplo, la disociación del ácido carbónico que tiene lugar en los pulmones:
H 2 CO 3 (aq) → CO 2 (g) + H 2 O (l)
solo procede a una tasa de ~10 -7 m/s a temperatura ambiente. Sin embargo, el CO 2 necesita ser producido en nuestro cuerpo a una tasa mucho mayor que esta. Si bien teóricamente es posible acelerar la reacción elevando la temperatura, desafortunadamente, la mayor parte de la vida solo es compatible con un rango de temperatura limitado.
Los catalizadores biológicos, conocidos como enzimas, son cruciales para la vida ya que pueden acelerar las reacciones por factores de 10 6 -10 20. Por ejemplo, la enzima anhidrasa carbónica acelera la reacción anterior a temperatura ambiente en más de un millón de veces la velocidad de la reacción no catalizada.
Como todos los catalizadores, las enzimas actúan combinándose con reactantes y formando así estados de transición de energía más bajos. En una reacción catalizada por enzimas, el (los) reactivo (s) con el que se combina la enzima se denomina sustrato (s). A diferencia de los catalizadores químicos, las interacciones de una enzima con moléculas de sustrato son a menudo parcial o completamente no covalentes; es decir, las interacciones involucran enlaces de hidrógeno, atracciones iónicas o atracciones dipolo-dipolo.
Además, las reacciones catalizadas por enzimas son altamente específicas para un sustrato particular o una categoría particular de moléculas de sustrato. Se dice que las enzimas “reconocen” el sustrato, o clase de sustratos, para los cuales la enzima sirve como catalizador. Las interacciones enzimáticas con sustratos son a veces tan específicas que una enzima no reconoce una molécula que difiere de su sustrato preferido en tan poco como un solo grupo metilo (-CH 3), y muchas enzimas reconocerán un enantiómero pero no su imagen especular.
¿Cómo aceleran las enzimas las reacciones químicas y logran su especificidad? La respuesta a ambas preguntas radica en cómo interactúan las enzimas con sus sustratos. Típicamente, una enzima es una molécula de proteína, una macromolécula. Por lo general, solo una parte de la molécula enzimática grande interactúa con un sustrato. La parte de una molécula enzimática que interactúa con un sustrato se llama el sitio activo.
 Figura 1. Estructura de la enzima lisozima. Izquierda: estructura de bola y palo. Derecha: estructura de vuelos espaciales. Observe la “hendidura” en el medio del lado derecho de la molécula. Las moléculas cuyas reacciones son catalizadas por la lisozima encajan en la hendidura, que es el sitio activo de la enzima. (Estructuras de http://lysozyme.co.uk. )
Figura 1. Estructura de la enzima lisozima. Izquierda: estructura de bola y palo. Derecha: estructura de vuelos espaciales. Observe la “hendidura” en el medio del lado derecho de la molécula. Las moléculas cuyas reacciones son catalizadas por la lisozima encajan en la hendidura, que es el sitio activo de la enzima. (Estructuras de http://lysozyme.co.uk. )
En 1890, el químico Emil Fischer propuso que el sustrato encaje en el sitio activo de la enzima como una llave encaja en una cerradura. La llave (sustrato) tiene una forma molecular específica (disposición de grupos funcionales y otros átomos) que le permite, y ninguna otra llave, encajar en la cerradura (la enzima).
En 1958, Daniel E. Koshland Jr. modificó este modelo de cerradura y llave al proponer que la unión del sustrato a la enzima altera la configuración de ambos, proporcionando un mejor ajuste. Este modelo de ajuste inducido explica tanto el gran aumento en las velocidades de reacción como la especificidad de las reacciones catalizadas por enzimas:
- A medida que el sustrato interactúa con la enzima, el sustrato se distorsiona (los átomos se desplazan, los enlaces se estiran y los grupos reactivos se acercan) a una estructura más cercana al estado de transición de la reacción. Esto disminuye la energía del estado de transición, acelerando la reacción.
- Solo las moléculas con los grupos funcionales correctos en las configuraciones correctas son capaces de ser inducidas para que se ajusten al sitio activo de la enzima.
Durante muchos años, se creía que las únicas enzimas eran las proteínas. Recientemente, sin embargo, se han descubierto varias enzimas ARN. Estas enzimas se denominan ribozimas y exhiben todas las mismas características que las enzimas proteicas (Figura 2).

Cinética enzimática D24.2: Mecanismo Michaelis-Menten
El mecanismo Michaelis-Menten es un mecanismo de reacción de dos pasos que se aplica a muchas reacciones catalizadas por enzimas. Una enzima (E) se une con un sustrato (S) para formar un complejo enzima-sustrato (ES), que luego se separa para dar el producto (P) y regenera la enzima. La reacción general es:
S → P
con el sencillo mecanismo de dos pasos:
\[\begin{array}{rcl}&\text{step 1: (fast)}&\;\;\;\;\;\;\;\;\;\;\;E + S &\xrightleftharpoons[k_{-1}]{k_1}& ES\\[0.5em] &\text{step 2: (slow)}&\;\;\;\;\;\;\;\;\;\;\;ES &\xrightarrow{k_2}& P + E\end{array} \nonumber \]
El segundo paso es la determinación de la tasa. Los estudios de cinética enzimática se llevan a cabo típicamente midiendo la velocidad de reacción en función de la concentración de sustrato y la concentración de enzima. La velocidad de la reacción catalizada se puede medir observando la velocidad de producción del producto:
\[rate=\dfrac{\Delta[P]}{\Delta t}=k_2[ES] \nonumber \]
pero ES es un intermedio reactivo cuya concentración no se determina fácilmente. Necesitamos expresar la velocidad de reacción en términos de concentraciones que se midan fácilmente. Esto se puede hacer asumiendo que, una vez que se forma el intermedio reactivo, ES, su concentración permanece aproximadamente constante durante el resto de la reacción; esto se denomina aproximación en estado estacionario. Se diferencia de la aproximación de equilibrio que discutimos en la Sección D23.3 en que no es necesario asumir que el paso 1 ha alcanzado el equilibrio. La aproximación en estado estacionario es razonable, porque una vez que [ES] se acumula lo suficiente, las reacciones que consumen ES se vuelven más rápidas y evitan que la concentración aumente aún más.
Cuando la concentración del complejo enzima-sustrato alcanza un estado estacionario:
\[\dfrac{d[ES]}{dt}=0 \nonumber \]
El complejo ES se forma mediante la reacción directa en la etapa 1, y se hace reaccionar en la reacción inversa de la etapa 1 y la reacción directa de la etapa 2. Sumando las tasas de estas reacciones:
\[\dfrac{d[ES]}{dt}=0=k_1[E][S]-k_{-1}[ES]-k_2[ES] \nonumber \]
Reorganizar la ecuación para resolver para [ES] da:
\[(k_{-1}+k_2)[ES]=k_1[E][S] \nonumber \]
\[[ES]=\dfrac{k_1[E][S]}{k_{-1}+k_2} \nonumber \]
o:
\[[ES]=\dfrac{[E][S]}{K_M} \nonumber \]
donde K M es la constante de Michaelis:
\[K_M=\dfrac{k_{-1}+k_2}{k_1} \nonumber \]
Es difícil conocer la concentración exacta de la enzima libre ([E]) en un momento dado. Sin embargo, sí conocemos la concentración total de enzima, [E] total (la enzima debe estar en su forma sin reaccionar (E) o combinada con sustrato (ES)):
[E] total = [E] + [ES]
Sustituir en la ecuación anterior da:
\[[ES]=\dfrac{([E]_{\text{total}}-[ES])[S]}{K_M} \nonumber \]
La reorganización de las variables da:
\[[ES]=\dfrac{[E]_{\text{total}}[S]}{K_M}-\dfrac{[ES][S]}{K_M} \nonumber \]
\[\dfrac{[ES][S]}{K_M}+[ES]=\dfrac{[E]_{\text{total}}[S]}{K_M} \nonumber \]
\[\left(\dfrac{[S]+K_M}{K_M}\right)[ES]=\dfrac{[E]_{\text{total}}[S]}{K_M} \nonumber \]
\[[ES]=\left(\dfrac{[E]_{\text{total}}[S]}{K_M}\right)\left(\dfrac{K_M}{[S]+K_M}\right)=\dfrac{[E]_{\text{total}}[S]}{[S]+K_M} \nonumber \]
Sustituir la expresión por [ES] en la expresión por la velocidad de reacción en términos de [ES} da
\[rate=\dfrac{\Delta[P]}{\Delta t}=\dfrac{k_2[E]_{\text{total}}[S]}{[S]+K_M} \nonumber \]
o
\[rate=\dfrac{V_{\text{max}}[S]}{[S]+K_M}\;\;\;\text{Michaelis-Menten equation} \nonumber \]
donde V max = k 2 [E] total es la velocidad máxima que puede alcanzar la reacción. Hay dos casos limitantes para esta ecuación, dependiendo de los tamaños relativos de [S] y K M.
Si hay mucho sustrato, [S] ≫ K M, y por tanto [S] + K M ≈ [S]. En este caso la ecuación de Michaelis-Menten se convierte en
\[\text{rate}=\dfrac{V_{\text{max}}[S]}{[S]}=V_{\text{max}}=k_2[E]_{\text{total}} \nonumber \]
La reacción alcanza su velocidad máxima, velocidad = V máx. La velocidad de reacción depende únicamente del [E] total y es independiente de [S]. Esto sucede cuando casi todas las moléculas enzimáticas tienen una molécula sustrato en el sitio activo, lo que significa que aumentar la concentración de sustrato ya no puede aumentar la concentración del complejo enzima-sustrato (y así ya no puede aumentar la velocidad).
Si hay una concentración muy pequeña de sustrato, [S] K M, tenemos [S] + K M ≈ K M, y la ecuación de Michaelis-Menten se convierte en primer orden en [S]:
\[rate=\left(\dfrac{V_{\text{max}}}{K_M}\right)[S] \nonumber \]
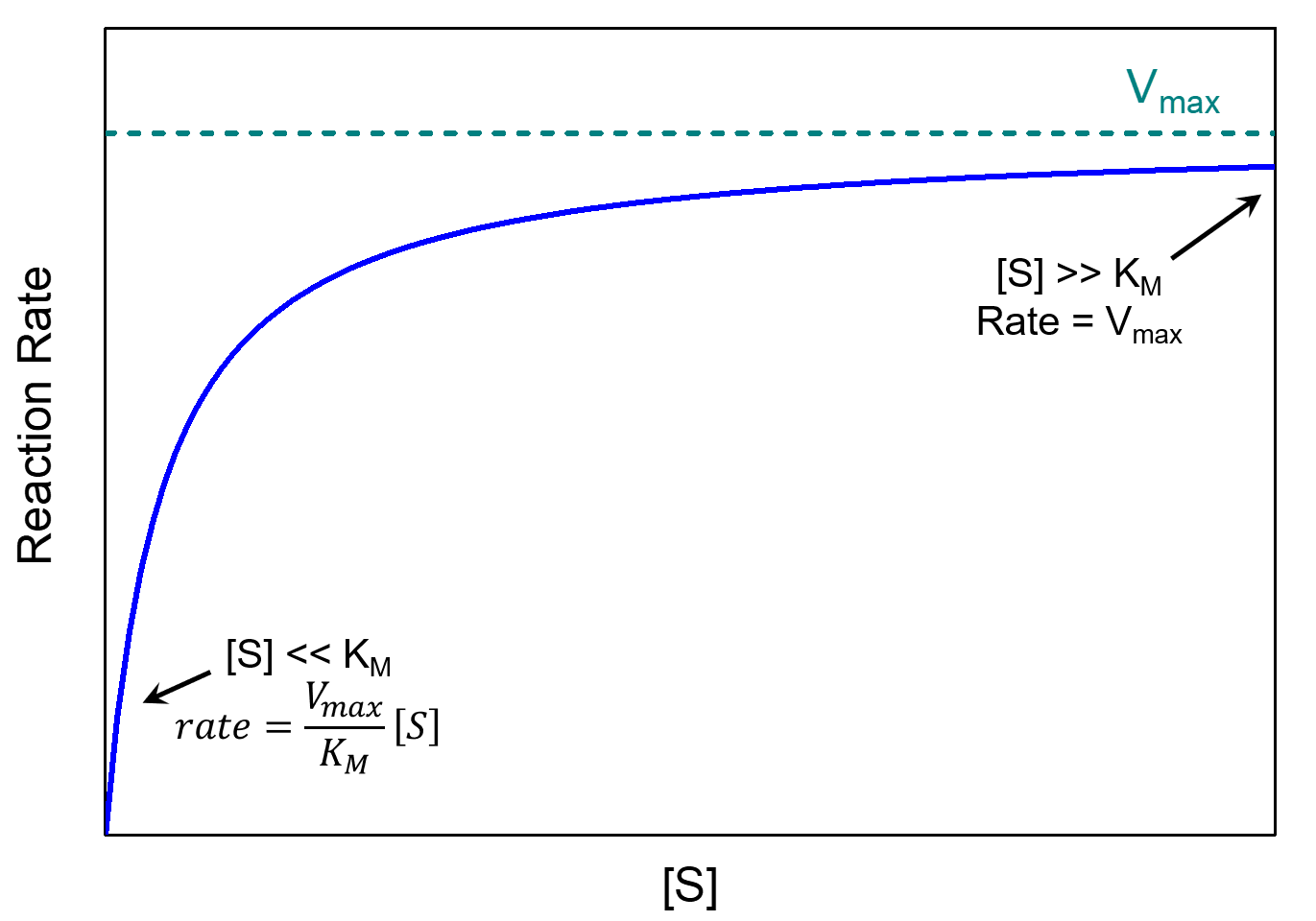
La constante de Michaelis es una medida inversa de la afinidad del sustrato por la enzima, una K M pequeña indica alta afinidad, lo que significa que la velocidad se acerca a V max más rápidamente. El valor de K M depende tanto de la enzima como del sustrato, así como de las condiciones de reacción como la temperatura y el pH.
D24.3 desnaturalización de enzimas e inhibidores
La desnaturalización es un proceso en el que las proteínas pierden su estructura cuaternaria, terciaria y secundaria (ver Sección D15.6). Las enzimas deben doblarse en la forma 3D correcta para funcionar. Pero los enlaces de hidrógeno, que juegan un papel importante en el plegamiento de proteínas, son bastante débiles, y no se necesita mucho calor, acidez u otro estrés para romper algunos enlaces de hidrógeno y desnaturalizar la enzima.
Por lo tanto, las reacciones catalizadas por enzimas exhiben una dependencia inusual de la temperatura. A temperaturas relativamente bajas, la velocidad de reacción aumenta con la temperatura, como se esperaba. Sin embargo, a temperaturas más altas, la velocidad de reacción disminuye drásticamente debido a la desnaturalización de la enzima, como se muestra en la Figura 4.

Por lo general, las enzimas no se desnaturalizarán a temperaturas típicamente encontradas por el organismo vivo en el que se encuentran. Como resultado, las enzimas de bacterias que viven en ambientes de alta temperatura, como las aguas termales, son apreciadas por los usuarios industriales por su capacidad para funcionar a altas temperaturas.
Un inhibidor (I) interactúa con una enzima para disminuir la eficiencia catalítica de la enzima. Un inhibidor irreversible se une covalentemente al sitio activo de la enzima, produciendo una pérdida permanente en la eficiencia catalítica aunque la concentración del inhibidor disminuya posteriormente. Un inhibidor reversible forma un complejo no covalente con la enzima, resultando en una disminución temporal de la eficiencia catalítica. La reducción de la concentración de un inhibidor reversible devuelve la eficiencia catalítica de la enzima a su nivel normal.
Existen varios tipos de inhibición reversible. En la inhibición competitiva el sustrato y el inhibidor compiten por el mismo sitio activo en la enzima. Debido a que el sustrato no puede unirse a un complejo enzima-inhibidor (EI), la concentración de enzima disponible para formar el complejo enzima-sustrato es menor y la reacción catalizada por enzimas es más lenta. Con una inhibición no competitiva, el inhibidor se une al complejo enzima-sustrato pero no al sitio activo, formando un complejo enzima-sustrato-inhibidor (ESI). La formación de un complejo ESI disminuye la eficiencia catalítica debido a que parte del complejo enzima-sustrato ha reaccionado con inhibidor. Esto reduce la concentración de ES, lo que reduce la velocidad del paso limitante de velocidad en el mecanismo. Finalmente, en la inhibición no competitiva el inhibidor se une tanto a la enzima misma como al complejo enzima-sustrato en un sitio diferente al sitio activo. Al igual que en la inhibición no competitiva, esto forma un complejo ESI inactivo y reduce la concentración de ES.

Figura 5. Mecanismos para la inhibición reversible de la catálisis enzimática. E: enzima, S: sustrato, P: producto, I: inhibidor, ES: complejo enzima-sustrato, EI: complejo enzima-inhibidor, ESI: complejo enzima-sustrato-inhibidor.
Pregunta Podia
Considere el mecanismo de reacción para la cinética enzimática de Michaelis-Menten en la Sección D24.2:
1. Dibuja un diagrama de energía de reacción para esta reacción. Si necesita hacer alguna suposición para dibujar el diagrama, describa cada suposición. Además, describe qué partes del diagrama puedes dibujar definitivamente dada la información en la Sección D24.2.
2. Supongamos que un inhibidor competitivo reversible está presente durante la reacción catalizada por enzimas. ¿Cómo afecta la presencia de este inhibidor al diagrama de energía de reacción?
Dos días antes de la próxima sesión de toda la clase, esta pregunta de Podia se pondrá en vivo en Podia, donde podrás enviar tu respuesta.


