11.5: Teorías del sueño
- Page ID
- 148311
- Evaluar las funciones del sueño en relación con los mecanismos biológicos subyacentes y afectados por él.
- Describir la naturaleza circadiana del sueño.
- Describir la teoría homeostática o recuperativa del sueño, y otras teorías de por qué dormimos.
Visión general
Cuando le preguntas a la mayoría de las personas por qué piensan que duermen, la respuesta es “para que pueda descansar” o “porque estoy cansado de las actividades del día”. No obstante, los animales que trabajan más duro no duermen más tiempo e incluso después de pasar toda la noche no dormimos todo el día siguiente para compensar la falta de sueño. Hay dos teorías del sueño que funcionan en conjunto para explicar por qué dormimos: recuperativa y circadiana.
Las investigaciones indican que para que alguien pueda conciliar el sueño, dos procesos corporales deben estar debidamente sincronizados. El primero es el ritmo circadiano, que tiene un periodo de 24 horas y se rige por el reloj biológico de tu cuerpo. El ritmo circadiano controla la secreción cíclica de varias hormonas, entre ellas la melatonina, que intervienen en el sueño. El segundo proceso es la función recuperativa ilustrada por la acumulación de sustancias hipnogénicas en tu cuerpo durante 16 horas todos los días. Estas sustancias inducen un deseo de dormir que no desaparece hasta que de hecho duermes un poco.
Por lo tanto, solo puedes conciliar el sueño cuando se han cumplido dos condiciones: el reloj biológico de tu cuerpo debe haberlo llevado a un equilibrio hormonal propicio para dormir, y debe haber sido un buen rato desde la última vez que dormiste, de modo que tus niveles de sustancias hipnogénicas (productoras de sueño) se hayan acumulado suficientemente. En la siguiente sección se describen estas dos teorías con mayor detalle, así como otras funciones del sueño.
Regulación del sueño y ritmos circadianos: un modelo de dos procesos
El sueño es un proceso dinámico que se ajusta a las necesidades del cuerpo todos los días. A qué hora te duermes, cuánto tiempo duermes y qué tan bien duermes resultan de los efectos combinados de dos fuerzas: la deuda homeostática y la fase de tu ritmo circadiano. Los individuos, por supuesto, difieren en cuanto a qué hora se acuestan y cuánto duermen necesitan para funcionar bien, pero en general, las características del sueño pueden considerarse como el resultado de complejas interacciones entre dos procesos.
El primero de estos procesos se llama deuda homeostática (ver más abajo) o teoría recuperativa, que aumenta en función de cuánto tiempo llevas despierto y disminuye a medida que duermes. El proceso es algo así como la arena que se acumula en un extremo de un reloj de arena y tiene que vaciarse en el otro después de cierto tiempo. Consulte la Figura\(\PageIndex{1}\) para ver una gráfica de cómo la presión para dormir aumenta en función del tiempo que pasamos despiertos, y luego disminuye a medida que dormimos.
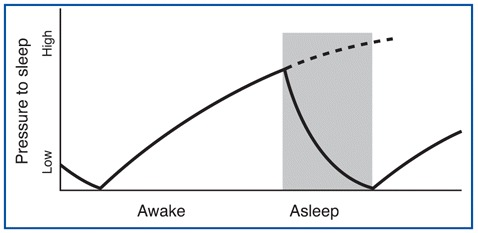
El segundo proceso que influye mucho en el inicio, la duración y la calidad de tu sueño es la fase de tu ritmo circadiano. Esta fase se rige por tu reloj biológico, cuyo ritmo es endógeno pero se restablece regularmente a la luz del día. Por lo tanto, este reloj produce un ciclo que dura aproximadamente 24 horas durante el cual los tiempos óptimos para conciliar el sueño, soñar, despertarse y hacer el trabajo ocurren a lo largo de cada día. Las señales externas o zeitgebers (alemán para “dadores de tiempo”) -de las cuales la luz solar es la más importante- arrastran tu reloj corporal endógeno (interno) para que caiga en línea con el día de la tierra.
Los ritmos endógenos del sueño se pueden representar gráficamente. La figura muestra una representación día a día del ciclo sueño/vigilia de un individuo. Las líneas negras indican periodos de sueño, y las líneas grises indican periodos de vigilia. La porción superior de la figura (días 1 a 9) representa el ciclo normal de sueño/vigilia de este individuo. En estas condiciones, el individuo está expuesto a una exposición regularmente cronometrada a luz diurna y oscuridad alternas, lo que ha arrastrado el ciclo de sueño/vigilia de esta persona a un periodo de 24 horas.
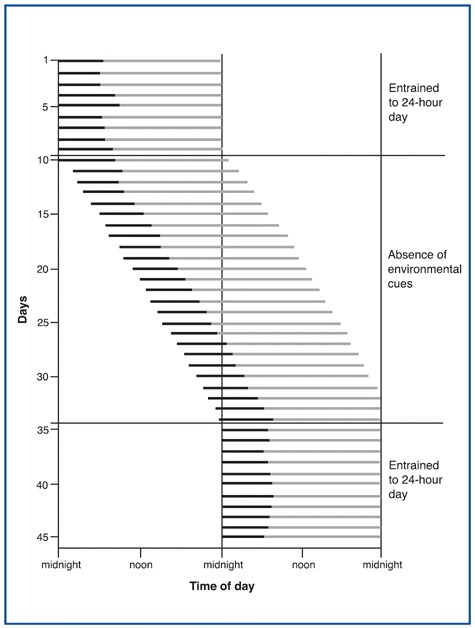
Así, todo tu ciclo sueño-vigilia funciona como si tu oscilador circadiano hiciera más fácil conciliar el sueño en ciertos momentos del día, haciéndote mucho más dormido de 1:00 PM a 4:00 PM, e incluso más dormido de 2:00 AM a 5:00 AM. Estos patrones son confirmados por las estadísticas sobre accidentes laborales y viales.
Este modelo de dos procesos -homeostático y circadiano- para regular el sueño puede ser diagramado como un péndulo doble.
En circunstancias normales, tus periodos de actividad y descanso están en fase con la alternancia de día y noche: tu péndulo “circadiano” y tu péndulo “homeostático” están sincronizados, duermes bien cuando te duermes y funcionas bien cuando te despiertas.
Pero cuando se altera esta relación y los dos péndulos ya no están en fase, entonces la calidad tanto de tu sueño como de tu desempeño cuando estás despierto se deterioran significativamente. Los picos de actividad para varios marcadores circadianos ocurren en momentos incómodos en el ciclo sueño-vigilia, que es la fuente de los problemas causados por el jet lag y por los turnos nocturnos de trabajo.
En otras palabras, cuanto más tiempo permanezcas despierto, mayor será la presión que sentirás para ir a dormir. Este proceso de deuda homeostática, o deuda de sueño, también explica por qué, si te quedas despierto toda la noche, entonces a la noche siguiente, no sólo vas a dormir más tiempo, sino que tu porcentaje de sueño profundo será mayor.
Moléculas que se acumulan y te hacen dormir — Adenosina y Melatonina
A medida que cada día llega a su fin, sientes la necesidad de acostarte e irte a dormir. El inicio del sueño, que parece un fenómeno tan simple desde una perspectiva conductual, en realidad es bastante complejo a partir de uno molecular.
Adenosina y homeostasis/recuperación
Fue a principios de la década de 1980 cuando los científicos descubrieron por primera vez el mecanismo químico por el cual tomar café ayuda a las personas a mantenerse despiertas: la cafeína, la sustancia psicoactiva en el café, evita que la adenosina se una a ciertas neuronas del cerebro. Tanto la cafeína en el café como la teofilina en el té son ejemplos de tales antagonistas de adenosina y son bien conocidos por sus efectos estimulantes.
Una vez realizado este descubrimiento, la adenosina se convirtió en un tema de interés para cada vez más neurobiólogos que estaban haciendo investigaciones sobre el sueño. Numerosos experimentos con animales finalmente confirmaron que la adenosina definitivamente juega un papel en el ciclo de sueño/vigilia. Algunos de los hallazgos experimentales que llevaron a esta conclusión: a) bloquear los efectos de la adenosina alertó a los animales; b) inyectar a los animales un agonista de adenosina (potenciador) provocó que se durmieran; c) en ciertas partes del cerebro, la concentración de adenosina normalmente aumenta de forma natural durante el día y disminuye por la noche, pero si los animales se ven obligados a permanecer despiertos por la noche, esta concentración sigue aumentando.
Estos experimentos demostraron así que la adenosina, junto con otros químicos como la serotonina y la melatonina, es una de las moléculas cuya concentración en el cerebro influye en el inicio del sueño.
La adenosina es producida por la degradación del trifosfato de adenosina (ATP), la molécula que sirve como “moneda de energía” para las diversas funciones celulares del cuerpo. La cantidad de adenosina producida en el cerebro refleja así el nivel de actividad de sus neuronas y células gliales. La intensa actividad cerebral durante los periodos de vigilia consume grandes cantidades de ATP y por lo tanto hace que la adenosina se acumule.
Glucogen=Reservas de ATP o moneda de energía del cerebro
El cerebro usa energía —> ATP se degrada en adenosina
Más energía cerebral utilizada = más adenosina se acumula
Más niveles de adenosina —> Desencadenado por sueño no REM
Sueño no REM = cerebro menos activo —> recuperación/reconstrucción de reservas de glucógeno
La acumulación de adenosina durante los períodos de vigilia se asocia así con el agotamiento de las reservas de ATP almacenadas como glucógeno en el cerebro. El aumento de los niveles de adenosina desencadena el sueño no REM, durante el cual el cerebro está menos activo, colocándolo así en una fase de recuperación que es absolutamente esencial, entre otras cosas, para permitir que reconstruya sus reservas de glucógeno.
Pero, ¿cómo ejerce exactamente esta influencia la adenosina? Durante los periodos de vigilia, la actividad neuronal aumenta la concentración de adenosina, lo que tiene un efecto inhibitorio sobre un gran número de neuronas. Entre estas se encuentran las neuronas de los sistemas hormonales que son las más activas cuando estamos despiertos: los sistemas de norepinefrina, acetilcolina y serotonina. Los experimentos han demostrado, por ejemplo, que cuando los niveles de adenosina en el prosencéfalo basal se elevan artificialmente, las neuronas en esta estructura que proyectan axones por toda la corteza producen menos acetilcolina. Como resultado, la actividad cortical se ralentiza y el individuo se queda dormido.
La actividad cerebral sincronizada característica del sueño no REM puede entonces establecerse. Pero una vez que el sueño no REM ha continuado por un tiempo, los niveles de adenosina comienzan a disminuir. Los sistemas responsables de la vigilia pueden entonces comenzar a ser más activos, haciendo que el individuo despierte y que el ciclo comience de nuevo. Así vemos que el ciclo sueño/vigilia implica un bucle de retroalimentación negativa altamente eficiente.
Ritmos circadianos
Existen dos estructuras importantes para el ciclo circadiano que podrían considerarse nuestros relojes biológicos.
Núcleos supraquiasmáticos y glándula pineal y melatonina
La mayoría de las funciones y comportamientos corporales humanos no son “estado estacionario”. En cambio, fluctúan en ciclos de 24 horas, como el ciclo de dormir y vigilia y los ciclos para la temperatura corporal, el hambre y la secreción de diversas hormonas. El reloj central que regula todos estos ciclos circadianos se localiza en dos pequeñas estructuras en el cerebro, en la base del hipotálamo izquierdo y derecho. Cada una de estas estructuras no es más grande que una punta de lápiz y contiene varias decenas de miles de neuronas. Estas estructuras se denominan núcleos supraquiasmáticos (como se mencionó anteriormente en la sección *) porque se encuentran justo por encima del quiasma óptico, donde se cruzan los nervios ópticos izquierdo y derecho.
Esta posición estratégica permite que los núcleos supraquiasmáticos reciban proyecciones del nervio óptico de células ganglionares retinianas especiales que les informan sobre la intensidad de la luz ambiental que ingresa a los ojos. Las neuronas de estos núcleos utilizan esta información para resincronizarse con la luz del día todos los días, porque como cualquier reloj, el reloj biológico humano no es perfecto y sí necesita ser reajustado periódicamente. Una cosa interesante de la trayectoria retinohipotalámica es que está separada de las de visión tal que incluso las personas ciegas (y las ratas topo ciegas, una especie que de otra manera es ciega) reciben información de la luz para restablecer sus relojes biológicos.
A pesar de esta necesidad de resincronizar con una señal externa, se ha demostrado que los núcleos supraquiasmáticos de hecho constituyen un reloj biológico con su propio ritmo independiente. En primer lugar, muchos experimentos han demostrado que las[1] fluctuaciones del ciclo circadiano humano persisten incluso cuando los individuos están separados de la luz del día. Segundo, en experimentos donde los núcleos supraquiasmáticos fueron destruidos en animales como los hámsters, sus comportamientos cíclicos, como sus ciclos de sueño/vigilia, se desorganizan por completo. Y cuando luego se trasplantaron núcleos supraquiasmáticos de fetos de hámster a estos animales, sus ritmos biológicos regresaron, pero con las propiedades de los donantes.
Estos hallazgos indican que el mecanismo del reloj biológico de los mamíferos es de hecho no solo endógeno, sino también de origen genético. Los científicos ahora incluso han determinado que estos ritmos son el resultado de la actividad cíclica de ciertos genes.
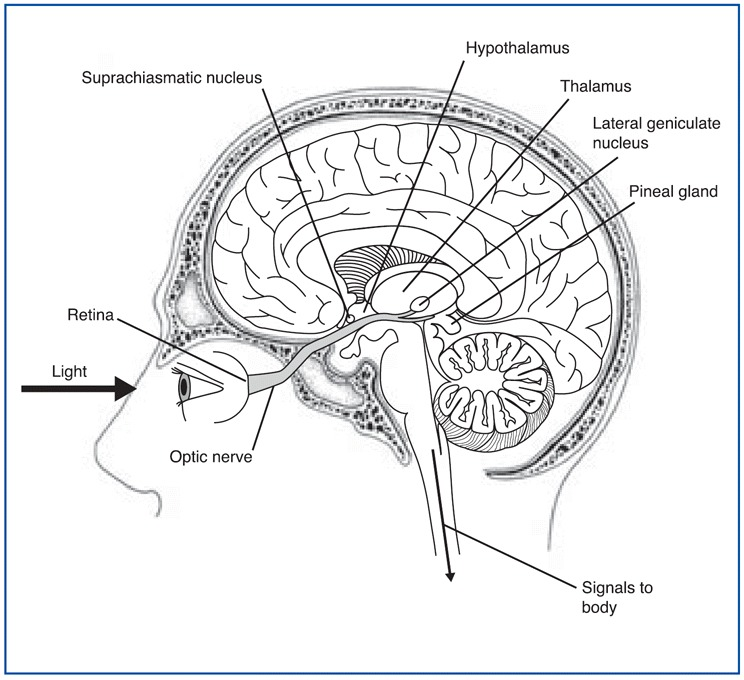
En la figura se muestra el circuito de luz que entra al ojo, la señal que va al SCN y a la glándula pineal\(\PageIndex{4}\). La melanopsina en las células ganglionares retinianas del ojo responde a la luz (natural o artificialmente) y transmite señales al SCN. Luego, la activación del SCN inducida por la luz impide que la glándula pineal produzca melatonina y; a la inversa, la producción y secreción de melatonina aumenta durante el período oscuro.
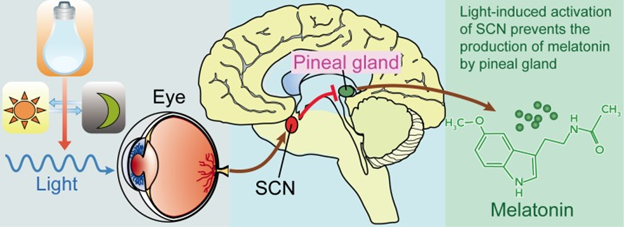
Glándula pineal
Usando estos ritmos cíclicos, los núcleos supraquiasmáticos envían señales a lo largo de sus vías de salida, por ejemplo, a la glándula pineal, para regular los ciclos de una serie de funciones fisiológicas y conductuales. En aves, reptiles y peces, esta pequeña glándula ubicada en la parte superior del cerebro es sensible a la luz y coordina algunos fenómenos cíclicos por sí sola. En los mamíferos, sin embargo, aunque la glándula pineal (mencionada anteriormente en la sección 12.2) conserva su capacidad de producir secreciones cíclicamente (específicamente, la hormona melatonina, por la noche), no constituye un reloj por sí sola; en cambio, su síntesis cíclica de melatonina está controlada por señales de temporización que recibe del SCN.
Cada día, la glándula pineal comienza a producir melatonina (a veces llamada la “hormona del sueño”) a medida que cae la noche. A medida que aumenta el nivel de melatonina en la sangre, la temperatura corporal disminuye ligeramente y el individuo se siente más dormido y dormido. El nivel de melatonina permanece alto por apenas unas 12 horas, luego comienza a caer nuevamente en la madrugada, ya que la luz del día (a través del SCN) inhibe la actividad de esta glándula.
El principal neurotransmisor que regula la actividad de la glándula pineal es la norepinefrina. Cuando la norepinefrina se une a sus receptores, desencadena una cascada de segundos mensajeros, incluyendo AMP cíclico. Este AMP cíclico contribuye a la síntesis de melatonina. Esta melatonina se libera en el torrente sanguíneo, a través del cual llega a todos los órganos del cuerpo. Es así como participa en la modulación de los circuitos del tronco encefálico que finalmente controlan el ciclo sueño-vigilia.
Salida de SCN
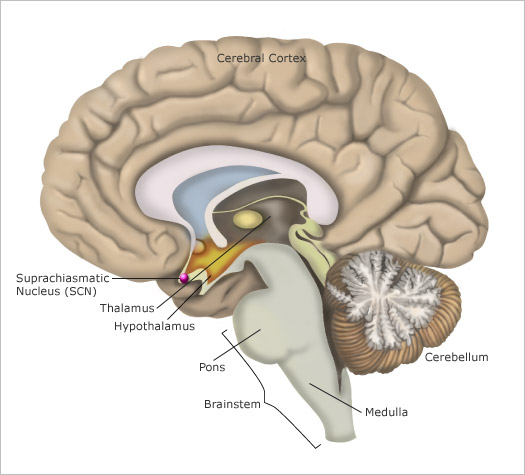
Las vías de salida de cada SCN (ver Figura\(\PageIndex{4}\) para otra imagen de su ubicación) consisten en axones que inervan principalmente el hipotálamo y las estructuras cercanas. Algunos de estos axones también se proyectan hacia otras partes del prosencéfalo, mientras que otros se proyectan hacia el mesencéfalo.
Los científicos aún no conocen los detalles de cómo el reloj biológico central en el SCN regula tantos comportamientos cíclicos humanos diferentes. Pero sí saben que usa la glándula pineal para hacerlo, y han demostrado que destruir las vías de salida del SCN también destruye los ritmos circadianos del cuerpo. Debido a que el GABA es el neurotransmisor esencial para casi todas las neuronas del SCN, uno esperaría un efecto inhibitorio sobre las neuronas que inervan. Además de enviar mensajes a lo largo de estas vías axonales, las neuronas del SCN parecen secretar un neuropéptido llamado vasopresina en un patrón cíclico.
Otra figura\(\PageIndex{5}\) muestra la ubicación relativa de las diferentes estructuras involucradas en la regulación de los ritmos circadianos.
Los científicos han descubierto ahora que el neurotransmisor GABA excita las células del SCN dorsal pero inhibe las del SCN ventral. Estos efectos opuestos pueden influir en los diferentes tiempos de reacción de estas dos subregiones cuando alguien viaja a través de varias zonas horarias. Este descubrimiento abre así nuevas ideas sobre los mecanismos detrás de los inquietantes síntomas del jet lag.
Los científicos retiraron neuronas de los núcleos supraquiasmáticos de ratas y aislaron estas células en un medio de cultivo in vitro y encontraron que los bucles de retroalimentación dentro de cada una de las células se descargan a frecuencias que varían en ciclos que duran aproximadamente 24 horas. Pero a diferencia de las células nucleares supraquiasmáticas en el cerebro, que sincronizan su actividad con el ciclo día/noche, las células nucleares supraquiasmáticas in vitro no lo hacen. Como cualquier otro reloj, el reloj biológico del cuerpo humano necesita ser reiniciado periódicamente. Para que eso suceda, cada célula de este reloj debe resincronizarse diariamente con señales externas que le digan cuándo comienza y termina el día. Estas señales externas, también conocidas como Zeitgebers (en alemán para “dadores de tiempo”), incluyen la temperatura ambiente, el consumo de comidas, el ruido ambiental y el nivel de actividad del cuerpo. Pero la más fuerte de estas señales es, sin duda, la intensidad general de la luz ambiental.
Reiniciando los relojes internos del cuerpo - Zeitgebers
Células ganglionares sensibles a la luz
Gracias a diversos métodos de etiquetado, los científicos saben ahora que cierta subpoblación de las células ganglionares en la retina humana contienen un pigmento fotosensible y proyectan sus axones directamente en los núcleos supraquiasmáticos así como en otras estructuras cerebrales que se preocupan por la intensidad del ambiente luz.
Estas células ganglionares sensibles a la luz tienen grandes campos receptivos, debido a sus largas dendritas ampliamente dispersas. En estas celdas, la recepción precisa de información sobre la forma, la orientación y el movimiento se sacrifica a la sensibilidad general. Estas células constituyen claramente otro sistema sensible a la luz que corre paralelo al sistema visual pero que se dedica a detectar la intensidad de la luz más que a formar imágenes.
Relojerías moleculares
Muchas funciones humanas, como el estado de alerta, la temperatura corporal y la secreción de ciertas hormonas, funcionan mejor si se ajustan de acuerdo a si es de día o de noche. Por lo tanto, como cabría esperar, un mecanismo ha evolucionado dentro del cuerpo humano para coordinarse sus principales funciones con la hora del día.
El reloj biológico humano es extremadamente regular, aunque no exactamente 24 horas: es preciso dentro del 1%. Pero al igual que un reloj que nunca es absolutamente preciso por sí solo y necesita reiniciarse ocasionalmente, este reloj biológico necesita un mecanismo para evitar que se acumulen pequeños errores en cada celda. Además, necesita sincronizarse con señales externas que le indiquen cuándo comienza cada nuevo día. La creciente intensidad de la luz natural es el primer signo de amanecer, y fotopigmentos especiales en la retina detectan este cambio en la intensidad de la luz y transmiten esta información al reloj biológico humano.
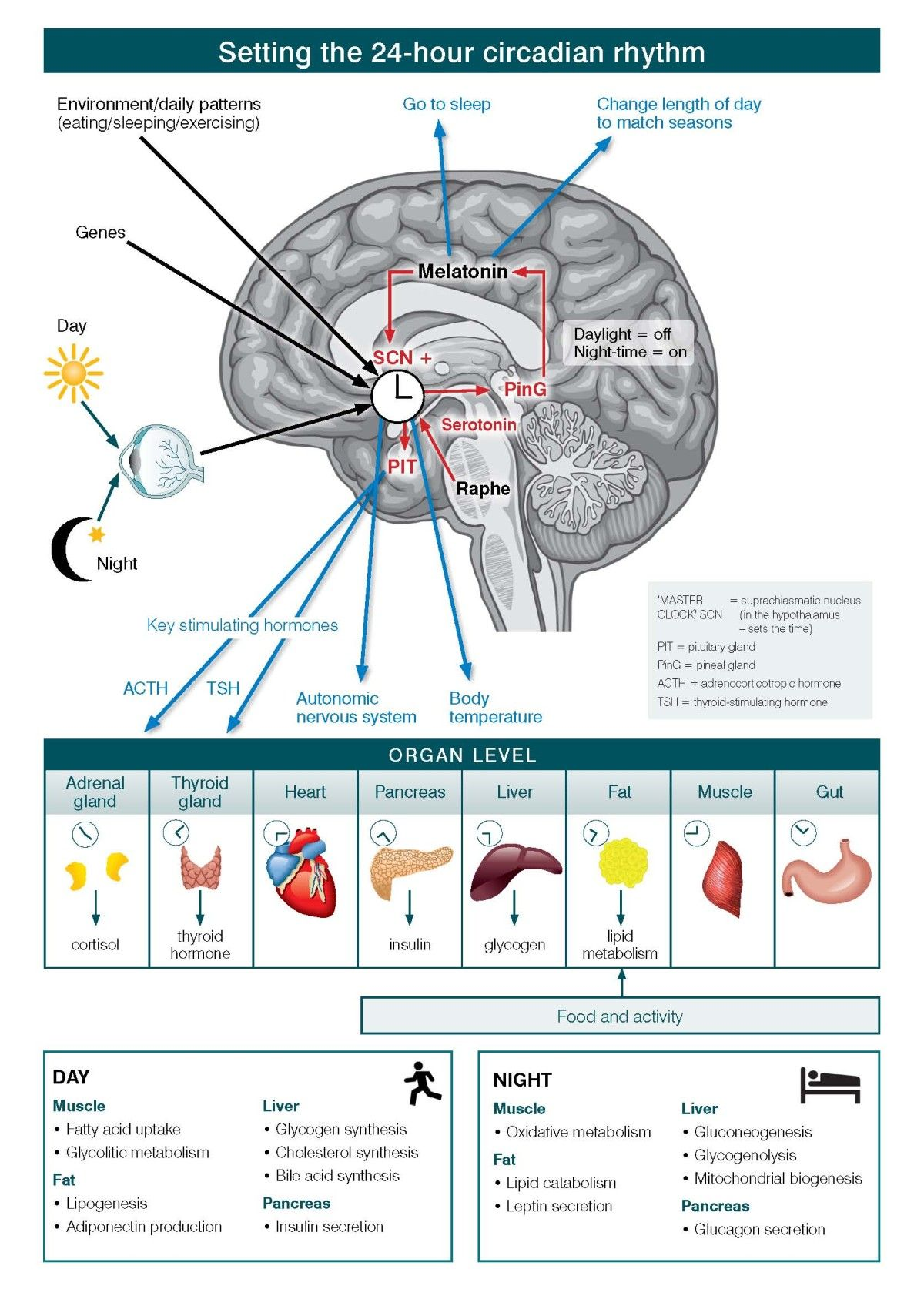
En la Figura\(\PageIndex{7}\) se muestran los niveles de organización de la información y funcionamiento de los sistemas circadianos. Los sistemas circadianos deben considerarse en relación con tres niveles diferentes de organización de la información y operación. Primero está la forma en que el entorno físico comunica (o 'Entradas') la información clave, particularmente relacionada con la diferenciación de la noche del día, al reloj interno 'maestro' (ubicado en el núcleo supraquiasmático (SCN) del cerebro). En segundo lugar están los factores cerebrales 'intrínsecos', que consisten en el reloj maestro y sus sistemas reguladores vinculados (notablemente la secreción de melatonina de la glándula pineal). Estos contribuyen al inicio del sueño, la arquitectura del sueño, los ciclos de sueño-vigilia y otros cambios de comportamiento dependientes del sistema nervioso central (SNC). En tercer lugar, la forma en que el sistema circadiano coordina todos los demás procesos hormonales, metabólicos, inmunes, termorreguladores, nerviosos autonómicos y otros procesos fisiológicos para optimizar las relaciones entre el comportamiento y las funciones corporales (es decir, las 'Salidas').
A nivel celular, casi todas las células individuales y, por lo tanto, los sistemas de órganos tienen sus propios relojes intrínsecos. Como estos relojes celulares (por ejemplo, fibroblastos, células grasas, músculos) y basados en órganos (por ejemplo, hígado, páncreas, intestino) corren a longitudes de período intrínsecamente diferentes, los diferentes sistemas fisiológicos deben alinearse en patrones coherentes. Fundamentalmente, el reloj circadiano maestro permite al organismo alinear los ritmos fisiológicos intrínsecos y conductuales clave de manera óptima con el ciclo externo de luz y oscuridad de 24 horas.
En la figura, las flechas negras desde el ojo (y la luz solar), los genes y los patrones ambientales/diarios (comer/dormir/hacer ejercicio) hasta el SCN indican la entrada recibida por el reloj maestro. Las flechas rojas desde los núcleos del rafe y la glándula pineal (vía melatonina) hasta el SCN, y desde el SCN a la hipófisis indican la modulación intra-CNS de las señales. Las flechas azules desde la melatonina hasta las señales de regulación del sueño, desde el SCN hasta la actividad ANS y la regulación de la temperatura, y la regulación de la hipófisis a la hormona (ACTH y TSH) indican la salida del cerebro controlando otros sistemas de órganos en el cuerpo.
La tabla al final ilustra cómo cambia la función muscular, hepática, grasa y páncreas dependiendo de la hora del día o de la noche. Durante el día, la absorción muscular de ácidos grasos, y aumentar el metabolismo glucolítico. Para las grasas, hay lipogénesis y producción de adiponectina. En el hígado, hay síntesis de glucógeno, colesterol y ácidos biliares. En el páncreas hay secreción de insulina. Por la noche, los músculos se involucran en el metabolismo oxidativo. Las grasas tienen catabolismo lipídico y secreción de leptina. El hígado se involucra en gluconeogénesis, glucogenólisis y biogénesis mitocondrial. El páncreas segrega glucagón.
Otras teorías de por qué dormimos
Como se menciona en la sección * hay muchas funciones del sueño entre ellas la consolidación de la memoria, la conservación de energía, el desarrollo cerebral y la descarga de emociones. Además, la importancia del sueño es evidente en las múltiples ramificaciones negativas de la privación del sueño.
Resumen
En circunstancias normales, existen dos mecanismos principales por los que se regula nuestro sueño: homeostático o recuperativo y circadiano o rítmico. La adenosina parece ser la principal sustancia química subyacente a las funciones homeostáticas/recuperativas del sueño. De hecho, la mayoría de nosotros somos conscientes de cómo nos sentimos cansados después de largos periodos de vigilia. La melatonina y los ritmos de carrera libre del SCN parecen ser la base de los aspectos circadios/rítmicos del sueño. El desfase horario, el trabajo por turnos y la interrupción general de los relojes corporales de las personas durante la pandemia de COVID brindan testimonio de cómo esta teoría también es una base importante del sueño. Ciertamente es claro que los humanos necesitan dormir por diversas razones y que cuando estamos privados de sueño, hay muchas consecuencias para la salud mental y física.
Referencias
Atribuciones
- Moléculas que se acumulan y te hacen dormir - intermedio por Bruno Dubuc bajo licencia Copyleft.
- Moléculas que se acumulan y te hacen dormir - principiante por Bruno Dubuc bajo licencia Copyleft.
- Los núcleos supraquiasmáticos y la glándula pineal - intermedio por Bruno Dubuc bajo licencia Copyleft.
- Células ganglionares sensibles a la luz - avanzadas por Bruno Dubuc bajo licencia Copyleft.
- Comportamiento cíclico de animales por CK-12: Conceptos de Biología licenciados CC BY-NC 4.0
- Nuestro Mecanismos Moleculares - intermedio por Bruno Dubuc bajo licencia Copyleft.
- Nuestro Mecanismos Moleculares - principiante por Bruno Dubuc bajo licencia Copyleft.
- Sueño y sueño por Lumen Boundless Psychology licenciado CC BY-SA
- Imagen sagital del cerebro licenciada CC BY-SA
- Núcleos ligeros, supraquiasmáticos (SCN) y la pinealmelatonina ciruit.jpg por Zhiqiang Ma, Yang Yang, Chongxi Fan, Jing Han, Dongjin Wang, Shouyin Di, Wei Hu, Dong Liu, Xiaofei Li, Russel J. Reiter, y Xiaolong Yan, con licencia CC BY 4.0, vía Wikimedia Commons
- Módulo de Herramientas: Regulación del Sueño y Ritmos Circadianos por Bruno Dubuc bajo licencia Copyleft.
- El reloj circadiano maestro en el brain.jpg humano por Ian B Hickie, Sharon L Naismith, Rébecca Robillard, Elizabeth M Scott, y Daniel F Hermens, con licencia CC BY 3.0, vía Wikimedia Commons


