30.2: Radiactividad
- Page ID
- 127931
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Objetivos de aprendizaje
- Nombrar las principales fuentes de radiación terrestre.
El material radiactivo se encuentra en toda la naturaleza. Las cantidades detectables ocurren naturalmente en el suelo, las rocas, el agua, el aire y la vegetación. De estas fuentes se puede inhalar e ingerir en el cuerpo. Además de esta exposición interna, los humanos también reciben exposición externa de materiales radiactivos que permanecen fuera del cuerpo y de la radiación cósmica del espacio. La dosis natural promedio mundial para humanos es de aproximadamente 2.4 milisieverts (mSv) por año. Esto es cuatro veces más que el promedio mundial de exposición a la radiación artificial, que en el año 2008 ascendió a cerca de 0.6 mSv por año. En algunos países más ricos, como Estados Unidos y Japón, la exposición artificial es, en promedio, mayor que la exposición natural, debido al mayor acceso a imágenes médicas. En Europa, la exposición de fondo natural promedio por país varía de menos de 2 mSv anuales en el Reino Unido a más de 7 mSv anuales en Finlandia, como se muestra en.

Atlas de Radiación Natural de Europa: Gráfico de barras de dosis anuales promedio de fuentes de radiación natural para los principales países europeos
Radiación de fondo natural
La mayor fuente de radiación de fondo natural es el radón aerotransportado, un gas radiactivo que emana del suelo. El radón y sus isótopos, los radionúclidos progenitores y los productos de descomposición contribuyen a una dosis inhalada promedio de 1.26 mSv/a. El radón se distribuye de manera desigual y es variable con el clima, de tal manera que se producen dosis mucho más altas en ciertas áreas del mundo. En estas áreas puede representar un riesgo significativo para la salud. Concentraciones más de 500 veces superiores a la media mundial se han encontrado dentro de edificios en Escandinavia, Estados Unidos, Irán y República Checa. El radón es un producto de desintegración del uranio, que es relativamente común en la corteza terrestre pero más concentrado en rocas que contienen minerales dispersas por todo el mundo. El radón se filtra de estos minerales a la atmósfera o al agua subterránea; también puede infiltrarse en edificios. Se puede inhalar en los pulmones, junto con sus productos de descomposición, donde residirá por un período de tiempo después de la exposición.
Radiación del espacio exterior
Además, la tierra, y todos los seres vivos que hay en ella, son constantemente bombardeados por la radiación del espacio exterior. Esta radiación consiste principalmente en iones cargados positivamente que van desde protones hasta hierro y núcleos más grandes derivados de fuentes fuera de nuestro sistema solar. Esta radiación interactúa con los átomos de la atmósfera para crear una lluvia de aire de radiación secundaria, incluyendo rayos X, muones, protones, partículas alfa, piones, electrones y neutrones. La dosis inmediata de la radiación cósmica proviene principalmente de muones, neutrones y electrones, y esta dosis varía en diferentes partes del mundo según el campo geomagnético y la altitud. Esta radiación es mucho más intensa en la troposfera superior (alrededor de 10 km de altitud) y por lo tanto es de particular preocupación para las tripulaciones de las aerolíneas y los pasajeros frecuentes, que pasan muchas horas al año en este entorno. Por lo general, la tripulación de una aerolínea recibe una dosis extra del orden de 2.2 mSv (220 mrem) por año.
Radiación Terrestre
La radiación terrestre solo incluye fuentes que permanecen externas al cuerpo. Los principales radionucleidos que preocupan son el potasio, el uranio y el torio y sus productos de desintegración. Algunos de estos productos de desintegración, como el radio y el radón, son intensamente radiactivos pero ocurren en bajas concentraciones. La mayoría de estas fuentes han ido disminuyendo, debido a la desintegración radiactiva desde la formación de la tierra, debido a que no existe una fuente significativa de reemplazo. Debido a esto, la actividad actual en la Tierra a partir del uranio-238 es solo la mitad de lo que era originalmente debido a su vida media de 4.5 mil millones de años. El potasio-40 (con una vida media de 1.25 mil millones de años) se encuentra en aproximadamente el ocho por ciento de su actividad original. Sin embargo, los efectos en humanos de la disminución real (debido a la descomposición) de estos isótopos es mínimo. Esto se debe a que los humanos evolucionaron demasiado recientemente para que la diferencia de actividad en una fracción de una vida media sea significativa. Dicho de otra manera, la historia humana es tan corta en comparación con una vida media de mil millones de años que la actividad de estos isótopos de larga vida ha sido efectivamente constante a lo largo de nuestro tiempo en este planeta.
Muchos isótopos de vida media más corta y, por lo tanto, más intensamente radiactivos no se han descompuesto del ambiente terrestre porque todavía se están produciendo. Ejemplos de estos son el radio-226 (un producto de desintegración del uranio-238) y el radón-222 (un producto de desintegración del radio-226).
Detección de Radiación
Un detector de radiación es un dispositivo utilizado para detectar, rastrear o identificar partículas de alta energía.
Objetivos de aprendizaje
- Explicar la diferencia entre los principales tipos de detectores de radiación.
Un detector de radiación es un dispositivo utilizado para detectar, rastrear o identificar partículas de alta energía, como las producidas por la desintegración nuclear, radiación cósmica y reacciones en un acelerador de partículas. Los detectores modernos también se utilizan como calorímetros para medir la energía de la radiación detectada. También se pueden usar para medir otros atributos, como el momento, el giro y la carga de las partículas. Existen diferentes tipos de detectores de radiación; los detectores de ionización gaseosa, los detectores de semiconductores y los detectores de centelleo son los más comunes.

Diferentes Tipos de Detectores de Radiación: diferentes tipos de detectores de radiación (contadores)
Detectores de ionización gaseosa
Los detectores de ionización gaseosa utilizan el efecto ionizante de la radiación sobre sensores llenos de gas. Si una partícula tiene suficiente energía para ionizar un átomo o molécula de gas, los electrones e iones resultantes provocan un flujo de corriente, que se puede medir.
Detectores de semiconductores
Un detector de semiconductores utiliza un semiconductor (generalmente silicio o germanio) para detectar partículas cargadas que atraviesan o la absorción de fotones. Cuando las estructuras sensibles de estos detectores se basan en diodos individuales, se denominan detectores de diodos semiconductores. Cuando contienen muchos diodos con diferentes funciones, se utiliza el término más general “detector de semiconductores”. Los detectores de semiconductores han tenido diversas aplicaciones en las últimas décadas, en particular en espectrometría gamma y de rayos X y como detectores de partículas.
Detectores de centelleo
Un detector de centelleo se crea acoplando un centelleador —un material que exhibe luminiscencia cuando se excita por radiación ionizante— a un sensor de luz electrónico, como un tubo fotomultiplicador (PMT) o un fotodiodo. Los PMT absorben la luz emitida por el centelleador y la vuelven a emitir en forma de electrones a través del efecto fotoeléctrico. La posterior multiplicación de esos electrones (a veces llamados fotoelectrones) da como resultado un pulso eléctrico, que luego puede ser analizado. El pulso produce información significativa sobre la partícula que originalmente golpeó el centelleador.
Los centelleadores son utilizados por el gobierno estadounidense, particularmente Seguridad Nacional, como detectores de radiación. Los centelleadores también se pueden utilizar en experimentos de física de neutrones y partículas de alta energía, exploración de nuevos recursos energéticos, seguridad de rayos X, cámaras nucleares, tomografía computarizada y exploración de gases. Otras aplicaciones de los centelleadores incluyen escáneres CT y cámaras gamma en diagnósticos médicos, pantallas en monitores de computadora y televisores.
Serie de desintegración radiactiva: Introducción
Las series de desintegración radiactiva describen la desintegración de diferentes productos de desintegración radiactiva discreta como una serie encadenada de transformaciones..
Objetivos de aprendizaje
- Describir la importancia de las series de desintegración radiactiva para el proceso
Serie de desintegración radiactiva, o cadenas de desintegración, describir la desintegración radiactiva de diferentes productos de desintegración radiactiva discreta como una serie encadenada de transformaciones. La mayoría de los elementos radiactivos no se descomponen directamente a un estado estable; más bien, sufren una serie de desintegraciones hasta que finalmente se alcanza un isótopo estable.

Diagrama de la serie de desintegración radiactiva: Este diagrama proporciona ejemplos de cuatro series de desintegración: torio (en azul), radio (en rojo), actinio (en verde) y neptunio (en púrpura).
Las etapas de decaimiento son referidas por su relación con etapas anteriores o posteriores. Un isótopo padre es aquel que sufre descomposición para formar un isótopo hijo. El isótopo hijo puede ser estable, o puede desintegrarse para formar un isótopo hijo propio. La hija de un isótopo hija a veces se llama isótopo nieta.
El tiempo que tarda un solo átomo parental en descomponerse en un átomo de su isótopo hijo puede variar ampliamente, no solo para diferentes cadenas padre-hija, sino también para emparejamientos idénticos de isótopos padre e hijo. Mientras que la descomposición de un solo átomo ocurre espontáneamente, la descomposición de una población inicial de átomos idénticos a lo largo del tiempo, tt, sigue una distribución exponencial en descomposición, e−te−t, donde λλse llama la constante de decaimiento. Debido a esta naturaleza exponencial, una de las propiedades de un isótopo es su vida media, tiempo en el que la mitad de un número inicial de radioisótopos parentales idénticos han decaído a sus hijas. Se han determinado vidas medias en laboratorios para miles de radioisótopos (radionúclidos). Estas vidas medias pueden variar desde períodos de tiempo casi inexistentes hasta\(\mathrm{10^{19}}\) años o más.
Las etapas intermedias suelen emitir más radiactividad que el radioisótopo original. Cuando se logra el equilibrio, un isótopo nieta está presente en proporción a su vida media. Pero, dado que su actividad es inversamente proporcional a su vida media, cualquier nucleido en la cadena de desintegración contribuye finalmente tanto como la cabeza de la cadena. Por ejemplo, el uranio natural no es significativamente radiactivo, pero la pitchblende, un mineral de uranio, es 13 veces más radiactivo debido al radio y otros isótopos hijos que contiene. No solo los isótopos de radio inestables son emisores de radiactividad significativos, sino que como siguiente etapa en la cadena de desintegración también generan radón, un gas radiactivo pesado, inerte y natural. La roca que contiene torio y/o uranio (como algunos granitos) emite gas radón, que puede acumularse en lugares cerrados como sótanos o minas subterráneas. La exposición al radón se considera la principal causa de cáncer de pulmón en los no fumadores.
Decaimiento Alfa
En la desintegración alfa un núcleo atómico emite una partícula alfa y se transforma en un átomo con menor masa (por cuatro) y número atómico (por dos).
Objetivos de aprendizaje
- Describir el proceso, el poder de penetración y los efectos de la radiación alfa
La desintegración alfa es un tipo de desintegración radiactiva en la que un núcleo atómico emite una partícula alfa que consta de dos protones y dos neutrones., como se muestra en. Como resultado de este proceso, el átomo padre se transforma (“decae”) en un nuevo átomo con un número másico menor en cuatro y un número atómico menor en dos.
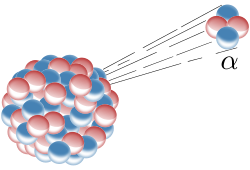
Desintegración alfa: La desintegración alfa es un tipo de desintegración radiactiva. Un núcleo atómico emite una partícula alfa y con ello se transforma (“decae”) en un átomo con un número másico menor en cuatro y un número atómico menor en dos. Muchos otros tipos de descomposición son posibles.
Por ejemplo:\(\mathrm{238U → 234Th + α}\)
Debido a que una partícula alfa es lo mismo que un núcleo de helio-4, que tiene el número de masa 4 y el número atómico 2, esto también se puede escribir como:
\(\mathrm{238}\)
\(\mathrm{92U → 234}\)
\(\mathrm{90Th + 4}\)
\(\mathrm{2He}\)
La partícula alfa también tiene carga +2, pero la carga generalmente no está escrita en ecuaciones nucleares, que describen reacciones nucleares sin considerar los electrones. Esta convención no pretende implicar que los núcleos necesariamente ocurren en átomos neutros.
La desintegración alfa es, con mucho, la forma más común de desintegración de racimos, en la que el átomo padre expulsa una colección hija definida de nucleones, dejando atrás otro producto definido (en la fisión nuclear, se forman varios pares diferentes de hijas de aproximadamente el mismo tamaño). La desintegración alfa es la desintegración de racimos más común debido a la energía de unión extremadamente alta combinada y la masa relativamente pequeña del núcleo del producto de helio-4 (la partícula alfa).
La desintegración alfa generalmente ocurre en los núclidos más pesados. En teoría solo puede ocurrir en núcleos algo más pesados que el níquel (elemento 28), en los que la energía de unión global por nucleón ya no es mínima y los nucleidos son, por lo tanto, inestables hacia procesos espontáneos de tipo fisión. Los emisores alfa más ligeros conocidos son los isótopos más ligeros (números de masa 106-110) de teluro (elemento 52).
Las partículas alfa tienen una energía cinética típica de 5 MeV (aproximadamente 0.13 por ciento de su energía total, es decir, 110 TJ/kg) y una velocidad de 15,000 km/s. Esto corresponde a una velocidad de alrededor de 0.05 c. Hay una variación sorprendentemente pequeña en esta energía, debido a la fuerte dependencia de la vida media de este proceso de la energía producida.
Debido a su masa relativamente grande, +2 carga eléctrica y velocidad relativamente baja, es muy probable que las partículas alfa interactúen con otros átomos y pierdan su energía, por lo que su movimiento hacia adelante se detiene efectivamente a unos pocos centímetros de aire.
La mayor parte del helio producido en la Tierra (aproximadamente el 99 por ciento del mismo) es el resultado de la desintegración alfa de depósitos subterráneos de minerales que contienen uranio o torio. El helio es llevado a la superficie como subproducto de la producción de gas natural.
Decaimiento Beta
La desintegración beta es un tipo de desintegración radiactiva en la que se emite una partícula beta (un electrón o un positrón) desde un núcleo atómico.
Objetivos de aprendizaje
- Explicar la diferencia entre decae beta menos y beta plus.
La desintegración beta es un tipo de desintegración radiactiva en la que una partícula beta (un electrón o un positrón) se emite desde un núcleo atómico, como se muestra en. La desintegración beta es un proceso que permite que el átomo obtenga la proporción óptima de protones y neutrones.

Desintegración Beta: desintegración β en un núcleo atómico (se omite el antineutrino acompañante). La inserción muestra la desintegración beta de un neutrón libre
Hay dos tipos de desintegración beta. Beta menos (β) conduce a una emisión de electrones (e −); beta plus (β+) conduce a una emisión de positrones (e +). En la emisión de electrones también se emite un electrón antineutrino, mientras que la emisión de positrones va acompañada de un neutrino electrónico. La desintegración beta está mediada por la fuerza débil.
Las partículas beta emitidas tienen un espectro continuo de energía cinética, que va desde 0 hasta la máxima energía disponible (Q), que depende de los estados nucleares padre e hijo que participan en la descomposición. Los espectros de energía continua de las partículas beta ocurren porque Q se comparte entre una partícula beta y un neutrino. Una Q típica es de alrededor de 1 MeV, pero puede variar desde unos pocos keV hasta varias decenas de MeV. Dado que la energía de masa en reposo del electrón es de 511 keV, las partículas beta más energéticas son ultrarelativistas, con velocidades muy cercanas a la velocidad de la luz.
Dado que el protón y el neutrón son parte de un núcleo atómico, los procesos de desintegración beta resultan en la transmutación de un elemento químico en otro. Por ejemplo:
\[\mathrm{137Cs → 137Ba + e^-}\]
\[\mathrm{11Na → 10Ne + e^+}\]
La desintegración beta no cambia el número de nucleones, A, en el núcleo; solo cambia su carga, Z. Por lo tanto, se puede introducir el conjunto de todos los nucleidos con la misma A; estos nucleidos isobáricos pueden convertirse entre sí a través de la desintegración beta.
Un núcleo beta-estable puede sufrir otros tipos de desintegración radiactiva (por ejemplo, desintegración alfa). En la naturaleza, la mayoría de los isótopos son beta-estables, pero existen algunas excepciones con vidas medias tan largas que no han tenido tiempo suficiente para descomponerse desde el momento de su nucleosíntesis. Un ejemplo es el nucleido de neutrones impares de protones impares 40 K, que sufre ambos tipos de desintegración beta con una vida media de 1.277 ·10 9 años.
Beta Decay 1/2: En este video presento el Decaimiento Beta y lo discuto desde un nivel básico hasta quizás un nivel universitario de segundo o tercer año.
Beta Decay 2/2: En este video presento el Decaimiento Beta y lo discuto desde un nivel básico hasta un quizás nivel universitario de segundo o tercer año.
Decaimiento Gamma
La desintegración gamma es un proceso de emisión de rayos gamma que acompaña a otras formas de desintegración radiactiva, como la desintegración alfa y beta.
Objetivos de aprendizaje
- Explicar la relación entre la desintegración gamma y otras formas de desintegración nuclear.
La radiación gamma, también conocida como rayos gamma y denotada como γγ, es radiación electromagnética de alta frecuencia y por lo tanto de alta energía. Los rayos gamma suelen tener frecuencias superiores a 10 exahercios (>1019>1019 Hz) y por lo tanto tienen energías superiores a 100 keV y longitudes de onda menores a 10 picometros (menores que el diámetro de un átomo). Sin embargo, esta no es una definición estricta; más bien, es una descripción de regla general para los procesos naturales. Los rayos gamma de la desintegración radiactiva se definen como rayos gamma sin importar cuál sea su energía, por lo que no hay un límite inferior para la energía gamma derivada de la desintegración radiactiva. La desintegración gamma comúnmente produce energías de unos pocos cientos de keV y generalmente menos de 10 MeV.
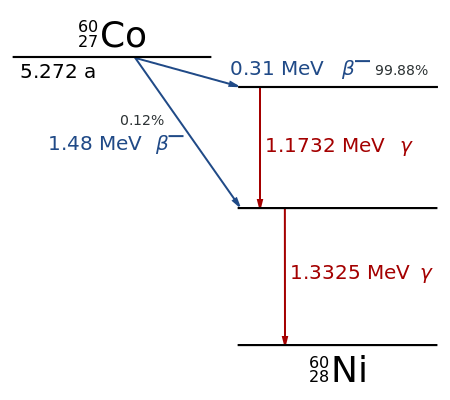
Esquema de Decaimiento Cobalto-60: Ruta de desintegración de Co-60 a Ni-60. Se indican los niveles excitados para Ni-60 que caen al estado fundamental a través de la emisión de rayos gamma
La desintegración gamma acompaña a otras formas de descomposición, como la desintegración alfa y beta; los rayos gamma se producen después de que ocurren los otros tipos de descomposición. Cuando un núcleo emite una partícula α o β, el núcleo hijo generalmente se deja en un estado excitado. Entonces puede pasar a un estado de menor energía emitiendo un rayo gamma, de la misma manera que un electrón atómico puede saltar a un estado de menor energía emitiendo un fotón. Por ejemplo, el cobalto-60 se desintegra en níquel-60 excitado por desintegración beta a través de la emisión de un electrón de 0.31 MeV. A continuación, el níquel-60 excitado desciende al estado fundamental emitiendo dos rayos gamma en sucesión (1.17 MeV, luego 1.33 MeV), como se muestra en. La emisión de un rayo gamma desde un estado nuclear excitado normalmente requiere solo 10−1210−12 segundos: es casi instantánea. La desintegración gamma de los estados excitados también puede seguir reacciones nucleares como la captura de neutrones, la fisión nuclear o la fusión nuclear.
En ciertos casos, el estado nuclear excitado después de la emisión de una partícula beta puede ser más estable que el promedio; en estos casos se denomina estado excitado metaestable si su decaimiento es de 100 a 1000 veces mayor que el promedio de 10−1210−12 segundos. Dichos núcleos tienen vidas medias que son fácilmente medibles; estos se calientan como isómeros nucleares. Algunos isómeros nucleares pueden permanecer en su estado excitado durante minutos, horas o días, u ocasionalmente mucho más tiempo, antes de emitir un rayo gamma. Este fenómeno se llama transición isomérica. Por lo tanto, el proceso de transición isomérica es similar a cualquier emisión gamma; solo difiere en que involucra los estados excitados metaestables intermedios de los núcleos.
Vida media y tasa de descomposición; Datación por carbono-14
La datación por carbono-14 es un método de datación radiométrica que utiliza el radioisótopo carbono-14 (14C) para estimar la edad del objeto.
Objetivos de aprendizaje
- Identificar la edad de los materiales que se pueden determinar aproximadamente utilizando la datación por radiocarbono
Datación por radiocarbono (generalmente referido simplemente como datación por carbono-14) es un método de datación radiométrica. Utiliza el radioisótopo natural carbono-14 (14C) para estimar la edad de los materiales portadores de carbono de hasta aproximadamente 58,000 a 62,000 años de edad.
El carbono tiene dos isótopos estables, no radiactivos: carbono-12 (12C) y carbono-13 (13C). También hay trazas del radioisótopo inestable carbono-14 (14C) en la Tierra. El carbono-14 tiene una vida media relativamente corta de 5,730 años, lo que significa que la fracción de carbono-14 en una muestra se reduce a la mitad en el transcurso de 5,730 años debido a la desintegración radiactiva a nitrógeno-14. El isótopo carbono-14 desaparecería de la atmósfera terrestre en menos de un millón de años si no fuera por la afluencia constante de rayos cósmicos que interactúan con moléculas de nitrógeno (N 2) y átomos individuales de nitrógeno (N) en la estratosfera. Ambos procesos de formación y descomposición del carbono-14 se muestran en.

Formación y desintegración del carbono-14: Diagrama de la formación de carbono-14 (1), la descomposición del carbono-14 (2) y ecuaciones que describen la relación carbono-12:carbono-14 en organismos vivos y muertos
Cuando las plantas fijan dióxido de carbono atmosférico (CO 2) en compuestos orgánicos durante la fotosíntesis, la fracción resultante del isótopo 14C en el tejido vegetal coincidirá con la fracción del isótopo en la atmósfera. Después de que las plantas mueren o son consumidas por otros organismos, se detiene la incorporación de todos los isótopos de carbono, incluido el 14C. Posteriormente, la concentración (fracción) de 14C disminuye a una tasa exponencial fija debido a la desintegración radiactiva de 14C. (Una ecuación que describe este proceso se muestra en.) Comparar la fracción de 14C restante de una muestra con la esperada del 14C atmosférico permite estimar la edad de la muestra.
Las edades de radiocarbono en bruto (es decir, no calibradas) generalmente se reportan en los años de radiocarbono “Antes del presente” (BP), con “presente” definido como CE 1950. Dichas edades en bruto pueden calibrarse para dar fechas de calendario. Uno de los usos más frecuentes de la datación por radiocarbono es estimar la edad de los restos orgánicos de sitios arqueológicos.
La técnica de datación por radiocarbono fue desarrollada por Willard Libby y sus colegas de la Universidad de Chicago en 1949. Emilio Segrè afirmó en su autobiografía que Enrico Fermi le sugirió el concepto a Libby en un seminario en Chicago ese año. Libby estimó que la concentración de radiactividad en estado estacionario del carbono-14 intercambiable sería de aproximadamente 14 desintegraciones por minuto (dpm) por gramo. En 1960, Libby fue galardonada con el Premio Nobel de Química por esta obra. Demostró la precisión de la datación por radiocarbono al estimar con precisión la edad de la madera a partir de una serie de muestras para las que se conocía la edad, incluida una antigua barcaza real egipcia que data de 1850 a. C.
Vida media: Describe la semivida radiactiva y cómo hacer algunos cálculos simples usando la semivida.
Cálculos que implican vida media y tasas de descomposición
La vida media de un radionúclido es el tiempo que toma la mitad de los átomos del radionúclido en desintegrarse.
Objetivos de aprendizaje
- Explicar qué es una vida media de un radionúclido.
La vida media de un radionúclido es el tiempo que toma la mitad de los átomos del radionúclido en desintegrarse. Tomando λλ como la tasa de desintegración (número de desintegraciones por unidad de tiempo), y ττ la vida media de un átomo antes de que se descomponga, tenemos:
\[\mathrm { N } ( \mathrm { t } ) = \mathrm { N } _ { 0 } \mathrm { e } ^ { - \lambda \mathrm { t } } = \mathrm { N } _ { 0 } \mathrm { e } ^ { - \mathrm { t } / \tau }\]
La vida media se relaciona con la constante de decaimiento sustituyendo la condición\(\mathrm { N } = \mathrm { N } _ { \mathrm { o } } / 2\) y resolviendo por\(\mathrm{t = t _ { 1 / 2 }}\):
\[\mathrm { t } _ { 1 / 2 } = \ln 2 / \lambda = \tau \ln 2\]
Una vida media no debe considerarse como el tiempo requerido para que exactamente la mitad de los átomos se descomponen.

Simulación de desintegración radiactiva: Una simulación de muchos átomos idénticos sometidos a desintegración radiactiva, comenzando con cuatro átomos (izquierda) y 400 átomos (derecha). El número en la parte superior indica cuántas vidas medias han transcurrido
La siguiente figura muestra una simulación de muchos átomos idénticos sometidos a desintegración radiactiva. Tenga en cuenta que después de una vida media no quedan exactamente la mitad de los átomos restantes; solo quedan aproximadamente la mitad debido a la variación aleatoria en el proceso. Sin embargo, con más átomos (las cajas de la derecha), la desintegración general es más suave y menos aleatoria que con menos átomos (las casillas de la izquierda), de acuerdo con la ley de los grandes números.
La relación entre la vida media y la constante de desintegración muestra que las sustancias altamente radiactivas se gastan rápidamente mientras que las que irradian débilmente perduran más tiempo. Las vidas medias de los radionucleidos conocidos varían ampliamente, desde más de 10 a 19 años, como para el nucleido muy casi estable 209 Bi, hasta 10 −23 segundos para los altamente inestables.
El factor ln (2) en las ecuaciones anteriores resulta del hecho de que el concepto de “vida media” es simplemente una manera de seleccionar una base diferente a la base natural e para la expresión de por vida. La constante de tiempo τ es la e--1 -vida, el tiempo hasta que solo queda 1/ e —alrededor del 36.8 por ciento, en lugar del 50 por ciento en la vida media de un radionúclido. Por lo tanto, τ es mayor que t 1/2. Se puede demostrar que la siguiente ecuación es válida:
\[\mathrm { N } ( \mathrm { t } ) = \mathrm { N } _ { 0 } \mathrm { e } ^ { - \mathrm { t } / \tau } = \mathrm { N } _ { 0 } 2 ^ { - \mathrm { t } / \mathrm { t } _ { 1 / 2 } }\]
Dado que la desintegración radiactiva es exponencial con una probabilidad constante, cada proceso podría describirse con la misma facilidad con un período de tiempo constante diferente que (por ejemplo) dio su vida 1/3 (cuánto tiempo queda hasta que solo queda 1/3), o su vida 1/10 (cuánto tiempo hasta que solo queda 1/10), y así sucesivamente. Por lo tanto, la elección de τ y t 1/2 para los tiempos de marcador es solo por conveniencia y por el bien de subir convención. Estos tiempos marcadores reflejan un principio fundamental sólo en que muestran que la misma proporción de una sustancia radiactiva dada se desintegrará durante cualquier periodo de tiempo que elijas.
Matemáticamente, la n-ésima vida para la situación anterior se encontraría por el mismo proceso mostrado anteriormente — fijando\(\mathrm { N } = \mathrm { N } _ { 0 } / \mathrm { n }\) y sustituyendo en la solución de decaimiento, para obtener:
\[\mathrm{t _ { 1 / n }} = \dfrac { \ln \mathrm { n } } { \lambda } = \tau \ln \mathrm{n}\]
Vida media: Parte de una serie de videos sobre resolución de problemas físicos. Los problemas están tomados de “La alegría de la física”. Éste trata de la vida media radiactiva. Se exhorta al espectador a pausar el video en la declaración del problema y trabajar el problema antes de ver el resto del video.
Puntos Clave
- La mayor fuente de radiación de fondo natural es el radón aerotransportado, un gas radiactivo que emana del suelo.
- La tierra es constantemente bombardeada por la radiación del espacio exterior que consiste en iones cargados positivamente que van desde protones hasta hierro y núcleos más grandes de fuentes fuera de nuestro sistema solar.
- La radiación terrestre incluye fuentes que permanecen externas al cuerpo. Los principales radionucleidos que preocupan son el potasio, el uranio y el torio y sus productos de desintegración.
- Los detectores de ionización gaseosa utilizan el efecto ionizante de la radiación sobre sensores llenos de gas.
- Un detector de semiconductores utiliza un semiconductor (generalmente silicio o germanio) para detectar partículas cargadas que atraviesan o la absorción de fotones.
- Se crea un detector de centelleo acoplando un centelleador a un sensor de luz electrónico.
- La mayoría de los elementos radiactivos no se descomponen directamente a un estado estable; más bien, sufren una serie de desintegraciones hasta que finalmente se alcanza un isótopo estable.
- Las vidas medias de los radioisótopos varían desde períodos de tiempo casi inexistentes hasta 1019 años o más.
- Las etapas intermedias de las series de desintegración radiactiva a menudo emiten más radiactividad que el radioisótopo original.
- Una partícula alfa es lo mismo que un núcleo de helio-4, que tiene el número de masa 4 y el número atómico 2.
- Debido a su masa relativamente grande, +2 carga eléctrica y velocidad relativamente baja, es muy probable que las partículas alfa interactúen con otros átomos y pierdan su energía, por lo que su movimiento hacia adelante se detiene efectivamente a unos pocos centímetros de aire.
- La mayor parte del helio producido en la Tierra (aproximadamente el 99 por ciento del mismo) es el resultado de la desintegración alfa de depósitos subterráneos de minerales que contienen uranio o torio.
- Hay dos tipos de desintegración beta: beta menos, que conduce a una emisión de electrones, y beta plus, que conduce a una emisión de positrones.
- La desintegración beta permite que el átomo obtenga la proporción óptima de protones y neutrones.
- Los procesos de desintegración beta transmutan un elemento químico en otro.
- La desintegración gamma acompaña a otras formas de descomposición, como la desintegración alfa y beta; los rayos gamma se producen después de que ocurren los otros tipos de descomposición.
- Aunque la emisión de rayos gamma es un proceso casi instantáneo, puede involucrar estados excitados metaestables intermedios de los núcleos.
- Los rayos gamma son generalmente la forma más energética de radiación electromagnética.
- La datación por carbono 14 se puede utilizar para estimar la edad de los materiales que contienen carbono de hasta aproximadamente 58,000 a 62,000 años de antigüedad.
- El isótopo carbono-14 desaparecería de la atmósfera terrestre en menos de un millón de años si no fuera por la afluencia constante de rayos cósmicos que interactúan con el nitrógeno atmosférico.
- Uno de los usos más frecuentes de la datación por radiocarbono es estimar la edad de los restos orgánicos de sitios arqueológicos.
- La vida media se relaciona con la constante de decaimiento de la siguiente manera:\(\mathrm { t } _ { 1 / 2 } = \ln 2 / \lambda\).
- La relación entre la vida media y la constante de desintegración muestra que las sustancias altamente radiactivas se gastan rápidamente mientras que las que irradian débilmente perduran más tiempo.
- Las vidas medias de los radionucleidos conocidos varían ampliamente, desde más de 10 a 19 años, como para el nucleido muy casi estable 209 Bi, hasta 10 -23 segundos para los altamente inestables.
Términos Clave
- radionúclido: Un radionúclido es un átomo con un núcleo inestable, caracterizado por el exceso de energía disponible para ser impartida ya sea a una partícula de radiación recién creada dentro del núcleo o a través de conversión interna.
- radón: un elemento químico radiactivo (símbolo Rn, anteriormente Ro) con número atómico 86; uno de los gases nobles
- sievert: en el Sistema Internacional de Unidades, la unidad derivada de dosis de radiación; la dosis recibida en una hora a una distancia de 1 cm de una fuente puntual de 1 mg de radio en un recinto de platino de 0.5 mm de espesor; símbolo: Sv
- centelleador: cualquier sustancia que brille bajo la acción de fotones u otras partículas de alta energía
- diodo: un dispositivo electrónico que permite que la corriente fluya en una sola dirección; una válvula
- semiconductor: Sustancia con propiedades eléctricas intermedias entre un buen conductor y un buen aislante.
- vida media: el tiempo requerido para que la mitad de los núcleos de una muestra de un isótopo específico sufran desintegración radiactiva
- radioisótopo: un isótopo radiactivo de un elemento
- decaimiento: cambiar sometiéndose a fisión, emitiendo radiación o capturando o perdiendo uno o más electrones
- partícula alfa: Núcleo cargado positivamente de un átomo de helio-4 (compuesto por dos protones y dos neutrones), emitido como consecuencia de la radiactividad; α-partícula.
- desintegración radiactiva: cualquiera de varios procesos por los cuales los núcleos inestables emiten partículas subatómicas y/o radiación ionizante y se desintegran en uno o más núcleos más pequeños
- desintegración beta: una reacción nuclear en la que se emite una partícula beta (electrón o positrón)
- positrón: El equivalente de antimateria de un electrón, que tiene la misma masa pero una carga positiva.
- transmutación: la transformación de un elemento en otro por una reacción nuclear
- radiación electromagnética: radiación (cuantificada como fotones) que consiste en campos eléctricos y magnéticos oscilantes orientados perpendicularmente entre sí, moviéndose por el espacio
- rayos gamma: Una radiación electromagnética de muy alta frecuencia (y por lo tanto de muy alta energía) emitida como consecuencia de la radiactividad.
- datación radiométrica: La datación radiométrica es una técnica utilizada para fechar objetos basada en una comparación entre la abundancia observada de un isótopo radiactivo natural y sus productos de desintegración utilizando tasas de desintegración conocidas..
- carbono-14: carbono-14 es un isótopo radiactivo de carbono con un núcleo que contiene 6 protones y 8 neutrones.
- radionúclido: Un radionúclido es un átomo con un núcleo inestable, caracterizado por el exceso de energía disponible para ser impartida ya sea a una partícula de radiación recién creada dentro del núcleo o a través de conversión interna.
LICENCIAS Y ATRIBUCIONES
CONTENIDO CON LICENCIA CC, COMPARTIDO PREVIAMENTE
- Curación y Revisión. Proporcionado por: Boundless.com. Licencia: CC BY-SA: Atribución-CompartirIgual
CC CONTENIDO LICENCIADO, ATRIBUCIÓN ESPECÍFICA
- Radiactividad natural. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Natural_Radioactivity. Licencia: CC BY-SA: Atribución-CompartirIgual
- radón. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/radon. Licencia: CC BY-SA: Atribución-CompartirIgual
- radionúclido. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Radionúclido. Licencia: CC BY-SA: Atribución-CompartirIgual
- sievert. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/sievert. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Detector de ionización gaseosa. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Gaseoso... ation_detector. Licencia: CC BY-SA: Atribución-CompartirIgual
- Detector de centelleo. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Detector de centelleo. Licencia: CC BY-SA: Atribución-CompartirIgual
- Detector de semiconductores. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Semiconductor_detector. Licencia: CC BY-SA: Atribución-CompartirIgual
- Detector de radiación. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Detector de Radiación. Licencia: CC BY-SA: Atribución-CompartirIgual
- centelleo. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/centelleador. Licencia: CC BY-SA: Atribución-CompartirIgual
- diodo. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/diode. Licencia: CC BY-SA: Atribución-CompartirIgual
- semiconductores. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/semiconductor. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _summary_3.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Serie de desintegración radiactiva. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Radioactive_Decay_Series. Licencia: CC BY-SA: Atribución-CompartirIgual
- decaimiento. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/decay. Licencia: CC BY-SA: Atribución-CompartirIgual
- vida media. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/vida media. Licencia: CC BY-SA: Atribución-CompartirIgual
- radioisótopo. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/radioisótopo. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _summary_3.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... iagram.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- partícula alfa. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/alpha_particle. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento alfa. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Alpha_decay. Licencia: CC BY-SA: Atribución-CompartirIgual
- desintegración radiactiva. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/radioactive_decay. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _summary_3.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... iagram.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento beta. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Beta_decay. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento beta. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Beta_decay. Licencia: CC BY-SA: Atribución-CompartirIgual
- transmutación. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/transmutación. Licencia: CC BY-SA: Atribución-CompartirIgual
- positrón. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/positron. Licencia: CC BY-SA: Atribución-CompartirIgual
- decaimiento beta. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/beta_decay. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _summary_3.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... iagram.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 2/2. Ubicado en: http://www.youtube.com/watch?v=r2Q6xdsGYfE. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 1/2. Ubicado en: http://www.youtube.com/watch?v=4Et47PE288U. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Desintegración gamma. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Gamma_d... ray_production. Licencia: CC BY-SA: Atribución-CompartirIgual
- rayos gamma. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/gamma_ray. Licencia: CC BY-SA: Atribución-CompartirIgual
- radiación electromagnética. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/electr... etic_radiation. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _summary_3.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... iagram.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 2/2. Ubicado en: http://www.youtube.com/watch?v=r2Q6xdsGYfE. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 1/2. Ubicado en: http://www.youtube.com/watch?v=4Et47PE288U. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... esquema.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Carbono-14. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Carbon-14. Licencia: CC BY-SA: Atribución-CompartirIgual
- Datación por radiocarbono. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Radiocarbon_dating. Licencia: CC BY-SA: Atribución-CompartirIgual
- datación radiométrica. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Radiometric%20Citas. Licencia: CC BY-SA: Atribución-CompartirIgual
- radioisótopo. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/radioisótopo. Licencia: CC BY-SA: Atribución-CompartirIgual
- carbono-14. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Carbon-14. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _summary_3.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... iagram.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 2/2. Ubicado en: http://www.youtube.com/watch?v=r2Q6xdsGYfE. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 1/2. Ubicado en: http://www.youtube.com/watch?v=4Et47PE288U. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... esquema.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Vida media. Ubicado en: http://www.youtube.com/watch?v=4UPmy_XofMo. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Desintegración radiactiva. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Radioac... Ay%23Vida media. Licencia: CC BY-SA: Atribución-CompartirIgual
- Tasa de decaimiento. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Decay_rate. Licencia: CC BY-SA: Atribución-CompartirIgual
- Vida media. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Vida media. Licencia: CC BY-SA: Atribución-CompartirIgual
- vida media. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/vida media. Licencia: CC BY-SA: Atribución-CompartirIgual
- radionúclido. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Radionúclido. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _of_Europe.jpg. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: Upload.wikimedia.org/wikipedia/commons/thumb/c/c0/detectors_summary_3.png/800px-detectors_summary_3.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: Upload.wikimedia.org/wikipedia/commons/thumb/6/62/Radioactive_Decay_Chains_Diagram.svg/800px-Radioactive_Decay_Chains_Diagram.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: Upload.wikimedia.org/wikipedia/commons/thumb/7/79/alpha_decay.svg/250px-alpha_decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 2/2. Ubicado en: http://www.youtube.com/watch?v=r2Q6xdsGYfE. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _Decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Decaimiento Beta 1/2. Ubicado en: http://www.youtube.com/watch?v=4Et47PE288U. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... esquema.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikimedia. Ubicado en: upload.wikimedia.org/wikipedi... _decay.svg.png. Licencia: CC BY-SA: Atribución-CompartirIgual
- Vida media. Ubicado en: http://www.youtube.com/watch?v=4UPmy_XofMo. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube
- Vida media. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Vida media. Licencia: Dominio Público: No Conocido Copyright
- Vida media. Ubicado en: http://www.youtube.com/watch?v=zYNpxqkRYlM. Licencia: Dominio público: Sin derechos de autor conocidos. Términos de licencia: Licencia estándar de YouTube

