21.3: La desintegración radiactiva
- Page ID
- 1980
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Habilidades para desarrollar
- Reconocer los modos comunes de la desintegración radiactiva
- Identificar las partículas y las energías comunes involucradas en las reacciones de desintegración nuclear
- Escribir y equilibrar las ecuaciones de desintegración nuclear
- Calcular los parámetros cinéticos para los procesos de descomposición, incluida la vida media
- Describir las técnicas comunes de la datación radiométrica
Después del descubrimiento fortuito de la radiactividad por Becquerel, muchos científicos destacados comenzaron a investigar este nuevo e interesante fenómeno. Entre ellos se encontraban Marie Curie (la primera mujer en ganar un Premio Nobel y la única persona en ganar dos Premios Nobel en diferentes ciencias: química y física), quien fue la primera en acuñar la palabra "radiactividad", y Ernest Rutherford (famoso por el experimento de la lámina de oro), que investigó y nombró tres de los tipos más comunes de radiación. Durante el comienzo del siglo XX, se descubrieron muchas sustancias radiactivas, se investigaron y cuantificaron las propiedades de la radiación y se desarrolló una sólida comprensión de la radiación y la desintegración nuclear.
El cambio espontáneo de un nucleido inestable a otro es la desintegración radiactiva. El nucleido inestable se llama el nucleido padre; el núclido que resulta de la desintegración se llama el núclido hijo. El nucleido hijo puede ser estable o se puede descomponer. La radiación producida durante la desintegración radiactiva es tal que el núclido hijo se encuentra más cerca de la banda de estabilidad que el núclido padre, por eso la ubicación de un núclido en relación con la banda de estabilidad puede servir como una guía para el tipo de desintegración que experimentara (Figura \(\PageIndex{1}\)).
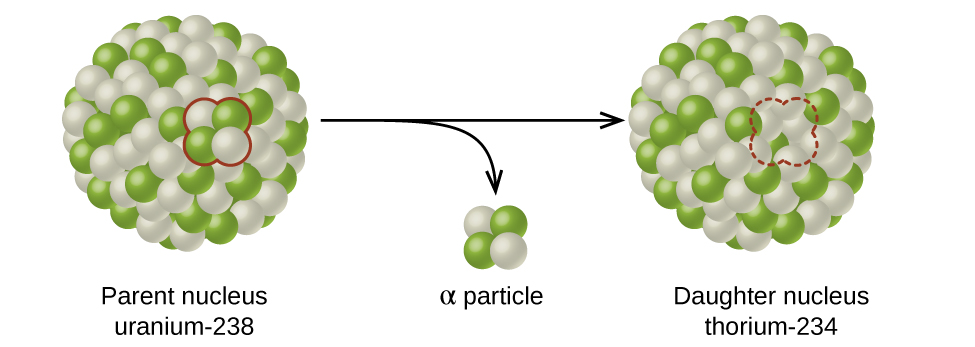
Figura \(\PageIndex{1}\): Un núcleo de uranio-238 (el nucleido padre) pasa por desintegración α para formar torio-234 (el nucleido hijo). La partícula alfa elimina dos protones (verde) y dos neutrones (gris) del núcleo de uranio-238.
Aunque la desintegración radiactiva de un núcleo es demasiado pequeña para verla a simple vista, podemos ver indirectamente la desintegración radiactiva en un entorno llamado la cámara de niebla. Haga clic aquí para obtener más información sobre las cámaras de nubes y para ver una demostración interesante de la cámara de nubes dentro del laboratorio de Jefferson.
Vídeo \(\PageIndex{1}\): ¡Cómo construir una cámara de nubes!
Los tipos de desintegración radiactiva
Los experimentos de Ernest Rutherford que involucran la interacción de la radiación con un campo magnético o eléctrico (Figura \(\PageIndex{2}\)) le ayudaron a determinar que un tipo de radiación consistía en partículas α cargadas positivamente y relativamente masivas; un segundo tipo estaba formado por partículas β cargadas negativamente y mucho menos masivas; y un tercero eran ondas electromagnéticas sin carga, rayos γ. Ahora sabemos que las partículas α son núcleos de helio de alta energía, las partículas β son electrones de alta energía y la radiación γ componen la radiación electromagnética de alta energía. Clasificamos diferentes tipos de desintegración radiactiva por la radiación producida.
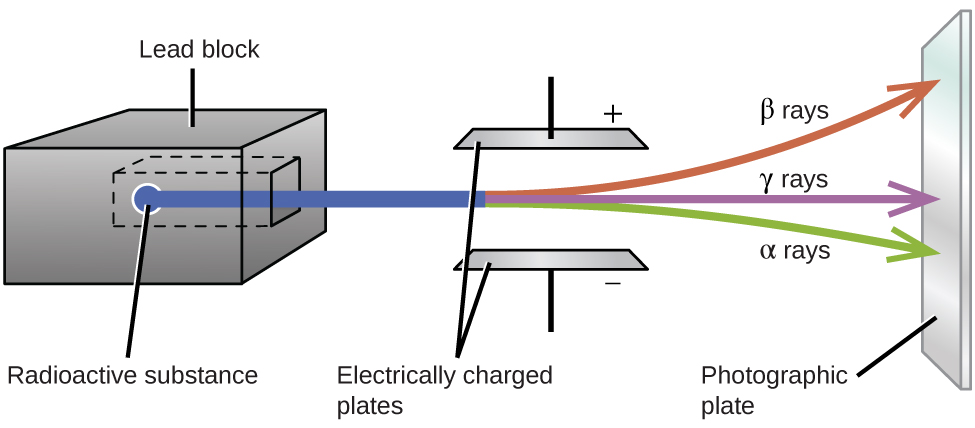
Figura \(\PageIndex{2}\): Las partículas alfa, que son atraídas por la placa negativa y desviadas en una cantidad relativamente pequeña, deben tener carga positiva y ser relativamente masivas. Las partículas beta, que son atraídas por la placa positiva y desviadas en una cantidad relativamente grande, deben tener carga negativa y ser relativamente ligeras. Los rayos gamma, que no se ven afectados por el campo eléctrico, deben estar descargados.
La desintegración alfa (α) es la emisión de una partícula α del núcleo. Por ejemplo, el polonio-210 pasar una desintegración α:
\[\ce{^{210}_{84}Po⟶ ^4_2He + ^{206}_{82}Pb} \hspace{40px}\ce{or}\hspace{40px} \ce{^{210}_{84}Po ⟶ ^4_2α + ^{206}_{82}Pb}\]
La desintegración alfa ocurre principalmente en los núcleos pesados (A> 200, Z> 83). Debido a que la pérdida de una partícula α produce un nucleido hijo con un número de masa cuatro unidades más pequeño y un número atómico dos unidades más pequeño que los del nucleido padre, el nucleido hijo tiene una relación n: p mayor que el nucleido padre. Si el nucleido padre que sufre la desintegración α se encuentra por debajo de la banda de estabilidad, el nucleido hijo estará más cerca de la banda.
La desintegración beta (β) es la emisión de un electrón de un núcleo. El yodo-131 es un ejemplo de un nucleido que pasa por la desintegración β:
\[\ce{^{131}_{53}I ⟶ ^0_{-1}e + ^{131}_{54}X} \hspace{40px}\ce{or}\hspace{40px} \ce{^{131}_{53}I ⟶ ^0_{-1}β + ^{131}_{54}Xe}\]
La desintegración beta, que se puede considerar como la conversión de un neutrón en un protón y una partícula β, se observa en los nucleidos con una gran proporción n:p. La partícula beta (electrón) emitida proviene del núcleo atómico y no es uno de los electrones que rodean el núcleo. Dichos núcleos se encuentran por encima de la banda de estabilidad. La emisión de un electrón no cambia el número de masa del nucleido, pero aumenta el número de sus protones y disminuye el número de sus neutrones. En consecuencia, la relación n: p disminuye y el nucleido hijo se encuentra más cerca de la banda de estabilidad que el nucleido padre.
La emisión gamma (emisión γ) se observa cuando un nucleido se forma en un estado excitado y luego decae a su estado fundamental con la emisión de un rayo γ, un cuanto de radiación electromagnética de alta energía. La presencia de un núcleo en un estado excitado a veces se indica con un asterisco (*). El cobalto-60 emite radiación γ y se usa en muchas aplicaciones, incluido el tratamiento del cáncer:
\[\mathrm{^{60}_{27}Co^* ⟶\, ^0_0γ +\, ^{60}_{27}Co}\]
No hay cambio en el número de masa o número atómico durante la emisión de un rayo γ aunque la emisión γ acompañe a uno de los otros modos de desintegración.
La emisión de los positrones (desintegración β+) es la emisión de un positrón desde el núcleo. El oxígeno 15 es un ejemplo de un nucleido que pasa por la emisión de los positrones:
\[\ce{^{15}_8O ⟶ ^0_{+1}e + ^{15}_7N} \hspace{40px}\ce{or}\hspace{40px} \ce{^{15}_8O ⟶ ^0_{+1}β + ^{15}_7N}\]
La emisión de los positrones se observa para los nucleidos en los que la relación n:p es baja. Estos nucleidos se encuentran por debajo de la banda de estabilidad. La desintegración de los positrones es la conversión de un protón en un neutrón con la emisión de un positrón. La relación n:p aumenta y el nucleido hijo se encuentra más cerca de la banda de estabilidad que el nucleido padre.
La captura de los electrones ocurre cuando uno de los electrones internos de un átomo es capturado por el núcleo del átomo. Por ejemplo, el potasio-40 pasa por la captura de sus electrones:
\[\ce{^{40}_{19}K + ^0_{-1}e ⟶ ^{40}_{18}Ar}\]
La captura de los electrones ocurre cuando un electrón de capa interna se combina con un protón y se convierte en un neutrón. La pérdida de un electrón de capa interna deja una vacante que será ocupada por uno de los electrones externos. Cuando el electrón externo cae en la vacante, emitirá energía. En la mayoría de los casos, la energía emitida será en forma de rayos X. Al igual que en la emisión de los positrones, la captura de los electrones ocurre para los núcleos "ricos en protones" que se encuentran por debajo de la banda de estabilidad. La captura de los electrones tiene el mismo efecto en el núcleo que la emisión de los positrones: el número atómico se reduce en uno y el número de masa no cambia. Esto aumenta la relación n:p, y el nucleido hijo se encuentra más cerca de la banda de estabilidad que el nucleido padre. Es difícil predecir si ocurrirá la captura de los electrones o la emisión de los positrones. Esta elección se debe principalmente a los factores cinéticos, siendo el que requiere la menor energía de activación el que tiene más probabilidades de ocurrir. La figura \(\PageIndex{3}\) resume estos tipos de desintegración, junto con sus ecuaciones y cambios en los números atómicos y de masa.
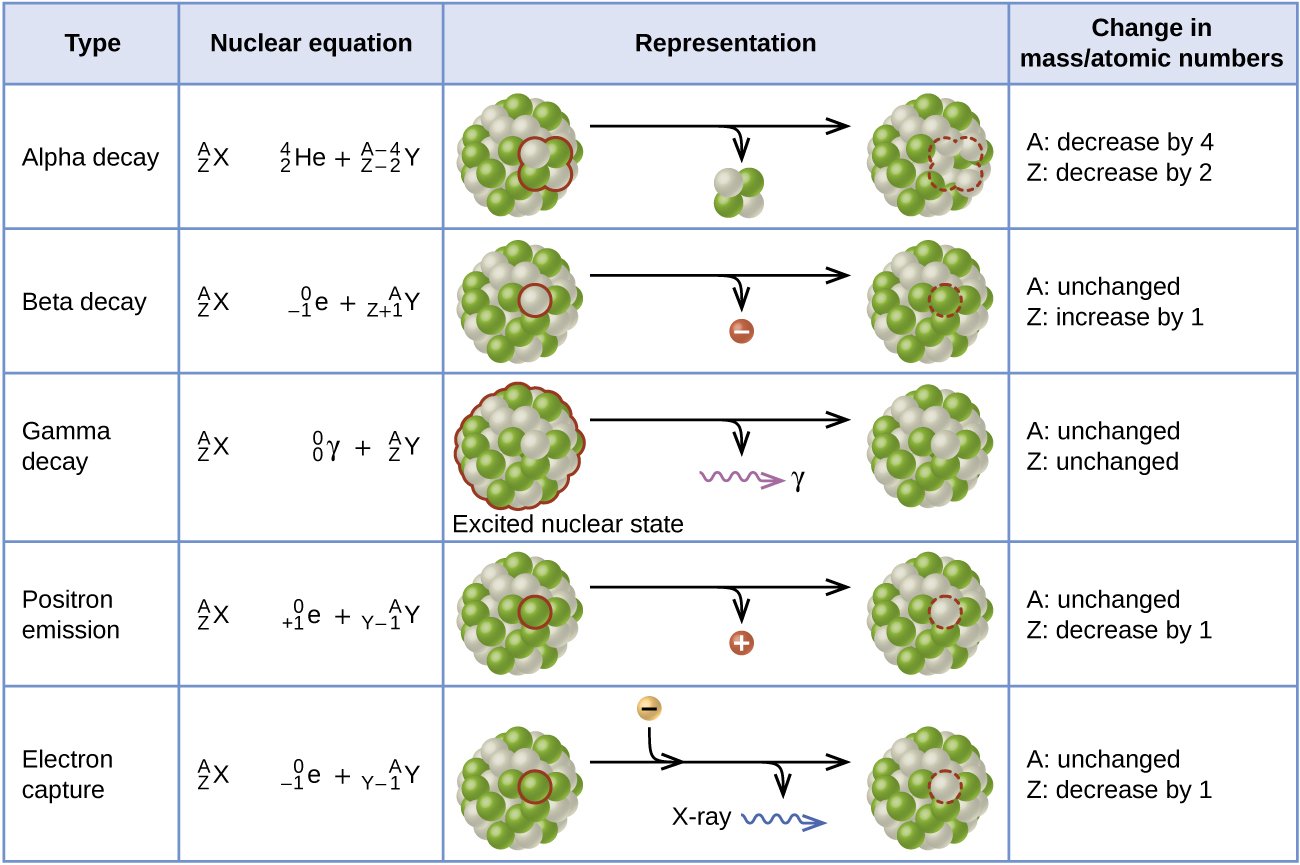
Figura\(\PageIndex{3}\): Esta tabla resume el tipo, la ecuación nuclear, la representación y cualquier cambio en la masa o los números atómicos de varios tipos de desintegración.
El escaneo de TEP
La tomografía por emisión de positrones (TEP) usa la radiación para diagnosticar y rastrear las condiciones de salud y monitorear los tratamientos médicos revelando cómo funcionan las partes del cuerpo de un paciente (Figura \(\PageIndex{4}\)). Para ejecutar una tomografía por emisión de positrones, se produce un radioisótopo emisor de positrones en un ciclotrón y luego se une a una sustancia que usa la parte del cuerpo que se está investigando. Este compuesto "marcado", o radiotrazador, se coloca en el paciente (se inyecta por vía intravenosa o se inhala como un gas), y la forma en que el tejido lo usa revela cómo funciona ese órgano u otra área del cuerpo.
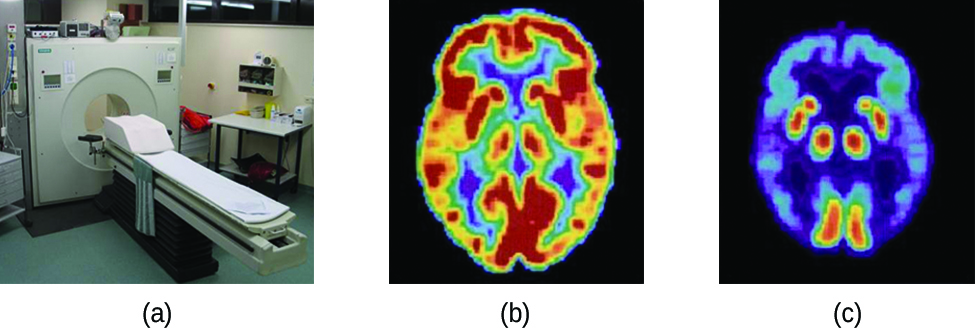
Figura \(\PageIndex{4}\): Un escáner TEP (a) usa la radiación para producir una imagen que muestra cómo funciona parte del cuerpo de un paciente. Los escaneos que produce se pueden usar para obtener imágenes de un cerebro sano (b) o se pueden usar para diagnosticar afecciones médicas como la enfermedad de Alzheimer (c). (crédito a: modificación del trabajo de Jens Maus) </
Por ejemplo, F-18 se produce por bombardeo de los protones de 18O \((\ce{^{18}_8O+^1_1p⟶^{18}_9F+^1_0n})\) y se incorpora en un análogo de glucosa llamado fludesoxiglucosa (FDG). La forma en que el cuerpo usa la FDG proporciona información de diagnóstico crítica; por ejemplo, la FDG puede revelar canceres porque los cánceres usan la glucosa de manera diferente a los tejidos normales. El 18F emite positrones que interactúan con los electrones cercanos, produciendo una explosión de radiación gamma. El escáner detecta esta energía y la convierte en una imagen en color tridimensional detallada que muestra cómo funciona esa parte del cuerpo del paciente. Los diferentes niveles de radiación gamma producen diferentes cantidades de brillo y colores en la imagen, que luego pueden ser interpretados por un radiólogo para revelar lo que está sucediendo. Las tomografías por emisión de positrones pueden detectar daño y enfermedades cardíacos, ayudar a diagnosticar la enfermedad de Alzheimer, indicar la parte del cerebro afectada por la epilepsia, revelar el cáncer, mostrar en qué etapa se encuentra y cuánto se ha propagado, y si los tratamientos son efectivos. A diferencia de las imágenes de resonancia magnética y los rayos X, que solo muestran cómo se ve algo, la gran ventaja de los escaneos TEP es que muestran cómo funciona algo. Las tomografías por emisión de positrones ahora se realizan generalmente junto con una tomografía computarizada.
Las series de desintegración radiactiva
Los isótopos radiactivos naturales de los elementos más pesados caen en cadenas de desintegraciones sucesivas o desintegraciones, y todas las especies de una cadena constituyen una familia radiactiva o serie de desintegraciones radiactivas. Tres de estas series incluyen la mayoría de los elementos radiactivos naturales de la tabla periódica. Son la serie del uranio, la serie de los actínidos y la serie del torio. La serie del neptunio es una cuarta serie, que ya no es significativa en la tierra debido a la corta vida media de las especies involucradas. Cada serie se caracteriza por un padre (primer miembro) que tiene una vida media larga y una serie de nucleidos hijos que forman un producto final estable, es decir, un nucleido en la banda de estabilidad (Figura \(\PageIndex{5}\)). En las tres series, el producto final es un isótopo estable de plomo. La serie del neptunio, que antes se pensaba que terminaba con bismuto-209, termina con talio-205.
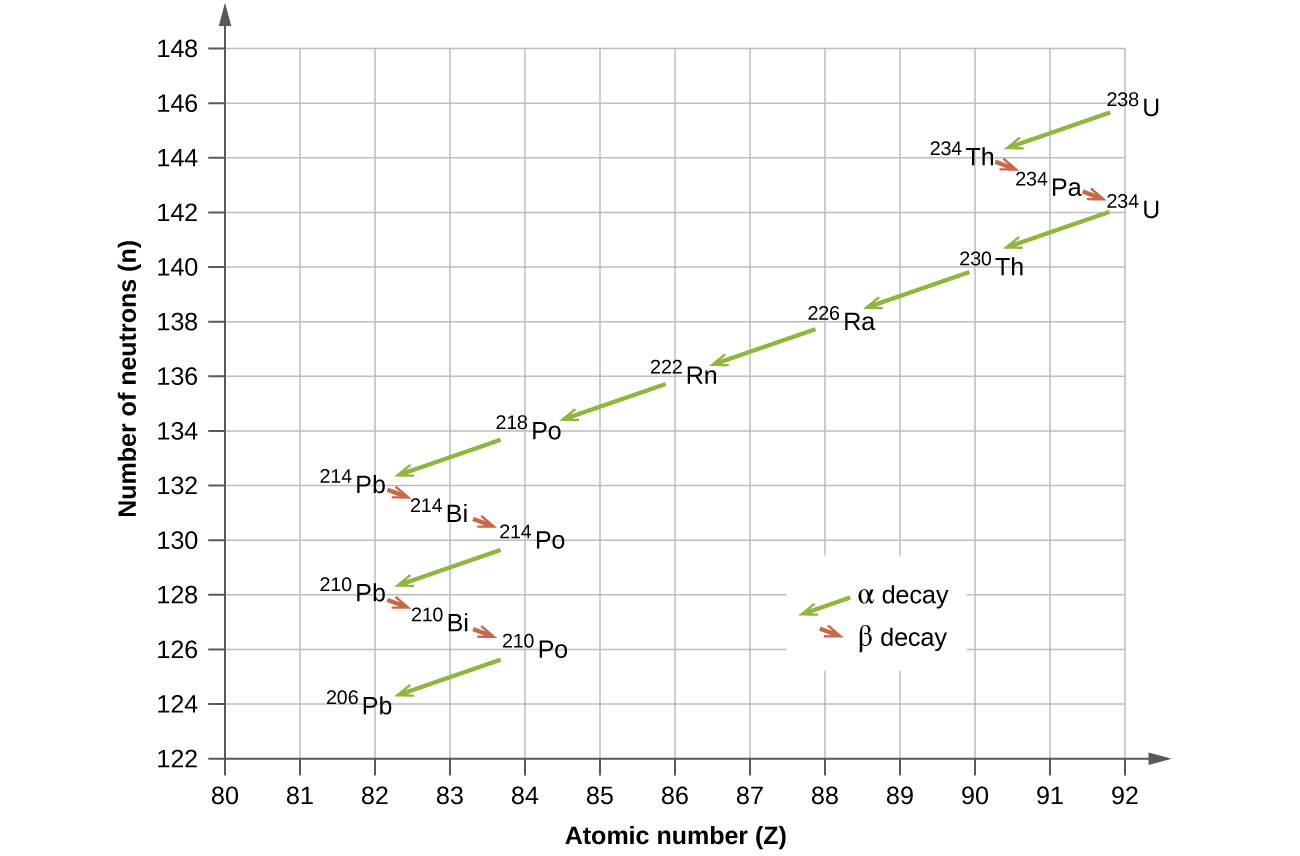
Figura \(\PageIndex{5}\): El uranio-238 pasa por una serie de desintegraciones radiactiva que consiste en 14 pasos separados antes de producir el plomo-206 estable. Esta serie consiste en ocho desintegraciones α y seis desintegraciones β.
Las medias vidas radiactivas
La desintegración radiactiva sigue una cinética de primer orden. Ya que las reacciones de primer orden se han discutido en detalle en el capítulo de la cinética, ahora aplicaremos esos conceptos a las reacciones de desintegración nuclear. Cada nucleido radiactivo tiene una vida media característica y constante (t1/2), el tiempo necesario para que la mitad de los átomos de una muestra decaiga. La vida media de un isótopo nos permite determinar cuánto tiempo estará disponible una muestra de un isótopo útil y cuánto tiempo se debe almacenar una muestra de un isótopo indeseable o peligroso antes de que se descomponga a un nivel de radiación suficientemente bajo que ya no es un problema.
Por ejemplo, el cobalto-60, un isótopo que emite rayos gamma que se usa para tratar el cáncer, tiene una vida media de 5.27 años (Figura \(\PageIndex{6}\)). En una fuente de cobalto-60, dado que la mitad de los núcleos \(\ce{^{60}_{27}Co}\) se desintegran cada 5.27 años, tanto la cantidad de la material como la intensidad de la radiación emitida se reducen en la mitad cada 5.27 años. (Tenga en cuenta que, para una sustancia dada, la intensidad de la radiación que produce es directamente proporcional a la velocidad de la desintegración de la sustancia y la cantidad de la sustancia). Esto se espera para un proceso que sigue una cinética de primer orden. Por lo tanto, una fuente de cobalto-60 que se usa para el tratamiento del cáncer se debe reemplazar con regularidad para que siga siendo eficaz.
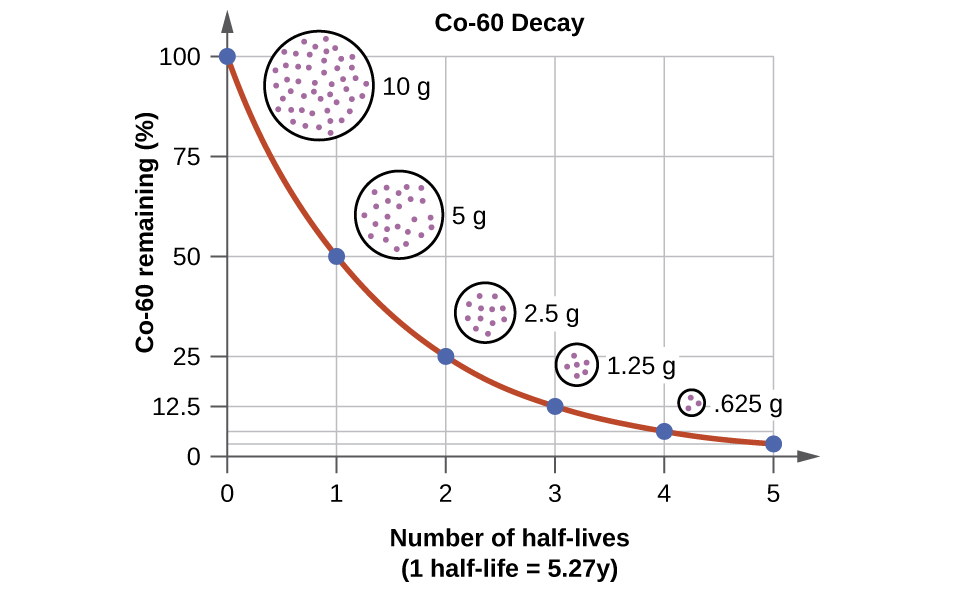
Figura \(\PageIndex{6}\): Para el cobalto-60, que tiene una vida media de 5.27 años, el 50% permanece después de 5.27 años (una vida media), el 25% permanece después de 10.54 años (dos vidas medias), el 12.5% permanece después de 15.81 años (tres vidas medias), y así sucesivamente.
Dado que la desintegración nuclear sigue una cinética de primer orden, podemos adaptar las relaciones matemáticas usadas para las reacciones químicas de primer orden. Generalmente sustituimos la concentración por el número de núcleos, N. Si la tasa se expresa en desintegraciones nucleares por segundo, nos referiremos a ella como la actividad de la muestra radiactiva. La tasa de desintegración radiactiva es:
\[\text{decay rate} = \lambda N\]
con \(\lambda\) siendo la constante de desintegración del radioisótopo particular.
La constante de desintegración, \(\lambda\), que es la misma que una constante de velocidad discutida en el capítulo de cinética. Es posible expresar la constante de desintegración en términos de la vida media, t1/2:
\[λ=\dfrac{\ln 2}{t_{1/2}}=\dfrac{0.693}{t_{1/2}} \hspace{40px}\ce{or}\hspace{40px} t_{1/2}=\dfrac{\ln 2}{λ}=\dfrac{0.693}{λ}\]
Las ecuaciones de primer orden que relacionan la cantidad, N y el tiempo son:
\[N_t=N_0e^{−kt} \hspace{40px}\ce{or}\hspace{40px} t=−\dfrac{1}{λ}\ln\left(\dfrac{N_t}{N_0}\right)\]
donde N0 es el número inicial de núcleos o moles del isótopo, y Nt es el número de núcleos o moles que quedan en el tiempo t. El ejemplo \(\PageIndex{1}\) aplica estos cálculos para encontrar las tasas de desintegración radiactiva de los nucleidos específicos.
Ejemplo \(\PageIndex{1}\): Las tasas de desintegración radiactiva
\(\ce{^{60}_{27}Co}\) decae con una vida media de 5.27 años para producir \(\ce{^{60}_{28}Ni}\).
a. ¿Cuál es la constante de desintegración de la desintegración radiactiva del cobalto-60?
b. Calcule la fracción de una muestra del isótopo \(\ce{^{60}_{27}Co}\) que permanecerá después de 15 años.
c. ¿Cuánto tiempo tarda una muestra de \(\ce{^{60}_{27}Co}\) en desintegrarse hasta el punto de que sólo queda el 2.0% de la cantidad original?
Solución
(a) El valor de la constante de velocidad se da por:
\[λ=\dfrac{\ln 2}{t_{1/2}}=\mathrm{\dfrac{0.693}{5.27\:y}=0.132\:y^{−1}}\]
(b) La fracción de \(\ce{^{60}_{27}Co}\) que queda después del tiempo t se da por \(\dfrac{N_t}{N0}\). Reordenando la relación de primer orden Nt = N0e– λt para resolver esta relación resulta en:
\[\dfrac{N_t}{N_0}=e^{-λt}=e^\mathrm{-(0.132/y)(15.0/y)}=0.138\]
La fracción de \(\ce{^{60}_{27}Co}\) que permanecerá después de 15.0 años es 0.138. O dicho de otra manera, el 13.8% del \(\ce{^{60}_{27}Co}\) \) originalmente presente permanecerá después de 15 años.
(c) 2.00% de la cantidad original de \(\ce{^{60}_{27}Co}\) es igual a 0.0200 × N0. Sustituyendo esto en la ecuación del tiempo para la cinética de primer orden nos da:
\[t=−\dfrac{1}{λ}\ln\left(\dfrac{N_t}{N_0}\right)=−\dfrac{1}{0.132\:\ce y^{−1}}\ln\left(\dfrac{0.0200×N_0}{N_0}\right)=29.6\:\ce y\]
Ejercicio \(\PageIndex{1}\)
El radón-222, \(\ce{^{222}_{86}Rn}\), tiene una vida media de 3.823 días. ¿Cuánto tiempo tardará una muestra de radón-222 con una masa de 0.750 g en descomponerse en otros elementos, dejando solo 0.100 g de radón-222?
- Respuesta
-
11.1 dias
Debido a que cada nucleido tiene un número específico de nucleones, un equilibrio particular de repulsión y atracción, y su propio grado de estabilidad, la vida media de los nucleones radiactivos varía extensamente. Por ejemplo: la vida media de \(\ce{^{209}_{83}Bi}\) es 1.9 × 1019 años; \(\ce{^{239}_{94}Ra}\) es 24.000 años; \(\ce{^{222}_{86}Rn}\) es 3.82 días; y el elemento 111 (Rg para roentgenium) es de 1.5 × 10–3 segundos. La vida media de varios isótopos radiactivos importantes para la medicina se muestra en la Tabla \(\PageIndex{1}\), y otros se enumeran en el Apéndice N1.
| Tipo | Modo de decaimiento | Vida Media | Usos |
|---|---|---|---|
| F-18 | desintegración β+ | 110. minutos | escaneos TEP |
| Co-60 | desintegración β, desintegración γ | 5.27 años | tratamiento para el cáncer |
| Tc-99m1 | desintegración γ | 8.01 horas | escaneos de cerebro, pulmón, corazón, y hueso |
| I-131 | desintegración β | 8.02 dias | escaneos y tratamiento de la tiroides |
| Tl-201 | captura de los electrones | 73 horas | escaneos del corazón y las arterias; prueba de esfuerzo cardiaco |
| La "m" en Tc-99m significa "metaestable", lo que indica que este es un estado inestable y de alta energía del Tc-99. Los isótopos metaestables emiten la radiación \(γ\) para deshacerse del exceso de energía y hacerse (más) estables. | |||
La datación radiométrica
Varios radioisótopos tienen vidas medias y otras propiedades que los hacen útiles para "fechar" el origen de estos objetos como artefactos arqueológicos, organismos anteriormente vivos o formaciones geológicas. Este proceso es la datación radiométrica y se ha usado para muchos descubrimientos científicos revolucionarios sobre la historia geológica de la tierra, la evolución de la vida y la historia de la civilización humana. Exploraremos algunos de los tipos más comunes de datación radiactiva y cómo funcionan los isótopos particulares para cada tipo.
La datación radiactiva usando el carbono 14
La radiactividad del carbono-14 proporciona un método para fechar los objetos que formaban parte de un organismo vivo. Este método de datación radiométrica, que también se llama la datación por radiocarbono o datación por carbono 14, es preciso para la datación de sustancias que contienen carbono que tienen una antigüedad de hasta aproximadamente 30,000 años y puede proporcionar fechas razonablemente precisas hasta un máximo de aproximadamente 50,000 años.
El carbono natural consiste en tres isótopos: \(\ce{^{12}_6C}\), que constituye aproximadamente el 99% del carbono de la tierra; \(\ce{^{13} 6C}\), aproximadamente el 1% del total; y trazas de \(\ce{^{14}_6C}\). El carbono 14 se forma en la atmósfera superior por la reacción de los átomos de nitrógeno con los neutrones de los rayos cósmicos en el espacio:
\[\ce{^{14}_7N + ^1_0n⟶ ^{14}_6C + ^1_1H}\]
Todos los isótopos de carbono reaccionan con el oxígeno para producir las moléculas de CO2. La relación de \(\ce{^{14} 6CO2}\) a \(\ce{^{12}_6CO2}\) depende de la relación de \(\ce{^{14}_6CO}\) a \(\ce{^{12}_6CO}\) en la atmósfera. La abundancia natural de \(\ce{^{14}_6CO}\) en la atmósfera es de aproximadamente 1 parte por billón; hasta hace poco, esto ha sido constante en el tiempo, como se ve en las muestras de gas que estan atrapadas en el hielo. La incorporación de \(\ce{^{14}_6C^{14}_6CO2}\) y \(\ce{^{12}_6CO2}\) en las plantas es una parte regular del proceso de fotosíntesis, lo que significa que la relación \(\ce{^{14}_6C:^{12}_6C} \) encontrada en una planta viva es la misma que la relación \(\ce{^{14}_6C:^{12}_6C}\) en la atmósfera. Pero cuando la planta muere, ya no atrapa el carbono usando la fotosíntesis. Debido a que \(\ce{^{12}_6C}\) es un isótopo estable y no pasa por la desintegración radiactiva, su concentración en la planta no cambia. Sin embargo, el carbono 14 se desintegra por emisión β con una vida media de 5730 años:
\[\ce{^{14}_6C⟶ ^{14}_7N + ^0_{-1}e}\]
Por lo tanto, la relación \(\ce{^{14}_6C:^{12}_6C}\) disminuye gradualmente después de que la planta muere. La disminución de la relación con el tiempo proporciona una medida del tiempo transcurrido desde la muerte de la planta (u otro organismo que se comió la planta). La figura \(\PageIndex{7}\) representa este proceso visualmente.
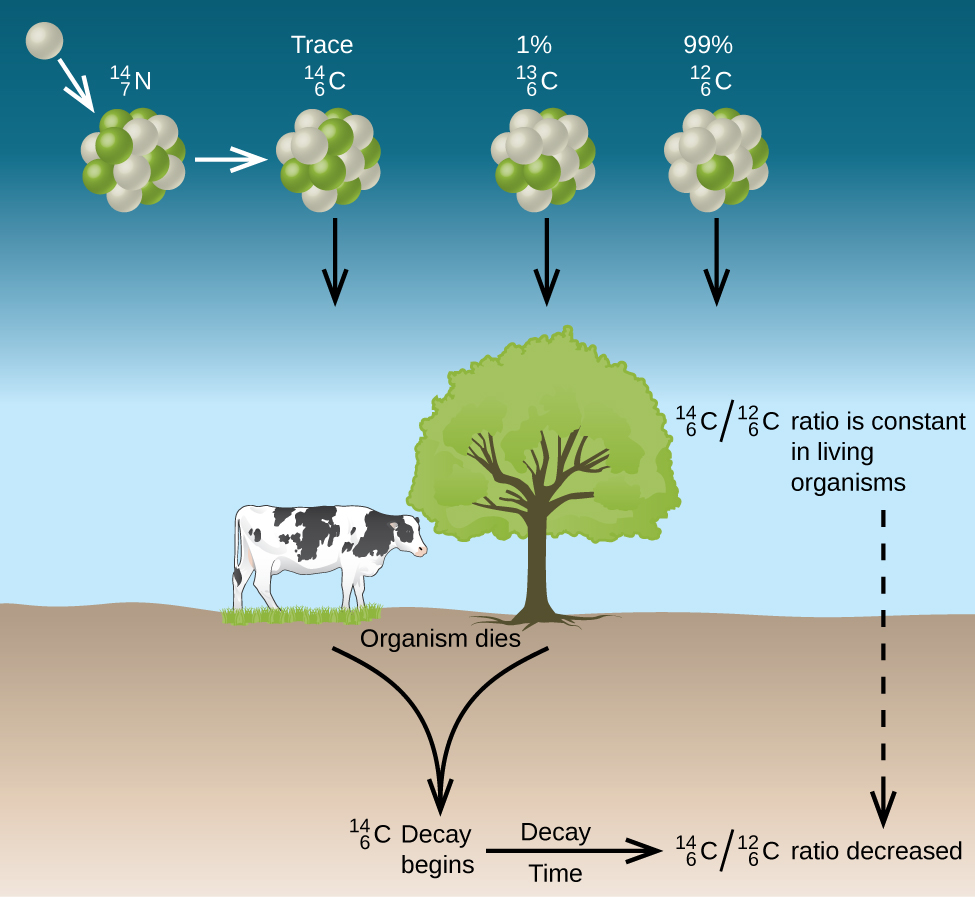
Figura\(\PageIndex{7}\): Junto con el carbono 12 estable, el carbono 14 radiactivo se absorbe por las plantas y los animales, y permanece en un nivel constante dentro de ellos mientras están vivos. Después de la muerte, el C-14 decae y la proporción de C-14:C-12 en los restos disminuye. La comparación de esta proporción con la proporción C-14:C-12 en los organismos vivos nos permite determinar cuánto tiempo hace que el organismo vivió (y murió).
Por ejemplo, con una vida media de \(\ce{^{14}_6C}\) siendo 5730 años, si la relación \(\ce{^{14}_6C:^{12}_6C}\) en un objeto de madera encontrado en una excavación arqueológica es la mitad de lo que es en un árbol vivo, esto indica que el objeto de madera tiene 5730 años. Se pueden obtener determinaciones altamente precisas de las relaciones \(\ce{^{14}_6C:^{12}_6C} \) a partir de muestras muy pequeñas (tan pequeñas como un miligramo) mediante el uso de un espectrómetro de masas.
Ejemplo \(\PageIndex{2}\): La datación por radiocarbono
Un pequeño trozo de papel (producido a partir de la materia vegetal que antes vivía) tomado de los Rollos del Mar Muerto tiene una actividad de 10.8 desintegraciones por minuto por gramo de carbono. Si la actividad inicial de C-14 fue de 13.6 desintegraciones/min/g de C, calcule la edad de los Rollos del Mar Muerto.
Solución
La tasa de desintegración (número de desintegraciones/minuto/gramo de carbono) es proporcional a la cantidad de C-14 radiactivo que queda en el papel, por eso podemos sustituir las tasas por las cantidades, N, en la relación:
\[t=−\dfrac{1}{λ}\ln\left(\dfrac{N_t}{N_0}\right)⟶t=−\dfrac{1}{λ}\ln\left(\dfrac{\ce{Rate}_t}{\ce{Rate}_0}\right)\]
donde el subíndice 0 representa el momento en que se cortaron las plantas para hacer el papel, y el subíndice t representa el momento actual.
La constante de desintegración se puede determinar usando la vida media de C-14, 5730 años:
\[λ=\dfrac{\ln 2}{t_{1/2}}=\mathrm{\dfrac{0.693}{5730\: y}=1.21×10^{−4}\:y^{−1}}\]
Sustituyendo y resolviendo, tenemos:
Por lo tanto, los Rollos del Mar Muerto tienen aproximadamente 1900 años (Figura \(\PageIndex{8}\)).

Figura \(\PageIndex{8}\): La datación por carbono 14 ha demostrado que estas páginas de los Rollos del Mar Muerto fueron escritas o copiadas en papel hecho de plantas que murieron entre el 100 a.C. y el 50 d.C.
Ejercicio \(\PageIndex{2}\)
Recientemente se han determinado fechas más precisas de los reinados de los antiguos faraones egipcios usando las plantas que se conservaron en sus tumbas. Las muestras de semillas y materia vegetal de la tumba del rey Tutankamón tienen una tasa de desintegración de C-14 de 9.07 desintegraciones/min/g de C. ¿Cuánto tiempo hace que el reinado del rey Tut llegó a su fin?
- Respuesta
-
hace unos 3350 años, o aproximadamente 1340 a.C.
Ha habido algunos cambios significativos y bien documentados en la proporción \(\ce{^{14}_6C : ^{12}_6C}\). La precisión de una aplicación sencilla de esta técnica depende de que la proporción \(\ce{^{14}_6C:^{12}_6C}\) en una planta viva sea igual ahora que en una era anterior, pero esto no siempre es válido. Debido a la creciente acumulación de moléculas de CO2 (en gran parte \(\ce{^{12}_6CO2}\)) en la atmósfera causada por la combustión de los combustibles fósiles (en la que esencialmente todos los \(\ce{^ {14}_6C}\) han decaído), la proporción de \(\ce{^{14}_6C:^{12}_6C}\) en la atmósfera se puede cambiar. Este aumento artificial en \(\ce{^{12}_6CO2}\) en la atmósfera hace que la proporción \(\ce{^{14}_6C:^{12}_6C}\) disminuya, y esto a su vez afecta la proporción en los organismos que viven en la tierra corrientemente. Sin embargo, afortunadamente, podemos usar otros datos, como la datación de los árboles examinando los anillos de crecimiento anual, para calcular los factores de corrección. Con estos factores de corrección, se pueden determinar las fechas precisas. En general, la datación radiactiva solo funciona durante aproximadamente 10 vidas medias; por tanto, el límite para la datación por carbono 14 es de aproximadamente 57,000 años.
La datación radiactiva usando los nucleidos distintos que el carbono-14
La datación radiactiva también puede usar otros nucleidos radiactivos con vidas medias más largas para fechar eventos más antiguos. Por ejemplo, el uranio-238 (que forma el plomo-206 después de una serie de pasos) se puede usar para establecer la edad de las rocas (y la edad aproximada de las rocas más antiguas de la tierra). Dado que el U-238 tiene una vida media de 4.5 mil millones de años, la mitad del U-238 original tarda esa cantidad de tiempo en desintegrarse en Pb-206. En una muestra de roca que no contiene cantidades apreciables de Pb-208, el isótopo de plomo más abundante, podemos asumir que el plomo no estaba presente cuando se formó la roca. Por eso, midiendo y analizando la relación de U-238: Pb-206, podemos determinar la edad de la roca. Esto supone que todo el plomo 206 presente proviene de la desintegración del uranio 238. Si hay plomo 206 adicional presente, lo que se indica por la presencia de otros isótopos de plomo en la muestra, se necesita hacer un ajuste. La datación por potasio-argón usa un método similar. K-40 se desintegra por emisión de positrones y captura de electrones para formar Ar-40 con una vida media de 1.25 mil millones de años. Si se tritura una muestra de roca y se mide la cantidad de gas Ar-40 que escapa, la determinación de la relación Ar-40: K-40 nos da la edad de la roca. Otros métodos, como la datación con rubidio-estroncio (el Rb-87 se desintegra en Sr-87 con una vida media de 48.8 mil millones de años), funcionan usando el mismo principio. Para estimar el límite inferior de la edad de la tierra, los científicos determinan la edad de varias rocas y minerales, asumiendo que la tierra es más antigua que las rocas y minerales más antiguos de su corteza. A partir de 2014, las rocas más antiguas conocidas en la tierra son los zircones de Jack Hills de Australia, que según la datación de uranio y plomo tienen casi 4.4 mil millones de años.
Ejemplo \(\PageIndex{3}\): La datación radiactiva de las rocas
Una roca ígnea contiene 9.58 × 10–5 g de U-238 y 2.51× 10–5 g de PB-206 y cantidades mucho más pequeñas de Pb-208. Determine la fecha aproximada de formación de la roca.
Solución
La muestra de la roca contiene muy poco Pb-208, el isotopo más común del plomo, por eso podemos asumir que todo el Pb-206 en la roca fue producido por la desintegración radiactiva del U-238. Cuando se formó la roca, contenía todo el U-238 que se encontraba actualmente en ella, además de algo de U-238 que desde entonces ha pasado por una desintegración radiactiva.
La cantidad de U-238 en la roca actualmente es:
Porque cuando un mol de U-238 se desintegra, produce un mol de Pb-206, la cantidad de U-238 que ha pasado por desintegración radiactiva desde que se formó la roca es:
The total amount of U-238 originally present in the rock is therefore:
\[\mathrm{4.03×10^{−7}\:mol+1.22×10^{−7}\:mol=5.25×10^{−7}\:mol\: U}\]El tiempo que ha pasado desde que se formo la roca se da por:
\[t=−\dfrac{1}{λ}\ln\left(\dfrac{N_t}{N_0}\right)\]donde N0 representa la cantidad original de U-238 y Nt representa la cantidad actual de U-238.
El U-238 se desintegra en Pb-206 con una vida media de 4.5 × 109 años, por eso la constante de desintegración λ es:
Sustituyendo y resolviendo nos da:
Por lo tanto, la roca tiene aproximadamente 1.7 mil millones de años.
Ejercicio \(\PageIndex{3}\)
Una muestra de roca contiene 6.14 × 10–4 g de Rb-87 y 3.51 × 10–5 g de Sr-87. Calcule la edad de la roca. (La vida media de la desintegración β de Rb-87 es 4.7 × 1010 años).
- Respuesta
-
3.7 × 109 años
Resumen
Los núcleos que tienen proporciones n:p inestables pasan por una desintegración radiactiva espontánea. Los tipos más comunes de radiactividad son la desintegración α, la desintegración β, la emisión γ, la emisión de positrones y la captura de los electrones. A veces, las reacciones nucleares también involucran rayos γ, y algunos núcleos se desintegran por la captura de los electrones. Cada uno de estos modos de desintegración causa la formación de un nuevo núcleo con una relación n:p más estable. Algunas sustancias pasan por una serie de desintegraciones radiactivas, pasando por múltiples desintegraciones antes de formar en un isótopo estable. Todos los procesos de desintegración nuclear siguen una cinética de primer orden, y cada radioisótopo tiene su propia vida media característica, el tiempo que se requiere para que la mitad de sus átomos se desintegran. Debido a las grandes diferencias de estabilidad entre los nucleidos, existe una extensa gama de semividas de las sustancias radiactivas. Muchas de estas sustancias se usan en el diagnóstico y el tratamiento médico, determinando la edad de los objetos arqueológicos y geológicos, y más.
Ecuaciones Clave
- tasa de descomposición = λN
- \(t_{1/2}=\dfrac{\ln 2}{λ}=\dfrac{0.693}{λ}\)
Glosario
- desintegración alfa (α)
- pérdida de una partícula alfa durante la desintegración radiactiva
- desintegración beta (β)
- descomposición de un neutrón en un protón, que permanece en el núcleo, y un electrón, que se emite como una partícula beta
- nucleido hijo
- nucleido producido por la desintegración radiactiva de otro nucleido; puede ser estable o puede desintegrarse aún más
- captura de los electrones
- combinación de un electrón del núcleo con un protón para producir un neutrón dentro del núcleo
- emisión gamma (γ)
- desintegración de un nucleido en estado excitado acompañado de la emisión de un rayo gamma
- vida media (t1/2)
- tiempo necesario para que la mitad de los átomos de una muestra radiactiva se desintegran
- nucleido padre
- nucleido inestable que cambia espontáneamente a otro nucleido (hijo)
- emisión de positrones
- (también, desintegración β+) conversión de un protón en un neutrón, que permanece en el núcleo, y un positrón, que se emite
- desintegración radioactiva
- descomposición espontánea de un nucleido inestable en otro nucleido
- serie de desintegración radiactiva
- cadenas de desintegraciones sucesivas (desintegraciones radiactivas) que finalmente forman un producto final estable
- datación por radiocarbono
- métodos muy precisos para fechar los objetos de entre 30,000 y 50,000 años de antigüedad que se derivaron de la materia que estaba viva en algún tiempo; esto se logra al calcular la proporción de \(\ce{^{14}_6C:^{12}_6C}\) en el objeto versus la proporción de \(\ce{^{14}_6C:^{12}_6C}\) en la atmósfera actual
- datación radiométrica
- uso de radioisótopos y sus propiedades para fechar la formación de los objetos tales como artefactos arqueológicos, organismos anteriormente vivos o formaciones geológicas
Contribuyentes y atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


