16.2: La Tercera Ley de la Termodinámica
- Page ID
- 127676
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
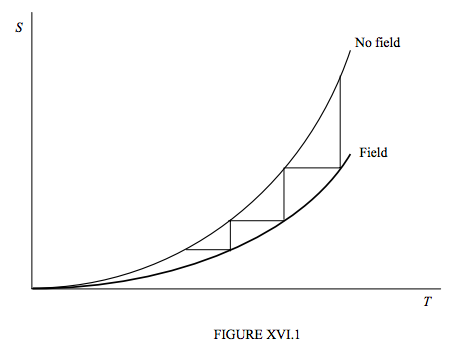
El teorema del calor de Nernst y la extensión de Planck del mismo, aunque originalmente se derivaban de observar el comportamiento de las reacciones químicas en sólidos y líquidos, ahora se cree que se aplican de manera bastante general a cualquier proceso y, en vista de ello, es hora de reconsiderar nuestra descripción de la desmagnetización adiabática. Vemos inmediatamente que la figura XV.1 necesita ser redibujada para reflejar el hecho de que la entropía de la sustancia se aproxima a cero, esté o no situada en un campo magnético. El dibujo revisado se muestra como la figura XVI.1, en la que he dibujado tres operaciones consecutivas de magnetización-desmagnetización, y se verá fácilmente que nunca alcanzaremos una temperatura de exactamente cero en un número finito de operaciones.
Lo mismo se aplica a cualquier operación en la que intentemos bajar la temperatura mediante una serie de restricciones isotérmicas que disminuyen la entropía seguida de relajaciones adiabáticas, ya sea que estemos comprimiendo un gas isotérmicamente y luego descomprimiéndolo adiabáticamente, o estirando una banda de goma isotérmicamente y aflojándolo adiabáticamente. En todos los casos, debido a la convergencia de las dos curvas de entropía a temperatura cero, se nos lleva a concluir:
Es imposible reducir la temperatura de un cuerpo material al cero absoluto de temperatura en un número finito de operaciones.
Esta es la Tercera Ley de la Termodinámica, y es una consecuencia inevitable de la extensión de Planck del Teorema del Calor de Nernst.
Esto suele tomarse para significar que es imposible nunca reducir la temperatura de cualquier cosa a cero absoluto. Desde un punto de vista práctico, eso puede ser cierto, aunque eso no es estrictamente lo que dice la tercera ley. Dice que es imposible hacerlo en un número finito de operaciones. No puedo evitar pensar en una pelota que rebota (ver Mecánica Clásica Capítulo V), en la que la pelota rebota un número infinito de veces antes de finalmente llegar a descansar después de un tiempo finito. Después de cada rebote, todavía hay un número infinito de rebotes por venir, sin embargo, todo ha terminado en un tiempo finito. Ahora bien, tal vez algún lector de estas notas algún día ideará un método para realizar un número infinito de operaciones de estrés isotérmico/relajación adiabática en un tiempo finito, y así alcanzar el cero absoluto.
La tercera ley también habla de un número finito de operaciones —por lo que supongo que se entiende operaciones como una restricción reductora de la entropía seguida de una relajación adiabática. No estoy seguro en qué medida esto se aplica a procesos como el enfriamiento por láser. En tales experimentos se dirige un rayo láser opuesto a un haz atómico. La frecuencia del láser es exactamente igual a la frecuencia necesaria para excitar los átomos a su nivel más bajo excitado, y así detiene a los átomos en sus pistas. A medida que los átomos disminuyen la velocidad, se puede cambiar la frecuencia requerida para permitir el efecto Doppler. Tales experimentos han reducido la temperatura a una fracción de una nanocelvina. Estos experimentos no parecen ser del tipo de experimento que teníamos en mente al desarrollar la tercera ley de la termodinámica. Bien podríamos preguntarnos si es conceptualmente posible o imposible reducir las velocidades de una colección de átomos a cero durante un período de tiempo finito. Podríamos argumentar que es conceptualmente posible —pero entonces podemos recordar que los átomos se atraen entre sí (fuerzas de van der Waals), así que, si todos los átomos están instantáneamente en reposo, no permanecerán así. Por supuesto si tuviéramos un gas ideal (como un gas real extrapolado a presión cero!) de tal manera que no hay fuerzas entre las moléculas, el concepto de temperatura cero implica que todos los átomos son estacionarios —es decir, cada uno tiene una posición definida y un impulso cero. Esto es, según el principio de incertidumbre de Heisenberg, inconcebible. Entonces lo dejo abierto como tema para las conversaciones a la hora del almuerzo exactamente cuán estrictamente la tercera ley nos impide alcanzar nunca el cero absoluto de la temperatura.
Ejercicio. Si la temperatura cinética de un conjunto de átomos de hidrógeno se reduce a una décima parte de una nanocelvina, ¿cuál es la velocidad de raíz cuadrática media de los átomos?


