2.1: Introducción
- Page ID
- 89286
Los suelos no existen simplemente en el paisaje, sino que crecen, se desarrollan, erosionan y se transforman lentamente en otros suelos a través del tiempo, un grupo de procesos conocidos colectivamente como pedogénesis. La pedogénesis comienza con el material parental, el material a partir del cual se forman los suelos. Aunque una pequeña minoría de suelos se desarrollan en depósitos orgánicos, la mayoría de los derivados de materiales parentales inorgánicos actuaron sobre ellos por adiciones, pérdidas, translocaciones y transformaciones
Un tipo importante de transformación es la meteorización de los materiales geológicos parentales. Todos los suelos minerales se desarrollan a partir de las rocas y minerales de la corteza terrestre. A través de la intemperie, los minerales y las rocas se desintegran físicamente en tamaños de partícula más pequeños y se descomponen químicamente en productos químicos y mineralógicos alterados. Sin embargo, el material rocoso original comúnmente es transportado o reelaborado por algún mecanismo antes de que se forme un suelo. Las variaciones en la historia del material inicial conducen a una variedad de tipos de materiales parentales del suelo (Cuadro 1). Además, estos procesos de meteorización liberan elementos, incluyendo nutrientes vegetales y animales, y convierten los minerales primarios en arcillas.
| Modo de transporte | Modo de deposición | Nombre del material padre |
|---|---|---|
| Gravedad | Gravedad | Colluvium |
| Agua | Stream | Aluvium |
| Lago | Lacustre | |
| Océano | Marina | |
| Hielo | Hielo | Till, morrena |
| Meltwater | Outash (aluvión, lacustre) | |
| Viento | Viento | Loess, dunas |
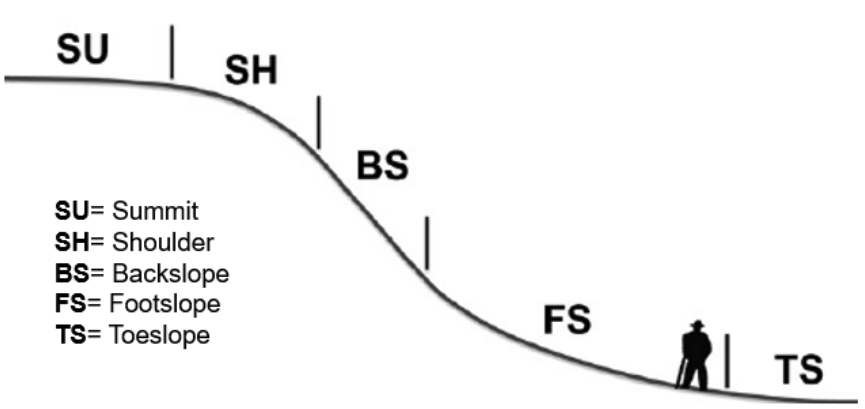
Estos materiales parentales continúan climatando a lo largo del tiempo en función de los factores y procesos de formación del suelo. Otra consideración importante para el potencial de meteorización de los materiales madre del suelo es la posición de la ladera. La posición de ladera hace referencia a donde en el paisaje se ubica un suelo (Figura 1). Posiciones de ladera esenciales y delegar el grado de pendiente e interacción con el nivel freático para los suelos de una ubicación de posición específica. Estas relaciones entre el suelo y la pendiente, o el nivel freático, influyen en gran medida en los procesos de meteorización a lo largo del tiempo, incrementando la meteorización física y química, dependiendo de la posición de la pendiente.
MINERALES
En geología y ciencia del suelo, un mineral es un sólido cristalino inorgánico de origen natural que tiene una composición química definida y propiedades físicas predecibles. De los seis criterios incluidos en esta definición, tres (de origen natural, inorgánico y sólido) necesitan poca elaboración; los tres restantes se explican en párrafos sucesivos.
Cristalinidad de Minerales
Cristalino significa que los átomos de un mineral están dispuestos de manera ordenada y repetible; no son aleatorios. El arreglo atómico, que varía entre los grupos minerales, contribuye a varias de las propiedades físicas del mineral, entre ellas la dureza y la escisión, las cuales se explican bajo “Propiedades físicas de los minerales”. Por el contrario, una sustancia que tiene átomos dispuestos aleatoriamente es amorfa, o no cristalina, y como tal no se considera un mineral. Un buen ejemplo de material amorfo es la obsidiana rocosa, una forma de vidrio volcánico.
Composición Química de Minerales
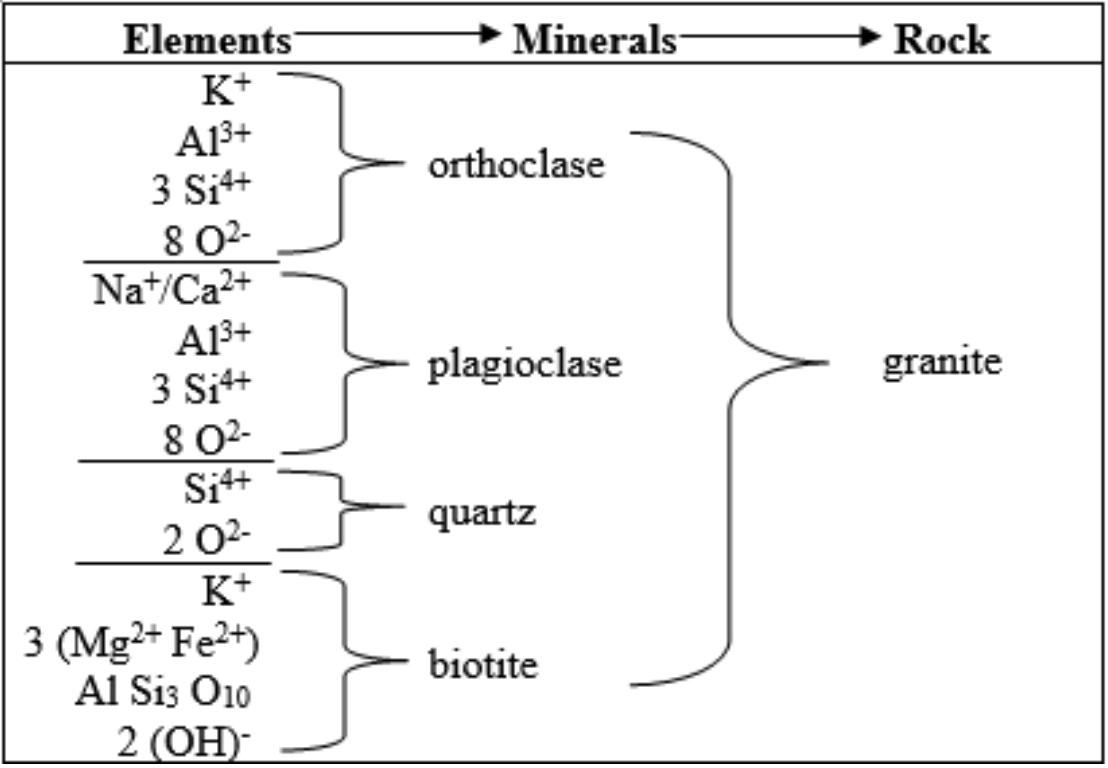
Los minerales están constituidos por uno o más elementos, los cuales dan lugar a composiciones químicas definidas (Figura 2). Aunque las fórmulas químicas se fijan con precisión para algunos minerales (por ejemplo, el cuarzo es SiO2 y la ortoclasa es KalSi3O8), pueden variar dentro de un rango estrecho para otros minerales (por ejemplo, la plagioclasa varía de NaAlSi3O8 a CaAl2Si2O8 porque el Na+ y el Ca2+, que se sustituyen entre sí, ocurren juntos variando proporciones en el mismo mineral). Además, no importa cuán precisa sea la fórmula, ocurren irregularidades en la naturaleza, permitiendo que las impurezas se colen. Obsérvese los elementos y minerales en la Figura 2. ¿Qué tienen en común los cuatro minerales?
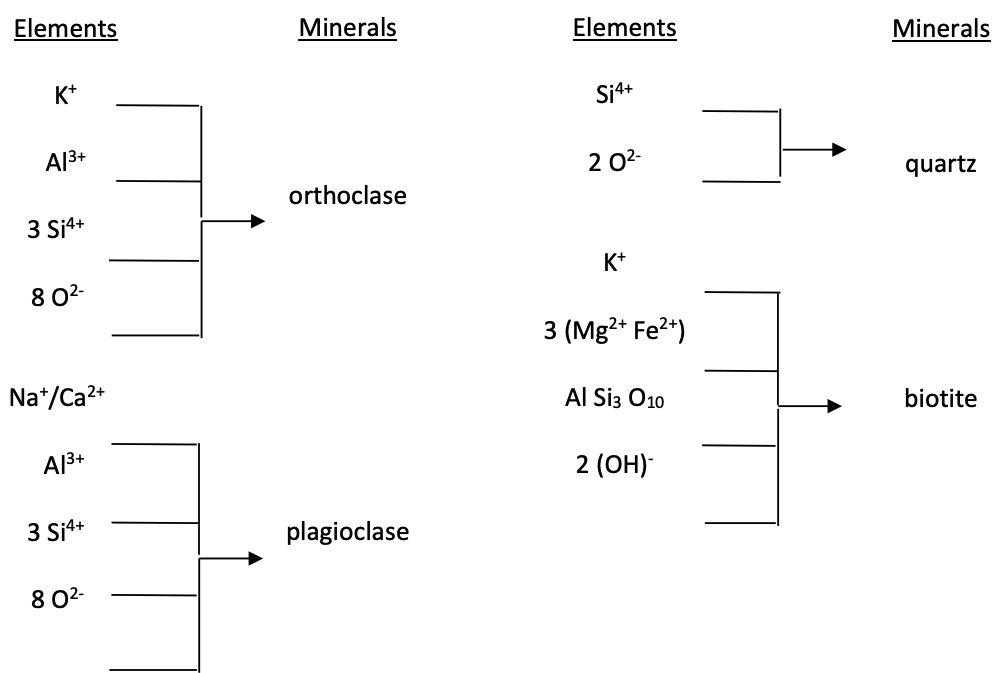
Sobre una base masiva, casi las tres cuartas partes de la corteza terrestre se compone de solo dos elementos: oxígeno y silicio; y sobre una base de volumen, ¡estos dos elementos constituyen más del 90%! Los siguientes seis elementos más comunes llevan los totales a aproximadamente 98.5 por ciento en masa, y a casi 100 por ciento en volumen (Cuadro 2). Obviamente, queda muy poco espacio para los 100 elementos restantes, incluyendo la mayoría de los nutrientes vegetales, que se encuentran en la corteza. ¿Cómo es entonces que los suelos, casi todos los cuales se derivan en última instancia de la intemperie de la corteza, pueden suministrar suficientes elementos nutritivos para casi toda la vida terrestre, incluidas las tres cuartas partes del suministro de alimentos de la humanidad? Tu trabajo en este ejercicio de laboratorio debería ayudarte a comenzar a entender y apreciar la respuesta a esta pregunta.
| Elemento | Fórmula Iónica | Porcentaje de Masa | Porcentaje de Volumen |
|---|---|---|---|
| Oxígeno |
O 2- |
46.60 |
91.97 |
|
Silicio |
Si 4+ |
27.72 | 0.80 |
| Aluminio |
Al 3+ |
8.13 |
0.77 |
| Hierro | Fe 2+ y Fe 3+ | 5.00 | 0.68 |
| Calcio | Ca 2+ | 3.63 | 1.48 |
| Sodio | Na + | 2.83 | 1.60 |
| Potasio | K + | 2.59 | 2.14 |
| Magnesio | Mg 2+ | 2.09 | 0.56 |
Clasificación de minerales basada en la composición química
La mayoría de los minerales se agrupan en siete clases en función de su unidad aniónica fundamental (Cuadro 3). (Existen algunas otras clases, pero éstas pueden ser ignoradas para este laboratorio). De estos, los silicatos son, con mucho, los más comunes; sin embargo, los productos de meteorización de otros pueden ser iguales y vitales.
| Clase Mineral | Ejemplo | Composición Química (espécimen #) |
Comentarios |
|---|---|---|---|
| Sulfuros |
1) pirita 2) esfalerita |
FeS 2 (19) ZnS (17) |
fácilmente oxidado en suelos húmedos |
| Óxidos | hematita | Fe 2 O 3 (15) |
fácilmente oxidado, produciendo colores rojos |
| Halogenuros |
1) halita 2) Sylvita |
NaCl (18) KCl |
sal de roca; a veces se encuentra en suelos desérticos |
| Carbonatos |
1) calcita 2) dolomita |
CaCo 3 (13) CaMG (CO 3) 2 |
1) calcáreo; reacciona a ácido; clima fácilmente en suelos húmedos 2) calcáreo; menos reactivo que la calcita |
| Sulfatos | yeso | CaSO 4 •2H 2 O (20) |
una agricultura común enmienda; a veces encontrados en suelos desérticos |
| Fosfatos | apatita | Ca 5 (PO 4) 3 (F, Cl, OH) (8) |
la única fuente significativa de fósforo |
| Silicatos | olivino | (Mg, Fe) 2SiO 4 |
más fácilmente desgastado de los silicatos |
| piroxeno: augite | (Ca, Na) (Mg, Fe, Al) (Si, Al) 2O 6 (12) | susceptibles a la oxidación e hidratación | |
| anfíbol: hornblende |
(Ca, Na) 2-3 (Mg, Fe, Al) 5Si 6 (Si, Al) 2O 22 (OH) 2 (11) |
susceptibles a la oxidación e hidratación, pero más resistentes que el augite | |
|
micas: 1) moscovita 2) biotita |
1) Kal 2 (AlSi 3 O 10) (OH) 2 (6) 2) K (Mg, Fe) 3 (AlSi 3 O 10) (OH) 2 (7) |
1) suave, pero resiste fuertemente la erosión química 2) suave; los climas más fácilmente que la moscovita |
|
|
feldespatos: 1) ortoclasa 2) plagioclasa |
1) KalSi 3 O 8 (9) 2) Na (AlSi 3 O 8) →Ca (Al 2 Si 2 O 8) (10) |
Minerales más comunes 1) duro, resistente 2) duro, climas |
|
| cuarzo | SiO 2 (4) |
duro y más resistente a la intemperie |
Propiedades Físicas de Minerales
Color: Los minerales existen en casi todos los colores, y aunque el color es fácil de determinar, puede que no sea confiable para identificar un mineral. Por ejemplo, la pirita casi siempre es de color amarillo latoso, pero el cuarzo puede variar a través de varios tonos, valores y cromas de incoloro a blanco, rosa, morado y gris. En algunos minerales, el color puede estar fuertemente influenciado por las impurezas.
Lustre: independiente del color de un mineral y determinado por la naturaleza de la luz reflejada desde la superficie de un mineral. La mayoría de los lusters se agrupan en dos grupos principales: metálicos y no metálicos. Los lustros metálicos son típicos de los minerales que absorben fuertemente la luz, y como resultado son opacos, incluso en piezas muy delgadas. Estos minerales tienden a parecerse a metales, a pesar de que sus superficies pueden variar de brillantes a opacas. Los lustres no metálicos se ven en minerales que permiten que la luz pase a través de rebanadas finamente cortadas. Las superficies de minerales no metálicos pueden ser brillantes como el diamante, vidriosas como el cuarzo, cerosas como serpentinas o terrosas como la arcilla.
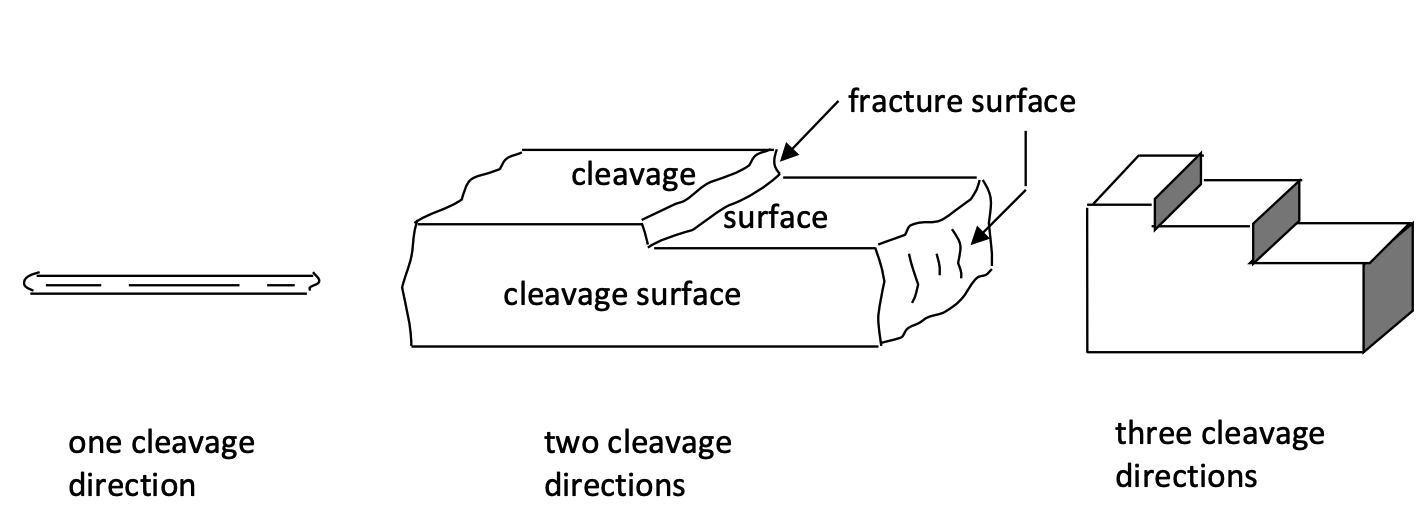
Escisión y fractura: La escisión es la tendencia de un mineral a romperse a lo largo de ciertas direcciones predecibles cuando el mineral es golpeado por un martillo. Las superficies de escisión resultantes pueden ser lisas y distintas, o pueden ser rugosas e indistintas, dependiendo del tipo de mineral. Diferentes minerales también se escinden a lo largo de diferentes direcciones y en diferentes ángulos, dependiendo del tipo y orientación de la unión atómica. Aunque el número de posibles direcciones de escisión es 1, 2, 3, 4 o 6, nos centraremos únicamente en los minerales que tengan direcciones 1 (por ejemplo, biotita), 2 (por ejemplo, ortoclasa) y 3 (por ejemplo, calcita) (Figura 3). Algunos minerales, al ser golpeados por un martillo, no se rompen a lo largo de planos predecibles: simplemente se rompen en cualquier dirección. Se dice que estos minerales se fracturan, más que se escinden. El cuarzo es un buen ejemplo de un mineral que exhibe fractura.
Dureza: La dureza está determinada por la resistencia de la superficie de un mineral al rayado por diversos instrumentos de dureza conocida. Se juzga por la escala de dureza de Mohs, que utiliza ciertos minerales de referencia clasificados de 1 (blando) a 10 (duro): (ver página siguiente
* Escala de Dureza Mohs *
- Talco (fácilmente “rayado” frotándose entre los dedos, dando una sensación jabonosa)
- Yeso (fácilmente rayado por una uña)
- Calcita (misma dureza que un centavo)
- Fluorita
- Apatita (un poco más suave que una hoja de navaja de bolsillo)
- Ortoclasa (más dura que una hoja de cuchillo, pero ligeramente más suave que el vidrio)
- Cuarzo (más duro que una hoja de cuchillo y vidrio)
- Topacio
- Corindón
- Diamante
(Los minerales del suelo rara vez son más duros que 7)
Elementos esenciales para plantas y animales
Los elementos esenciales son aquellos que los organismos necesitan para crecer y completar sus ciclos de vida. Para las plantas, dieciséis elementos son universales y reconocidos como esenciales; sin embargo, investigaciones realizadas a finales del siglo XX sugieren que el número es dieciocho o quizás incluso mayor. Consideraremos que las plantas requieren dieciocho elementos (Cuadro 4), aunque se debe entender que muchas plantas, dependiendo de su especie, ocupan más de lo que parecen necesitar.
Una frase mnemotécnica puede ayudarte a memorizar los 18 elementos:
C HOPKNS Café Mg B Mn CuZn Cl Como Ni
Traducido, esto dice “Café C Hopkns, administrado por “míos” primos Clyde, Como y Nicky”.
Nótese que de los ocho elementos más comunes en la corteza terrestre, sólo cinco, oxígeno, hierro, calcio, potasio y magnesio, se encuentran entre los 18 elementos esenciales (Cuadro 4); y el primero de ellos, el oxígeno, es suministrado por O2 en la atmósfera, no por meteorización de minerales y rocas. De los trece elementos esenciales restantes, el hidrógeno proviene del agua, el carbono proviene del dióxido de carbono (CO2) en la atmósfera y el nitrógeno se mantiene mediante ciclos de materia orgánica. (El nitrógeno primero se pone a disposición de las plantas mediante la fijación de la atmósfera). Los diez elementos restantes, fósforo, azufre, boro, manganeso, cobre, zinc, cloro, molibdeno, níquel y cobalto, derivan de la meteorización de minerales y rocas
| Macronutrientes | Micronutrientes | ||||
|---|---|---|---|---|---|
| Elemento | Símbolo atómico | Formulario disponible para plantas | Elemento | Símbolo atómico | Formulario disponible para plantas |
| carbono | C | CO 2 | hierro |
Fe |
Fe 2+, Fe 3+ |
| hidrógeno | H | H + | manganeso | Mn | Mn 2+ |
| oxígeno | O | O 2, H 2 O | boro | B | H 3 BO 3 |
| nitrógeno | M | NH 4 +, NO 3 - | zinc | Zn | Zn 2+ |
| fósforo | P | H 2 PO 4 -, HPO 4 2- | cobre | Cu | Cu 2+ |
| potasio | K | K + | cloro | Cl | Cl - |
| calcio | Ca | Ca 2+ | cobalto | Co | Co 2+ |
| magnesio | Mg | Mg 2+ | molibdeno | Mo | MoO 4 2- |
| azufre | S | SO 4 2- | níquel | Ni | Ni 2+ |
Además de los 18 elementos que requieren las plantas, los animales también requieren arsénico (As), cromo (Cr), flúor (F), yodo (I), litio (Li), sodio (Na), selenio (Se), silicio (Si) y estaño (Sn). Los animales herbívoros obtienen estos elementos al comer plantas, que absorben los elementos, aunque la planta podría no necesitarlos. Los animales carnívoros, a su vez, obtienen los elementos aprovechándose de otros animales.
Independientemente de si los elementos son requeridos por plantas o animales, todos excepto carbono, hidrógeno, oxígeno y nitrógeno, están disponibles inicialmente por meteorización de minerales. Los elementos se concentran gradualmente en la biosfera a través de ciclos biogeoquímicos, incluyendo los ciclos de carbono y nitrógeno, los cuales serán cubiertos en un laboratorio posterior.
ROCAS
Las rocas más comunes son conjuntos consolidados de minerales, pero algunas (por ejemplo, obsidiana, piedra pómez y carbón) comprenden materiales no cristalinos (por lo tanto, no minerales). A pesar de la gran cantidad de posibles composiciones y arreglos, las rocas pueden dividirse en tres categorías según su modo de formación: ígneas, sedimentarias y metamórficas.
Rocas Ígneas
Intrusivo y Extrusivo: Las rocas ígneas se forman cuando el material fundido llamado magma se enfría y solidifica.
Aunque el magma se origina decenas de kilómetros por debajo de la superficie de la Tierra, puede solidificarse a cualquier profundidad desde su profundidad de origen hasta la superficie. El magma que permanece en profundidad mientras se enfría y solidifica forma rocas ígneas intrusivas. Debido al enfriamiento extremadamente lento, los minerales pueden crecer a un tamaño macroscópico y pueden identificarse fácilmente en un espécimen manual.
En lugar de permanecer profundo durante todo el proceso de enfriamiento, algunos magmas entran en erupción a la superficie, donde se enfrían y solidifican rápidamente. Las rocas extrusivas ígneas resultantes pueden ser vítreas (es decir, amorfas) o microcristalinas, aunque muchas contienen una pequeña cantidad de macrocristales que se formaron antes de la erupción. En erupción, el magma podría rezumar hacia la superficie como lava, o podría explotar violentamente en la atmósfera, formando piedra pómez y ceniza volcánica.
Félsico y Máfico: Además de tener tamaños de cristal distintivamente diferentes, las rocas ígneas también varían en composición mineralógica debido a las diferencias químicas entre los magmas. Algunas rocas están dominadas por el cuarzo y la ortoclasa (feldespato rico en potasio) porque derivaban del magma que era rico en sílice y potasio. Estas rocas, que suelen ser de color claro, se llaman félsicas. Otras rocas ígneas tienen poco o ningún cuarzo u ortoclasa, pero en cambio se caracterizan por plagioclasa cálcica (feldespato rico en calcio) y minerales ferromagnesios (por ejemplo, augita y hornblende). Estos se llaman máficos y son de color oscuro. Otras rocas de composiciones intermedias se pueden encontrar entre estos extremos.
Clasificación de Rocas Ígneas
La tendencia textural causada por las diferentes tasas de enfriamiento, combinada con la tendencia mineralógica resultante de las diferencias químicas en el magma proporcionan la base para clasificar las rocas ígneas (Cuadro 5). Los elementos seleccionados también se combinan para formar minerales, que luego se combinan para formar una roca intrusiva ígnea común (Cuadro 6).
Los minerales accesorios, que pueden ser significativos, también varían de félsico a máfico. De las micas, la moscovita es félsica y la biotita es más máfica. Como resultado, la moscovita se encuentra en rocas félsicas, incluido el granito verdadero, mientras que la biotita puede ocurrir en rocas que van desde félsicas hasta moderadamente máficas. Una roca importante de composición intermedia es la granodiorita, la cual tiene un aspecto característico de sal y pimienta derivado del cuarzo y feldespatos de color claro, especialmente la plagioclasa sódica, combinada con biotita de color oscuro. El olivino, un mineral fuertemente máfico, y el augita, que es un poco menos máfico, son constituyentes comunes del gabro y el basalto.
Cuadro 5. Clasificación de rocas ígneas
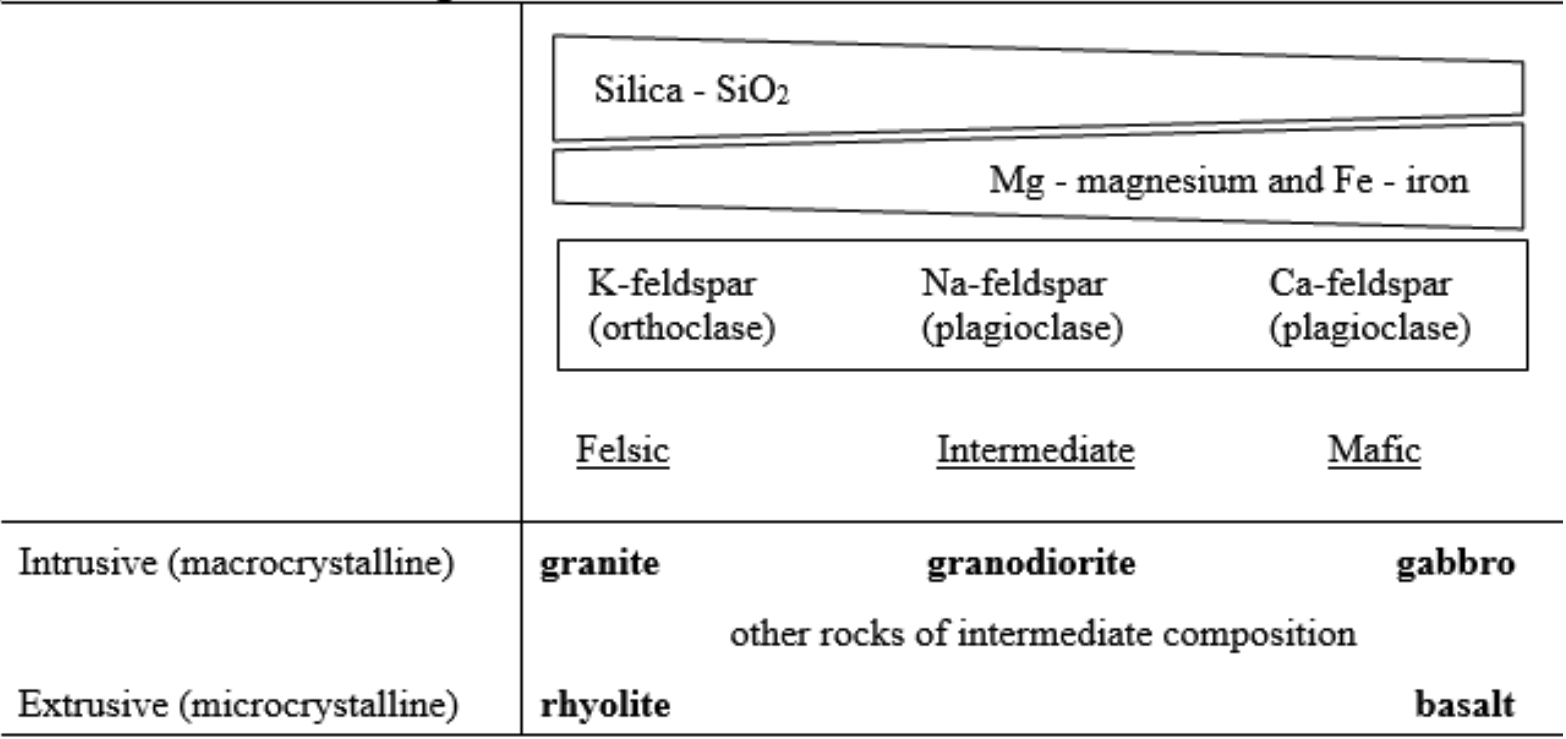
Cuadro 6. Un ejemplo de elementos que se combinan para formar minerales y minerales que se combinan para formar una roca ígnea.
Rocas sedimentarias
Las rocas sedimentarias, que constituyen la mayor parte de la corteza continental de la Tierra, pueden ser clásticas (es decir, fragmentarias) o no clásticas (es decir, no fragmentarias). Consulte el Cuadro 7 para ver ejemplos.
Roca clástica: consiste en fragmentos de rocas previamente existentes (ígneas, sedimentarias o metamórficas) que han sido transportadas a una nueva ubicación (a menudo un fondo oceánico), donde fueron depositadas y enterradas capa tras capa, y cementadas juntas. ¡Los depósitos pueden tener varios miles de metros de espesor!
Los fragmentos, o clastos, pueden variar en tamaño para incluir arcilla, limo, arena, grava y adoquines.
Roca no clástica: forma por precipitación química de sales disueltas y por precipitación bioquímica de compuestos derivados orgánicamente en agua, más comúnmente en los pisos de mares poco profundos. Los organismos que generan rocas no clásticas incluyen bacterias, algas, diatomeas, corales y moluscos. Las rocas sedimentarias no clásticas más comunes son la piedra caliza y la dolomita (también llamada piedra caliza dolomítica). Otros incluyen yeso de roca, chert y carbón.
Aunque se reconocen las dos categorías principales, la mayoría de las rocas sedimentarias son una combinación de clástica y no clástica, sin embargo, suelen ser dominantemente una u otra. Por ejemplo, los granos de arena en la arenisca son clásticos, pero el cemento que los mantiene unidos puede ser no clástico.
| Clastico | No clástico | ||
|---|---|---|---|
| Constituyente dominante | Roca sedimentaria | Constituyente dominante | Roca sedimentaria |
| arcilla | piedra arcillosa | calcita (CaCO3) | piedra caliza |
| limo | limosidad | dolomita (CaMg) (CO3) 2 | dolomita |
| barro (limo + arcilla) | Mudstone | yeso (CaSO4•2H2O) | yeso |
| barro en capas delgadas | esquisto | cuarzo microcristalino (SiO2) | chert |
|
arena (≥ 50%): principalmente cuarzo, feldespatos, micas arena: 50-85% de arena con resto de lodo y posiblemente algunos guijarros arena: > 85% de arena con resto de lodo y posiblemente guijarros |
areniscas Wacke (arenisca sucia) arenita (arenisca limpia) |
||
| grava (guijarros) con arena y barro; cuarzo, ortoclasa, cuarcita | conglomerado | ||
Rocas Metamórficas
Las rocas metamórficas se forman principalmente por la aplicación de calor y presión extremadamente altas a algunas rocas previamente existentes. La roca original puede ser ígnea, sedimentaria o incluso metamórfica, pero las rocas sedimentarias son las más susceptibles a la metamorfosis. Las rocas metamórficas pueden ser foliadas o no foliadas. Las rocas foliadas consisten en minerales que están alineados u orientados para producir una apariencia algo estratificada o estratificada, mientras que los minerales en las rocas no foliadas están casi igualmente dispuestos en todas las direcciones, dándoles una apariencia más uniforme y masiva (Cuadro 8).
| Foliado | ||
|
Roca Metamórfica |
Roca Original Común |
Apariencia/Comentarios |
| pizarra | esquisto | fuertemente estratificado (estratificado), plano; a menudo con cuarzo muy fino y mica; se escinde en láminas, pero más densas que el esquisto |
| esquisto |
esquisto u otra pizarra |
foliación ondulada; a menudo con micas, cuarzo, feldespatos |
| gneiss (pronunciado “nice”) |
rocas graníticas |
minerales orientados a dar una estratificación más débil que el esquisto; a menudo contiene los mismos minerales que su contraparte granítica |
| No Foliado | ||
| mármol |
piedra caliza |
escisión de calcita generalmente visible; fizzes para liberar CO2 cuando se prueba con HCl |
| cuarcita | arenita de cuarzo | duro; muy resistente a la intemperie |
| serpentinita | peridotita (una roca ígnea ultramáfica) | ensamble verdoso de minerales serpentinos; alto contenido de magnesio; ocurre intermitentemente a lo largo de la costa oeste de América del Norte, y áreas más pequeñas de la costa este |
INTEMPERACIÓN
La meteorización rompe rocas y minerales, lo que resulta en la producción de suelos. La meteorización se produce a través de dos procesos: la desintegración física (rompiendo en trozos más pequeños) y la descomposición química (cambiando la naturaleza de los propios minerales).
La desintegración física hace que las masas de roca se separen o se desgasten y se desgasten de la superficie rocosa más grande. La congelación y descongelación, la abrasión por partículas suspendidas en el viento o el agua y la molienda causada por los glaciares resultan en la desintegración. Las acciones repetidas de estos procesos provocan tensiones, que eventualmente rompen y erosionan las superficies rocosas. La meteorización física generalmente precede o ocurre en concierto con el proceso de descomposición química. Con una disminución en el tamaño de las partículas individuales, el número total de esquinas y bordes y la superficie total de la masa rocosa aumentan en gran medida.
Descomposición química
La descomposición química progresa más rápidamente cuando hay más área de superficie disponible para que ocurran reacciones químicas. Los ambientes cálidos y húmedos mejoran la descomposición química. Cuanto más pequeñas sean las partículas, mayor será la superficie de un volumen dado de roca (mayor será el total de esquinas y bordes expuestos) y mayor será la tasa de descomposición química. El número total de esquinas expuestas a procesos de meteorización es el factor principal en la determinación de las tasas de meteorización. Esto se debe a que una esquina tiene tres superficies y tres bordes para ataque químico. La meteorización química es una combinación de cinco procesos principales: carbonatación, hidratación, hidrólisis, oxidación-reducción (redox) y solución.
Hidrólisis y tamaño de partícula: La hidrólisis es un proceso de descomposición química que implica la división de moléculas de agua durante una reacción. Una reacción de hidrólisis se puede identificar fácilmente buscando agua en el lado izquierdo de una ecuación química y la ausencia de agua (pero la formación de H + y/o OH -) en el lado derecho de la ecuación. Todos los minerales climatológicos por hidrólisis. La reacción de hidrólisis es particularmente evidente con minerales de silicato (por ejemplo, feldespatos y micas). La hidrólisis es la reacción primaria que resulta en la liberación de la mayoría de los elementos nutritivos vegetales de los minerales. La ortoclasa mineral resistirá por hidrólisis.
\[ \mathrm{KAlSi_3O_8 + H_2O \rightarrow HAlSi_3O8 + K^+ + OH^-} \nonumber \]
Orthoclasa + Agua\(\rightarrow\) mineral de Al silicato + Ión Potasio + Ión
El catión potasio (K +) liberado por esta reacción de hidrólisis es soluble en agua y puede ser adsorbido por los minerales arcillosos del suelo y coloides orgánicos, utilizados por las plantas, o ser removido (lixiviado) por el agua de drenaje. El compuesto de silicato de aluminio puede cristalizar en un mineral arcilloso (p. ej. caolinita). Este proceso de meteorización química natural ocurre a una velocidad muy lenta pero continua en todas las rocas, materiales madre y suelos. Cuanto más pequeño sea el mineral original, más rápida se producirá la reacción de hidrólisis. El ion hidróxido (OH -) incrementará el pH. Cuando un glaciar muele rocas con hielo glacial (agua), la molienda es un proceso de desintegración física. Sin embargo, la reacción de hidrólisis resultante de las partículas finas que se hidrolizan con el agua provoca que la caja glacial tenga un pH alto (pH de abrasión). Inicialmente, el pH de la caja glacial será de 9 o 10, pero a medida que la caja glacial absorbe dióxido de carbono del aire, el pH bajará.
Carbonatación y Solución: Las actividades metabólicas de las raíces y microorganismos de las plantas producen una abundancia de CO 2 dentro de los poros del suelo. Este CO 2 reacciona con el agua del suelo para producir la mayor parte del ácido carbónico que se encuentra en los suelos.
\[ CO_2 + H_2O \leftrightarrow H_2CO_3 \nonumber \]
Dióxido de Carbono + Agua Ácido\( \leftrightarrow \) carbónico
El ácido carbónico en el agua del suelo reacciona continuamente con los minerales a medida que el agua se percola a través de suelos y rocas. El ácido carbónico, un ácido débil, es el ácido más común que se encuentra en los suelos. El ácido carbónico puede ionizarse en iones de hidrógeno ácidos (H +) y bicarbonato (HCO 3 -):
\[H_2CO_3 \leftrightarrow H^+ + HCO_3 \nonumber \]
Ácido carbónico Ión hidrógeno\( \leftrightarrow \) ácido + Ión bicarbonato
A pH < 6, esta reacción tiende a ir más a la izquierda que a la derecha, lo que indica que el ácido carbónico es un ácido débil y no produce muchos iones de hidrógeno ácidos. El ácido carbónico es eficaz para acelerar los procesos de descomposición química de los minerales porque la naturaleza proporciona continuamente agua de lluvia y dióxido de carbono. Así, el agua de lluvia impulsa esta reacción hacia la derecha. A medida que el agua de lluvia se mueve a través del suelo, transporta iones de bicarbonato solubles más profundamente en el perfil del suelo y deposita los iones de hidrógeno ácido en las superficies del suelo. La ley de acción masiva permite que el suelo eventualmente se vuelva ácido con el tiempo de meteorización, ya que la lluvia conduce la reacción anterior hacia la derecha.
Como resultado de la molienda de rocas glaciares, la reacción de hidrólisis da como resultado que la caja glacial contenga iones Ca2+ solubles e iones OH- (lo que provoca un pH alto, mayor a 8.3). A medida que la caja glacial se expone al ácido carbónico, la caja glacial experimenta dos reacciones de carbonatación. El primer proceso de reacción es bastante rápido, mientras que la segunda reacción es lenta y requiere tiempo para completarse. La primera reacción de carbonatación es
\[ Ca^{2+} + 2OH^- + H_2CO^3 \rightarrow CaCO_3 + 2H_2O \nonumber \]
Calcio soluble + Hidróxido soluble + Ácido carbónico Calcita\( \rightarrow \) baja soluble + Agua
La segunda reacción es:
\[ CaCO_3 + H_2CO_3 \rightarrow Ca(HCO_3)_2 \nonumber \]
Calcita + Ácido carbónico Bicarbonato de calcio\( \rightarrow \) soluble
El bicarbonato de calcio se disuelve lentamente y libera iones de calcio solubles (Ca 2+) para la absorción de la planta o posible lixiviación hacia abajo a través del suelo cuando se produce una lluvia excesiva o riego. La pérdida de los minerales de calcita (el principal mineral en la piedra caliza) eventualmente conduce al desarrollo de suelos ácidos, carbonatos duros y la formación de enormes cavernas subterráneas (por ejemplo, Mammoth Cave y Carlsbad Caverns). La cueva por la que se camina es el agujero que queda después de que el bicarbonato de calcio soluble haya salido de la cavidad donde el ácido carbónico disolvió la roca caliza.
El calcio soluble y el bicarbonato se mueven hacia abajo y entran en el agua subterránea, que finalmente emerge como agua en arroyos que fluyen hacia el océano. La presencia del bicarbonato de calcio en las aguas subterráneas es la razón principal por la que el agua subterránea de piedra caliza se denomina “agua dura”.
Finalmente, la segunda reacción tiene dos efectos principales en un ambiente de alta precipitación. Primero, el suelo superficial se volverá ácido y el pH disminuirá debido al aumento de las precipitaciones y la producción de CO 2 (H 2 CO 3). Segundo, el calcio soluble se pone a disposición de las plantas. Sin embargo, más lluvias lixiviarán el bicarbonato de calcio soluble a la baja.
Eventualmente, el suelo se agotará de calcio (Ca 2+). El mismo fenómeno será cierto para los cationes de magnesio (Mg 2+), potasio (K +) y sodio (Na +) liberados al suelo por la hidrólisis de diversos minerales. Este proceso da como resultado una pérdida de la nutrición general de las plantas y la fertilidad del suelo.
Reacciones de reducción-oxidación (redox): implican la transferencia de electrones de un reactivo a otro. En cada reacción redox, alguna sustancia se oxida y alguna otra sustancia se reduce por la transferencia del electrón. La sustancia que pierde el electrón se oxida y el componente que acepta los electrones se reduce. Comúnmente, pero no siempre, el oxígeno sirve como agente oxidante.
El oxígeno se combina con un elemento en un mineral, como el hierro (Fe 2+), haciendo que el hierro renuncie a algunos de sus electrones, los cuales son aceptados por el oxígeno. El hierro se oxida mientras que el oxígeno se reduce. Estas transferencias de electrones constituyen una forma de meteorización química, que altera la estructura atómica del mineral, liberando varios elementos y conduciendo al desarrollo de nuevos compuestos, incluidos los minerales arcillosos.
Aunque las reacciones redox se producen continuamente en los suelos, sus velocidades de reacción pueden ser muy lentas e imperceptibles. Si un suelo está húmedo y bien aireado, el hierro tiende a oxidarse (Fe 3+, pierde electrones por oxígeno), pero si el aire (gas oxígeno) está ausente, como ocurre con el suelo saturado de agua, el hierro se reduce (Fe 2+, gana electrones). El grado de oxidación o reducción en los suelos se manifiesta en el color del suelo. El hierro oxidado (Fe 3+) ocurre donde el oxígeno está presente en suelos bien drenados y produce colores rojos, amarillos o marrones en los suelos. El hierro reducido (Fe 2+) existe en suelos inundados o muy poco drenados y produce colores negro, gris, oliva y azul. Los períodos alternos de oxidación y reducción, causados por la fluctuación de los niveles de agua en un suelo, dan como resultado moteado (manchas de rojo y amarillo mezcladas con colores grises). Las condiciones continuas de fuerte reducción causadas por el anegamiento a largo plazo forman condiciones de deslumbramiento. Los suelos Gleyed tienen colores de gris oscuro a azul a negro.
\[ Fe^{2+} \xleftrightarrow{O_2} Fe^{3+} \nonumber \]
Reducido (colores grises del suelo) ↔ Oxidado (colores del suelo rojo y amarillo)
Lea y complete la siguiente actividad y preguntas. Todas las preguntas deben ser respondidas y los laboratorios concluidos vencen al final del periodo de laboratorio. No se aceptarán trabajos tardíos.


