6.4: Modelo ODE y Excel CSTR con intercambio de calor
- Page ID
- 85606
Introducción
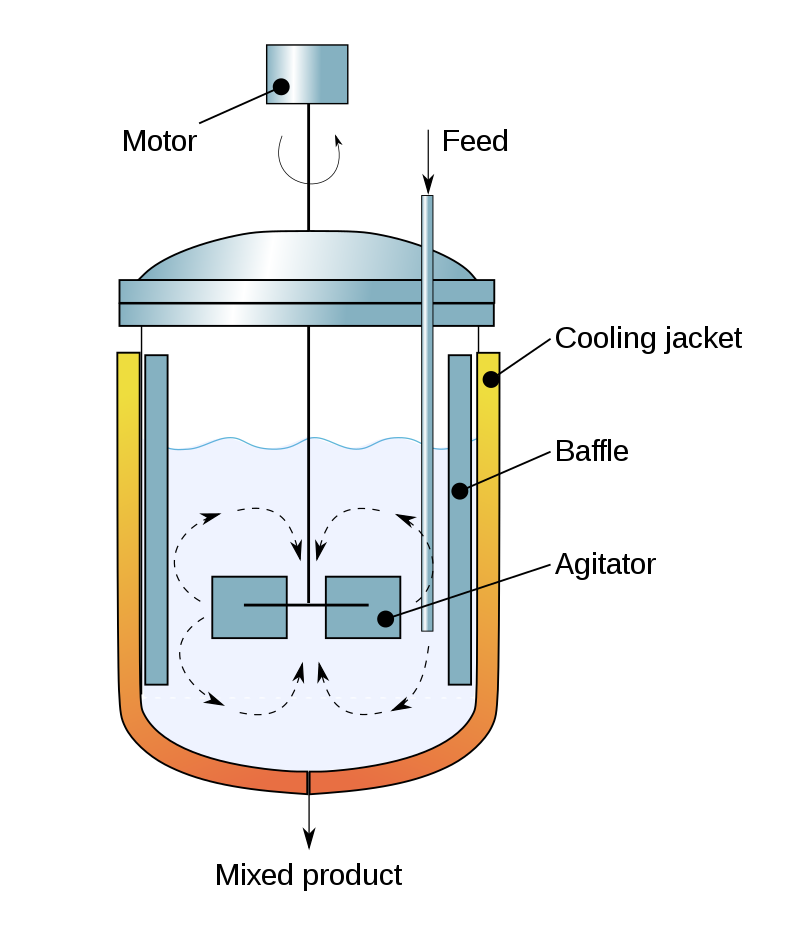
Un reactor de tanque agitado continuo (CSTR) es un recipiente de reacción química en el que un impulsor agita continuamente el contenido asegurando una mezcla adecuada de los reactivos para lograr una salida específica (Figura\(\PageIndex{1}\)). Útil en la mayoría de los procesos químicos, es una piedra angular del kit de herramientas de ingeniería química. El conocimiento adecuado de cómo manipular las ecuaciones para el control del CSTR equivale a la operación exitosa y producción de los productos deseados. El propósito de esta sección es modelar condiciones dinámicas dentro de un CSTR para diferentes condiciones de proceso. La simplicidad dentro del modelo se utiliza ya que el enfoque es entender el proceso de control dinámico.
Supuestos
Para los efectos de esta sección, hemos hecho los siguientes supuestos para explicar CSTR con modelado de intercambio de calor.
- Mezcla perfecta: El agitador dentro del CSTR creará un ambiente de mezcla perfecta dentro del recipiente. La corriente de salida tendrá la misma concentración y temperatura que el fluido del reactor.
- Reacción única de primer orden: Para evitar confusiones, la cinética compleja no se considera en los siguientes modelos. \ [\ -r_ {a} =k C_ {A}]
- Parámetros especificados: Suponemos que se han especificado los parámetros necesarios para resolver el problema.
- Volumen especificado: En un ambiente de control, el tamaño de la embarcación generalmente ya está especificado.
- Propiedades Constantes: Para este modelo, hemos hecho la suposición de que las propiedades de las especies que estamos tratando de modelar permanecerán constantes en el rango de temperatura en el que estaremos viendo. Es importante hacer esta suposición, ya que de lo contrario estaremos lidiando con un problema mucho más complejo que tiene una capacidad calorífica variable, calor de reacción, etc.
Modelado de ODE en Excel
Para configurar el modelo, los balances de masa y energía deben considerarse en todo el reactor. A partir de estos balances energéticos, podremos desarrollar relaciones para la temperatura del reactor y la concentración del reactivo limitante dentro del mismo.
Definiciones de variables
La siguiente tabla da un resumen de todas las variables que utilizamos en nuestras fórmulas matemáticas.
| Símbolo | Significado | Símbolo | Significado |
|---|---|---|---|
| V | Volumen de Reactor | ρ | Densidad de la corriente |
| m | Caudal másico | C A0 | Concentración Original |
| C A | Concentración de corriente | T 0 | Temperatura Original |
| T | Temperatura actual | T C | Temperatura del Refrigerante |
| ΔH rxn | Calor de Reacción | ΔC p | Cambio general en la capacidad calorífica |
| k 0 | Constante de Ley de Tasa | E | Energía de activación |
| R | Constante de Gas Ideal | UA | Coeficiente general de transferencia de calor |
Balance de Masa
A partir de nuestros cursos de balance energético y material, sabemos que la ecuación general para un balance de masas en cualquier sistema es la siguiente:
\[\text {Rate Accumulation}= (\text {Flow } \text {In})-(\text{Flow Out}) - (\text{\mathrm{Rate } \text{Generation}) } \nonumber \]
\[\text{Rate Accumulation} =V \frac{d C_{A}}{d t} \nonumber \]
\[\text {Flow In}-\text {Flow } \mathrm{Out} =\frac{m}{\rho}\left(C_{A 0}-C_{A}\right) \nonumber \]
\[\text{Rate Generation} =V\left(-r_{a}\right)=V C_{A} k_{0} e^{-E / R T} \nonumber \]
En el caso de un CSTR, sabemos que la tasa de acumulación será igual a\(V \frac{d C_{A}}{d t}\). Esto viene de que el número global de moles en el CSTR es\(V C_{A}\), por lo que la acumulación de moles solo será el diferencial de esto. Ya que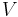 es una constante, esto se puede sacar del diferencial, y nos quedamos con nuestro resultado anterior. También sabemos que el flujo de moles in versus el flujo de moles out es igual a\(\frac{m}{\rho}\left(C_{A 0}-C_{A}\right)\), que es el caudal másico, dividido por la densidad del flujo, y luego multiplicado por la diferencia en la concentración de moles en la corriente de alimentación y la corriente de producto. Finalmente, podemos determinar cuál es la tasa de generación de moles en el sistema usando la Ecuación de Arrhenius. Esto nos dará la tasa de generación igual a
es una constante, esto se puede sacar del diferencial, y nos quedamos con nuestro resultado anterior. También sabemos que el flujo de moles in versus el flujo de moles out es igual a\(\frac{m}{\rho}\left(C_{A 0}-C_{A}\right)\), que es el caudal másico, dividido por la densidad del flujo, y luego multiplicado por la diferencia en la concentración de moles en la corriente de alimentación y la corriente de producto. Finalmente, podemos determinar cuál es la tasa de generación de moles en el sistema usando la Ecuación de Arrhenius. Esto nos dará la tasa de generación igual a
.
Combinando todas estas ecuaciones y luego resolviendo para\(\frac{d C_{A}}{d t}\), obtenemos eso:
\[\frac{d C_{A}}{d t}=\frac{m}{\rho V}\left(C_{A 0}-C_{A}\right)-k_{0} C_{A} e^{-E / R T} \nonumber \]
Balance Energético
De nuestros cursos de termodinámica, sabemos que la ecuación general para un balance energético en cualquier sistema es la siguiente:
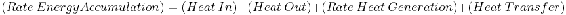
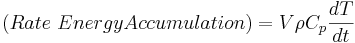
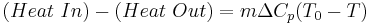
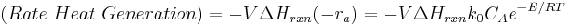
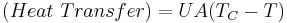
En el caso de un CSTR, sabemos que la tasa de acumulación de energía dentro del reactor será igual a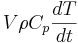 . Esta ecuación es básicamente el número total de moles (masa real) en el reactor multiplicado por la capacidad calorífica y el cambio de temperatura. También sabemos que el calor generado por esta reacción es
. Esta ecuación es básicamente el número total de moles (masa real) en el reactor multiplicado por la capacidad calorífica y el cambio de temperatura. También sabemos que el calor generado por esta reacción es, que es la velocidad de generación de masa (− Vr a) multiplicado por el calor específico de reacción (Δ H rxn). La tasa general de transferencia de calor dentro y fuera del sistema viene dada por
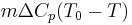 . Esta ecuación es el caudal multiplicado por la capacidad calorífica y la diferencia de temperatura, lo que nos da la cantidad total de flujo de calor para el sistema. Finalmente, la cantidad de calor transferido al sistema viene dada por
. Esta ecuación es el caudal multiplicado por la capacidad calorífica y la diferencia de temperatura, lo que nos da la cantidad total de flujo de calor para el sistema. Finalmente, la cantidad de calor transferido al sistema viene dada por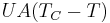 . Combinando todas estas ecuaciones y resolviendo el balance energético para
. Combinando todas estas ecuaciones y resolviendo el balance energético para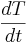 , obtenemos eso:
, obtenemos eso:
En una situación realista en la que muchos productos químicos procesados se enfrentan a múltiples reacciones y efectos de calor, se deben hacer ligeros cambios en la ecuación modelada. El siguiente diagrama evalúa el intercambiador de calor bajo efectos de calor en los que hay una temperatura de entrada y salida que se contabiliza en el término de entalpía en la ecuación recién modelada.
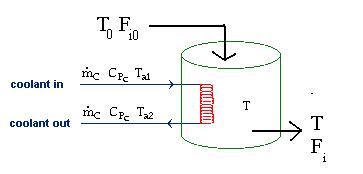
Para modelar un intercambiador de calor que tenga en cuenta múltiples reacciones, simplemente tome el\(\delta C_p\) término\(\delta H_{rxn}\) y y agregue la letra griega sigma para la suma frente a los términos. Al considerar un caso con múltiples reacciones y efectos térmicos, la entalpía y la capacidad calorífica de cada reacción deben implementarse en el balance energético, de ahí que i y j representan las especies de reacción individuales. La ecuación ahora se ve algo así:
Método de Euler
Para modelar una ODE en Excel, utilizaremos el Método de Euler. La razón por la que elegimos el Método de Euler sobre otros métodos (como Runge-Kutta) se debió a la simplicidad asociada con el de Euler. Tratar de modelar con métodos como Runge-Kutta es mucho más difícil en Excel, mientras que el método de Euler es bastante sencillo. También verificamos la exactitud de nuestros resultados usando el Método de Euler comparando nuestras respuestas con la de Polymath, un programa de modelado ODE de alta precisión. Encontramos que nuestras respuestas fueron las mismas que las de Polymath, por lo que nos sentimos bastante cómodos usando el Método de Euler para nuestro modelo. Aquí están todos los detalles sobre el Método de Euler. Para este modelo, nos interesará principalmente el cambio en la concentración de un reactivo y la temperatura del reactor. Estas son las dos ecuaciones diferenciales que pudimos obtener de los balances de masa y energía en la sección anterior. La siguiente es una aplicación del método de Euler para el CSTR sobre el cambio en la concentración:
\[C_{A i}=C_{A(i-1)}+\frac{d C_{A}}{d t} \Delta t \nonumber \]
Esta misma aplicación se puede hacer al cambio de temperatura con respecto al tiempo:
\[T_{i}=T_{i-1}+\frac{d T}{d t} \Delta t \nonumber \]
Suponiendo que todos los valores en las ODE permanecen constantes excepto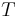 y
y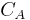 , el nuevo valor se encuentra entonces tomando el valor permeable y sumando el cambio diferencial multiplicado por el paso de tiempo.
, el nuevo valor se encuentra entonces tomando el valor permeable y sumando el cambio diferencial multiplicado por el paso de tiempo.
Lista de Ecuaciones
A continuación se presenta una lista resumida de todas las ecuaciones que se utilizarán al modelar CSTR con un intercambio de calor.
\[\frac{d C_{A}}{d t}=\frac{m}{\rho V}\left(C_{A 0}-C_{A}\right)-k_{0} C_{A} e^{-E / R T} \nonumber \]
\[C_{A i}=C_{A(i-1)}+\frac{d C_{A}}{d t} \Delta t \nonumber \]
\[T_{i}=T_{i-1}+\frac{d T}{d t} \Delta t \nonumber \]
Combinar el uso de Excel
Para modelar el CSTR usando Excel se utiliza el Método de Euler, Balance Energético y Balance de Masa juntos para resolver la concentración en el tiempo t.
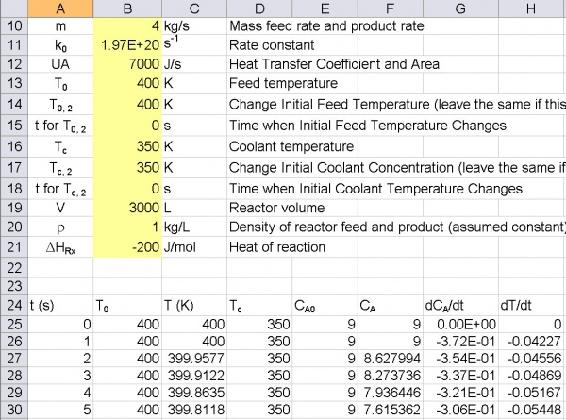
Captura de pantalla del modelo Excel para CSTR con intercambio de calor
Cómo usar nuestro modelo
Para ayudar a facilitar la comprensión de este proceso, hemos desarrollado una hoja de cálculo Excel específicamente para observar los cambios en la concentración y temperatura dado algún cambio en la entrada al sistema CSTR. Un ejemplo de un cambio en el sistema podría ser que la temperatura de la corriente de alimentación haya disminuido en un número dado de grados, o que la velocidad a la que se está suministrando la corriente de alimentación haya cambiado en alguna cantidad. Al usar nuestra hoja de cálculo, podrá conectar fácilmente sus parámetros dados y observar la tendencia de la concentración y la temperatura en un amplio intervalo de tiempo.
La forma en que funciona esta hoja de cálculo es bastante sencilla. Se proporcionan cajas para que ingrese toda la información dada para su problema de CSTR. También se han proporcionado diversas columnas que contienen valores para la temperatura, concentración, etc., con respecto al tiempo. Luego hay más columnas que contienen los valores para las diversas ecuaciones diferenciales desde arriba. Con la derivada del tiempo en la mano, entonces podemos predecir el valor de la temperatura o concentración en el siguiente intervalo de tiempo dado.
Nuestro modelo Excel fácil de usar se da aquí: Plantilla de Modelado CSTR. En nuestro modelo, encontrará una columna de incógnitas que deben especificarse para resolver la temperatura de conversión óptima y la concentración óptima de A. Luego hay dos celdas que mostrarán la temperatura y concentración óptimas. También se proporcionan gráficas para observar el cambio de temperatura y concentración a lo largo del tiempo. La mayoría de las variables del modelo son autoexplicativas. Una característica importante de nuestro modelo es la opción de tener un cambio en la temperatura de la corriente de alimentación o la concentración de A después de un tiempo dado t. No es necesario ingresar un valor para estas celdas si no hay cambio en la alimentación; solo proporciona una manera conveniente de ver el cambio de temperatura y concentración de A. También se le proporciona una celda para el paso de tiempo,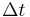 . Dependiendo del tamaño de paso de tiempo que elija, es posible que deba elegir un valor mayor si sus gráficas no alcanzan el estado estacionario. Si este es el caso, las celdas de salida le indicarán que aumente el paso de tiempo.
. Dependiendo del tamaño de paso de tiempo que elija, es posible que deba elegir un valor mayor si sus gráficas no alcanzan el estado estacionario. Si este es el caso, las celdas de salida le indicarán que aumente el paso de tiempo.
Aplicaciones para el Control de Procesos
El modelo creado puede dar cuenta de muchas situaciones diferentes. Sin embargo, en el control de procesos, es muy importante que se considere lo siguiente.
- Reacción exotérmica - En la industria, la reacción exotérmica suele ser de mayor importancia para los controles ya que hay un factor de seguridad involucrado. (es decir, condiciones explosivas del reactor)
- Constante de volumen - Para los CSTR, se utilizan principalmente líquidos.
El modelo desarrollado puede ayudar a controlar un proceso real de muchas maneras, incluyendo las siguientes, pero no limitadas a:
- Mantenimiento de la concentración del producto a pesar de los cambios
- Predecir y prevenir las condiciones explosivas del reactor
- Optimización del caudal
- Optimización de concentración de entrada
- Optimización de temperatura de funcionamiento
- Optimización de temperatura del refrigerante
Este modelo es muy útil para muchas situaciones simples de reactores y ayudará en la comprensión de un proceso y cómo las situaciones dinámicas afectarán la operación.
En aplicaciones de la vida real, la reacción puede no ser de primer orden o irreversible o implicar múltiples reacciones. En todos estos casos, modificamos el Balance Energético y Masivo con consideraciones adicionales de ley de tarifas.
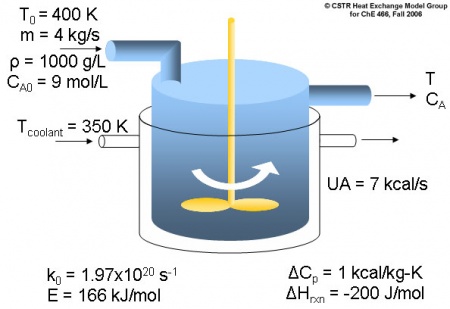
Usted es contratado por WOW Chemical para controlar el funcionamiento de su CSTR con camisa de 3000 L. Desean crear el químico B a partir del químico A en una conversión óptima. ¿Cuál es la temperatura a la que se logra la conversión óptima?
A → B es una reacción irreversible de primer orden.
Alguna información sobre el proceso:
Temperatura de la corriente de alimentación = 400 K
Temperatura del refrigerante = 350 K
Calor de reacción = -200 J/mol
Concentración de entrada de A = 9 mol/L
Caudal de entrada = 4 kg/s
Densidad de A = 1000 g/L
UA del intercambiador de calor = 7 kcal/s
Constante de velocidad = 1.97x10 20 s -1
Energía de activación = 166 kJ/mol
Cambio general en la capacidad calorífica = 1 Kcal/kg-K.
 |
Funcionado Ejemplo 1
4.6.1 Respuesta al Ejemplo Problema #1
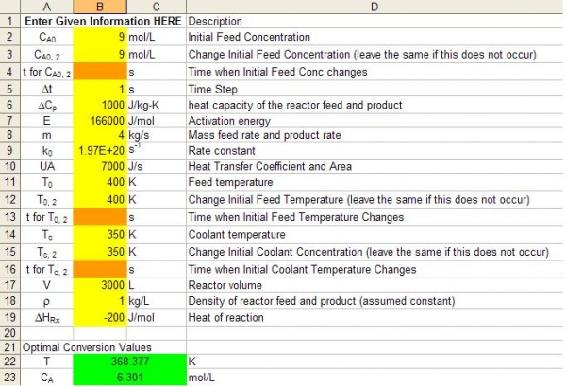
Al usar nuestra hoja de trabajo handy-dandy, vemos que la conversión óptima ocurre en 368.4 K. Esto proviene de ingresar toda la información dada de la declaración del problema en la hoja de Excel, y luego leer el valor para la temperatura óptima. Además, asegúrate de que estás convirtiendo a unidades adecuadas, como de kJ a J, para usar nuestro modelo (solo para ver si estabas prestando atención a las unidades).
Ejemplo 1 Solución
Funcionado Ejemplo 2
1. En el ejemplo anterior, la planta operaba durante el día. Por la noche, hay una caída de 5 K en la temperatura de la corriente de alimentación. Para mantener la misma concentración necesitamos...
A. Disminuir la temperatura del agua de refrigeración en el intercambiador de calor.
B. Aumentar la temperatura del agua de refrigeración en el intercambiador de calor.
C. Mantener la misma temperatura del agua de refrigeración en el intercambiador de calor.
2. Por la noche, el caudal de entrada del sistema también disminuye debido a que la planta no opera a plena capacidad. ¿Qué sucede con la temperatura de la reacción si la concentración de A en la corriente de alimentación permanece igual?
A. Disminución
B. Incremento
C. Permanecer igual
3. Finalmente, si la constante de velocidad se duplicó, ¿qué efecto tendrá esto en la concentración general si la temperatura se mantiene constante?
A. Incremento
B. Disminución
C. Permanecer igual
Respuestas al Ejemplo Problema #2
1: B. Dado que la temperatura de la corriente de alimentación ha disminuido, necesitaremos aumentar la temperatura de la corriente de enfriamiento para mantener la misma temperatura a la que el CSTR estaba operando antes. Usando la hoja de cálculo Excel del Ejemplo 1 y bajando la temperatura de la corriente de alimentación en 5 K, podemos ver primero que la temperatura del CSTR ha caído a 366.5 K.
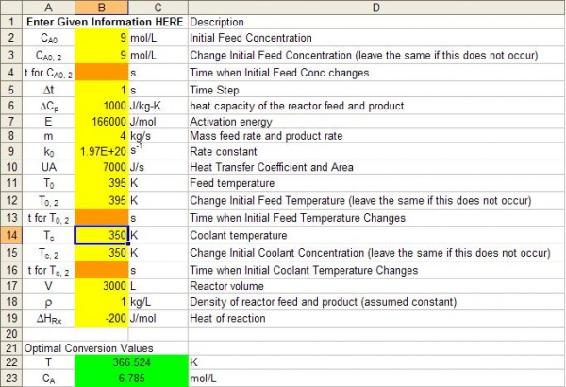
Luego podemos ajustar la temperatura de la corriente de alimentación y ver que debe elevarse 3 K para volver a la temperatura de funcionamiento original de 368.4 K.
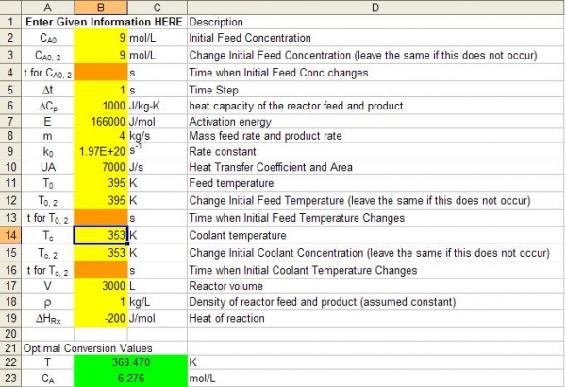
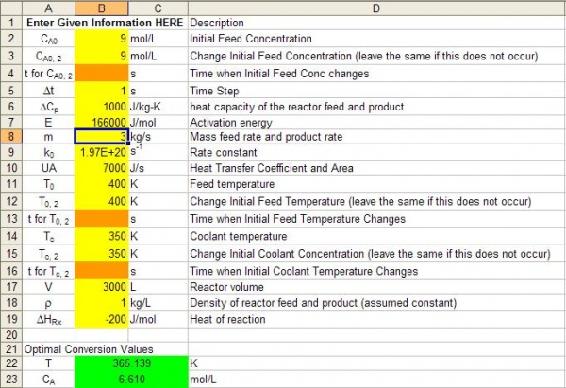
2: A. Dado que hay menos alimentación entrando en el CSTR, la temperatura óptima del reactor también disminuirá. Esto se puede ver de nuevo usando nuestro modelo Excel del Ejemplo 1. Sabemos que originalmente la temperatura del reactor estaba en 368.4 K. Al disminuir el caudal a 3 kg/s, podemos ver que la temperatura del reactor disminuye en más de 3 K hasta 365.1 K.
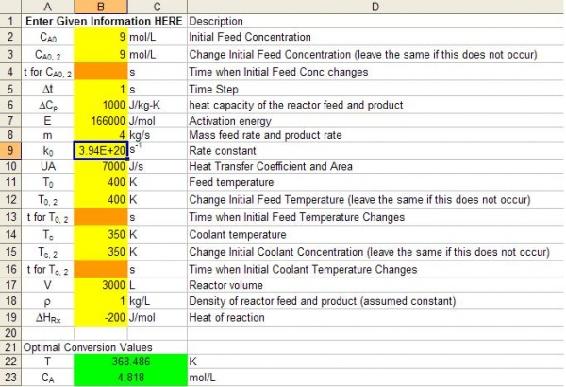
3: B. Vemos en las ecuaciones para las ecuaciones diferenciales que la constante de velocidad tiene un efecto negativo en la conctración de A. Al duplicar su valor, entonces estaremos disminuyendo también C A. Esto también se puede ver en el modelo Excel del Ejemplo 1. Vemos que la concentración original de A es 6.3 mol/L, entonces podemos duplicar el valor de la constante de velocidad, y vemos que la concentración de A desciende a 4.8 mol/L, que es lo que habíamos predicho que sucedería.
Referencias
- Bechette, B. Wayne. Modelado, análisis y simulación de dinámica de procesos, Nueva Jersey: Prentice Hall.
- Fogler, H. Scott. Los Elementos de la Ingeniería de Reacciones Químicas, Prentice Hall. ISBN 0-13-047394-4
- Kravaris, Costas. Control de Procesos Químicos: Un Enfoque en el Dominio del Tiempo, La Universidad de Michigan.
- Riggs, James B.; Karim, M. Nazmul. Control Químico y Bio-Process, Texas Tech University, Ferret Publishing.
Colaborador
Autores: Jason Bourgeois, Michael Kravchenko, Nicholas Parsons, Andrew Wang


