5.1: Efecto de la composición sobre el comportamiento de fase
- Page ID
- 81430
Tratemos de conciliar las gráficas P-T para la mezcla binaria con lo que sabemos de las gráficas P-T para sistemas de un solo componente. Al final del día, se forma una mezcla por componentes individuales que, al ser puros, actúan como se presenta en el diagrama P-T mostrado en la Fig. 3.1.1 [Módulo 3, repetido a continuación]. Por lo tanto, esperaríamos que el diagrama P-T de cada componente puro tenga algún tipo de influencia en el diagrama P-T de cualquier mezcla en la que se encuentre.
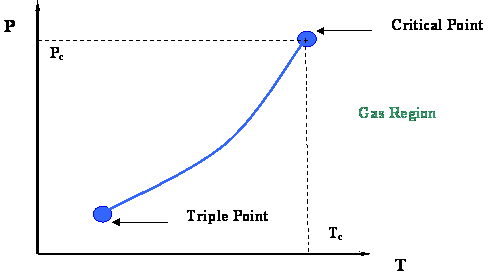
De hecho, sería razonable pensar que a medida que la presencia de un determinado componente A domina sobre B, la gráfica P-T de esa mezcla (A+B) debería acercarse cada vez más a la de A como componente puro.
Lo que esto nos está diciendo es que una nueva variable está entrando en el cuadro: la composición. Hasta el momento no hemos considerado la relación entre el componente A y el componente B en el sistema. Ahora vamos a estudiar cómo diferentes proporciones (composiciones) darán diferentes envolventes, es decir, diferentes comportamientos P-T.
Digamos que tenemos una mezcla de componentes A (Metano, CH 4) y B (Etanos, C 2 H 6), donde A es el más volátil de los dos. Es claro que para los dos componentes puros, tendríamos dos curvas de punto de ebullición para cada componente (A y B) como se muestra en la Figura 5.1.1.
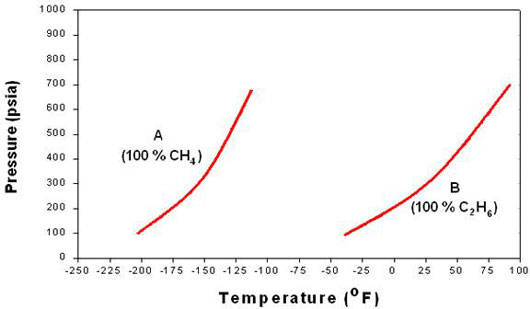
(Bloomer, O.T., Gami, D.C., Parent, J.D., “Propiedades Físico-Químicas de Mezclas de Metano-Etanos”. Copyright 1953, Instituto de Tecnología del Gas (ahora “Instituto de Tecnología del Gas”, en Chicago). Boletín de Investigación No. 17.)
Tenga en cuenta que la posición de cada una de las curvas con respecto a la otra depende de su volatilidad. Ya que estamos considerando que A es la más volátil, se espera que tenga mayores presiones de vapor a temperaturas más bajas, así, su curva se ubica hacia la izquierda. Para B, el componente menos volátil, tenemos una curva de punto de ebullición con menores presiones de vapor a temperaturas más altas. De ahí que la curva de punto de ebullición de B se encuentre hacia la derecha a presiones más bajas.
Ahora bien, si mezclamos A y B, la nueva envoltura de fase puede estar en cualquier lugar dentro de las curvas A y B. Esto se muestra en la Figura 5.1.2, donde se ilustra el efecto de la composición sobre el comportamiento de fase de la mezcla binaria Metano/ Etanos.
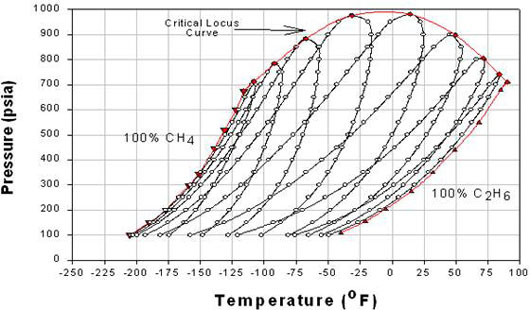
(Bloomer, O.T., Gami, D.C., Parent, J.D., “Propiedades Físico-Químicas de Mezclas de Metano-Etanos”. Copyright 1953, Instituto de Tecnología del Gas (ahora “Instituto de Tecnología del Gas”, en Chicago). Boletín de Investigación No. 17.)
En la Figura 5.1.2, cada envoltura de fase representa una composición diferente o una composición particular entre A y B (condiciones puras). Las envolventes de fase están delimitadas por la curva de presión de vapor de componente puro para el componente A (Metano) a la izquierda, la del componente B (etano) a la derecha y el lugar crítico (es decir, la curva que conecta los puntos críticos para las envolventes de fase individuales) en la parte superior. Obsérvese que cuando uno de los componentes es dominante, las curvas son características de sistemas de ebullición relativamente estrechos, mientras que las curvas para las que los componentes están presentes en cantidades comparables constituyen sistemas de ebullición relativamente amplia.
Observe que el rango de temperatura del lugar del punto crítico está limitado por la temperatura crítica de los componentes puros para mezclas binarias. Por lo tanto, ninguna mezcla binaria tiene una temperatura crítica, ya sea por debajo de la temperatura crítica del componente más ligero o por encima de la temperatura crítica del componente más pesado. Sin embargo, esto es cierto solo para temperaturas críticas; pero no para presiones críticas. Se puede encontrar que la presión crítica de una mezcla es mayor que las presiones críticas de ambos componentes puros, por lo tanto, vemos una forma cóncava para el lugar crítico. En general, cuanto más diferentes sean las dos sustancias, más lejos será el alcance ascendente del locus crítico. Cuando las sustancias que componen la mezcla son similares en complejidad molecular, la forma del locus crítico se aplana.


