14.4: Hidrólisis de las soluciones salinas
- Page ID
- 1913
Habilidades para desarrollar
- Predecir si una solución salina será ácida, básica o neutral
- Calcular las concentraciones de varias especies en una solución salina
- Describir el proceso que causa las soluciones de ciertos metales ser ácidas
Como hemos visto en la sección sobre reacciones químicas, cuando un ácido y una base se mezclan, experimentan una reacción de neutralización. La palabra "neutralización" parece implicar que una solución estequiométricamente equivalente de un ácido y una base sería neutral. Esto a veces es cierto, pero las sales que se forman en estas reacciones pueden tener propiedades ácidas o básicas propias, como veremos ahora.
Neutralización de ácido-base
Una solución es neutra cuando contiene concentraciones iguales de iones de hidronio e hidróxido. Cuando mezclamos soluciones conteniendo un ácido y una base, se produce una reacción de neutralización ácido-base. Sin embargo, incluso si mezclamos cantidades estequiométricamente equivalentes, podemos ver que la solución que resulta no es neutral. Podría contener un exceso de iones hidronio o un exceso de iones hidróxido porque las características de la sal formada determinan si la solución es ácida, neutra o básica. Las siguientes cuatro situaciones ilustran cómo pueden surgir soluciones con varios valores de pH después de una reacción de neutralización usando cantidades estequiométricamente equivalentes:
- Un ácido fuerte y una base fuerte, como HCl (aq) y NaOH (aq) reaccionarán para formar una solución neutra, ya que las pares conjugados producidos tienen una fuerza despreciable: \[\ce{HCl}(aq)+\ce{NaOH}(aq) ⇌ \ce{NaCl}(aq)+\ce{H2O}(l)\]
- Un ácido fuerte y una base débil producen una solución un poco ácida, no por el ácido fuerte involucrado, sino por el ácido conjugado de la base débil.
- Un ácido débil y una base fuerte producen una solución un poco básica. Una solución de un ácido débil reacciona con una solución de una base fuerte para formar la base conjugada del ácido débil y el ácido conjugado de la base fuerte. El ácido conjugado de la base fuerte es un ácido más débil que el agua y no tiene efecto sobre la acidez de la solución resultante. Sin embargo, la base conjugada del ácido débil es una base débil y se ioniza un poco en el agua. Esto aumenta la cantidad de ion hidróxido en la solución producida en la reacción y causa que la reacción sea un poco básica otra vez.
- Un ácido débil más una base débil puede producir una solución ácida, básica o neutra. Este es el más complejo de los cuatro tipos de reacciones. Cuando el ácido conjugado y la base conjugada son de fuerzas desiguales, la solución puede ser ácida o básica, dependiendo de las fuerzas relativas de los dos conjugados. Ocasionalmente, el ácido débil y la base débil tendrán la misma fuerza, por lo que su respectiva base conjugada y ácido tendrán la misma fuerza, y la solución será neutral. Para predecir si una combinación particular será ácida, básica o neutra, se deben comparar los valores de K tabulados de los conjugados.
Antiácidos estomacales
Nuestros estómagos contienen una solución de aproximadamente 0.03 M HCl, que nos ayuda a digerir los alimentos que comemos. La sensación de ardor asociada con la acidez estomacal es el resultado de la fuga de ácido del estómago a través de la válvula muscular en la parte superior del estómago hacia los tramos inferiores del esófago. El revestimiento del esófago no está protegido de los efectos corrosivos del ácido del estómago como lo está el revestimiento del estómago, y los resultados pueden ser muy dolorosos. Cuando tenemos acidez estomacal, se siente mejor si reducimos el exceso de ácido en el esófago tomando un antiácido. Como habrás adivinado, los antiácidos son bases. Uno de los antiácidos más comunes es el carbonato de calcio, CaCO3. La reacción,
\[CaCO_3(s)+2HCl(aq)⇌CaCl_2(aq)+H_2O(l)+CO_2(g)\]
no solo neutraliza el ácido del estómago, también produce CO2(g), lo que puede resultar en un eructo satisfactorio.
La leche de magnesia es una suspensión de la base de hidróxido de magnesio escasamente soluble, Mg(OH)2. Funciona de acuerdo con la reacción:
\[Mg(OH)_2(s)⇌Mg^{2+}(aq)+2OH^-(aq)\]
Los iones de hidróxido generados en este equilibrio luego reaccionan con los iones de hidronio del ácido del estómago, de modo que:
\[H_3O^+ + OH^- ⇌ 2H_2O(l)\]
Esta reacción no produce dióxido de carbono, pero los antiácidos que contienen magnesio pueden tener un efecto laxante. Varios antiácidos tienen hidróxido de aluminio, Al(OH)3, como un ingrediente activo. El hidróxido de aluminio tiende a causar estreñimiento, y algunos antiácidos con hidróxido de aluminio junto con hidróxido de magnesio para equilibrar los efectos secundarios de las dos sustancias.
Aspectos culinarios de la química
Cocinar es esencialmente una química sintética que resulta segura para comer. Hay varios ejemplos de química ácido-base en el mundo culinario. Un ejemplo es el uso de bicarbonato de sodio o bicarbonato de sodio en la cocción. NaHCO3 es una base. Cuando reacciona con un ácido como el jugo de limón, suero de leche o crema agria en una masa, se forman burbujas de dióxido de carbono a partir de la descomposición del ácido carbónico resultante, y la masa "se eleva". El polvo para hornear es una combinación de bicarbonato de sodio y una o más sales ácidas que reaccionan cuando los dos químicos entran en contacto con el agua en la masa.
A muchas personas les gusta agregar jugo de limón, vinagre, o ambos ácidos en el pescado cocido (Figura \(\PageIndex{1}\)). Resulta que los peces tienen aminas (bases) volátiles en sus sistemas, que son neutralizados por los ácidos para producir sales de amonio no volátiles. Esto reduce el olor del pescado y también agrega un sabor "agrio" que parece que disfrutamos.

La conservación en vinagre es un método utilizado para preservar vegetales usando un ambiente ácido producido naturalmente. El vegetal, como un pepino, se coloca en un frasco sellado sumergido en una solución de salmuera. La solución de salmuera favorece el crecimiento de bacterias beneficiosas y suprime el crecimiento de bacterias dañinas. Las bacterias beneficiosas se alimentan de almidones en el pepino y producen ácido láctico como producto de desecho en un proceso llamado la fermentación. El ácido láctico eventualmente aumenta la acidez de la salmuera a un nivel que mata cualquier bacteria dañina, que requiere un ambiente básico. Sin las bacterias dañinas que consumen los pepinos, pueden durar mucho más tiempo que si no estuvieran protegidos. Un subproducto del proceso de la conservación en vinagre cambia el sabor de las verduras con el ácido, lo que hace que tengan un sabor agrio.
Sales de bases débiles y ácidos fuertes
Cuando neutralizamos una base débil con un ácido fuerte, el producto es una sal que contiene el ácido conjugado de la base débil. Este ácido conjugado es un ácido débil. Por ejemplo, el cloruro de amonio, NH4Cl, es una sal formada por la reacción del amoníaco de base débil con el ácido fuerte HCl:
\[\ce{NH3}(aq)+\ce{HCl}(aq)⟶\ce{NH4Cl}(aq)\]
Una solución de esta sal contiene iones de amonio e iones de cloruro. El ion cloruro no tiene efecto en la acidez de la solución porque el HCl es un ácido fuerte. El cloruro es una base muy débil y no aceptará un protón en una medida medible. Sin embargo, el ion amonio, el ácido conjugado del amoníaco, reacciona con el agua y aumenta la concentración de iones hidronio:
\[\ce{NH4+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{NH3}(aq)\]
La ecuación de equilibrio para esta reacción es simplemente la constante de ionización, Ka, para el ácido \(\ce{NH4+}\):
\[\ce{\dfrac{[H3O+][NH3]}{[NH4+]}}=K_\ce{a}\]
No encontraremos un valor de Ka para el ion amonio en Tabla E1. Sin embargo, no es difícil determinar Ka para \(\ce{NH4+}\) a partir del valor de la constante de ionización del agua, Kw y Kb, la constante de ionización de su base conjugada, NH3, utilizando la siguiente relación:
\[K_\ce{w}=K_\ce{a}×K_\ce{b}\]
Esta relación es válida para cualquier base y su ácido conjugado o para cualquier ácido y su base conjugada.
Ejemplo \(\PageIndex{1}\): pH de una solución de una sal de una base débil y un ácido fuerte
La anilina es una amina que se usa para fabricar tintes. Se aísla como el clorhidrato de anilina, \(\ce{[C6H5NH3+]Cl}\), una sal preparada por reacción de la base débil anilina y el ácido clorhídrico. ¿Cuál es el pH de una solución de clorhidrato de anilina 0.233 M?
\[\ce{C6H5NH3+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{C6H5NH2}(aq)\]
Solución
El nuevo paso en este ejemplo es determinar Ka para el ion \(\ce{C6H5NH3+}\). El ion \(\ce{C6H5NH3+}\) es el ácido conjugado de una base débil. El valor de Ka para este ácido se ve en la Tabla E1, pero podemos determinarlo a partir del valor de Kb para la anilina, C6H5NH2, que se da como 4.6 × 10−10:
\[\mathrm{\mathit{K}_a(for\:C_6H_5NH_3^+)×\mathit{K}_b(for\:C_6H_5NH_2)=\mathit{K}_w=1.0×10^{−14}}\]
\[\mathrm{\mathit{K}_a(for\:C_6H_5NH_3^+)=\dfrac{\mathit{K}_w}{\mathit{K}_b(for\:C_6H_5NH_2)}=\dfrac{1.0×10^{−14}}{4.6×10^{−10}}=2.3×10^{−5}}\]
Ahora tenemos la constante de ionización y la concentración inicial del ácido débil, la información necesaria para determinar la concentración de equilibrio de H3O+ y el pH:
Con estos pasos encontramos que [H3O+] = 2.3 × 10−3 M y pH = 2.64
Ejercicio \(\PageIndex{1}\)
- Haga los cálculos y demuestre que la concentración de los iones hidronio para una solución 0.233-M de \(\ce{C6H5NH3+}\) es 2.3 × 10−3 y el pH es 2.64.
- ¿Cuál es la concentración de los iones hidronio en una solución 0.100-M de nitrato de amonio, NH4NO3, una sal compuesta de iones \(\ce{NH4+}\) y \(\ce{NO3-}\). Use los datos en Tabla E1 para determinar Kb para el ion amonio. ¿Cuál es el ácido mas fuerte \(\ce{C6H5NH3+}\) o \(\ce{NH4+}\)?
- Respuesta a
-
\(K_a\ce{(for\:NH4+)}=5.6×10^{−10}\), [H3O+] = 7.5 × 10−6 M
- Respuesta b
-
\(\ce{C6H5NH3+}\) es el ácido mas fuerte (a)(b) .
Sales de ácidos débiles y bases fuertes
Cuando neutralizamos un ácido débil con una base fuerte, obtenemos una sal que contiene la base conjugada del ácido débil. Esta base conjugada suele ser una base débil. Por ejemplo, el acetato de sodio, NaCH3CO2, es una sal formada por la reacción del ácido acético ácido débil con la base fuerte hidróxido de sodio:
\[ce{CH3CO2H}(aq)+\ce{NaOH}(aq)⟶\ce{NaCH3CO2}(aq)+\ce{H2O}(aq)\]
Una solución de esta sal contiene iones de sodio e iones de acetato. El ion sodio no tiene efecto sobre la acidez de la solución. Sin embargo, el ion acetato, la base conjugada del ácido acético, reacciona con el agua y aumenta la concentración de ion hidróxido:
\[ce{CH3CO2-}(aq)+\ce{H2O}(l)⇌\ce{CH3CO2H}(aq)+\ce{OH-}(aq)\]
La ecuación de equilibrio para esta reacción es la constante de ionización, Kb, para la base \(\ce{CH3CO2-}\). El valor de Kb se puede calcular a partir del valor de la constante de ionización del agua, Kw y Ka, la constante de ionización del ácido conjugado del anión usando la ecuación:
\[_\ce{w}=K_\ce{a}×K_\ce{b}\]
Para el ion acetato y su ácido conjugado tenemos:
\[\mathrm{\mathit{K}_b(for\:\ce{CH_3CO_2^-})=\dfrac{\mathit{K}_w}{\mathit{K}_a(for\:CH_3CO_2H)}=\dfrac{1.0×10^{−14}}{1.8×10^{−5}}=5.6×10^{−10}}\]
Algunos manuales no informan valores de Kb. Solo reportan constantes de ionización para los ácidos. Si queremos determinar un valor de Kb usando uno de estos manuales, debemos buscar el valor de Ka para el ácido conjugado y convertirlo en un valor de Kb.
Ejemplo \(\PageIndex{2}\): Equilibrio de una sal de un ácido débil y una base fuerte
Determine la concentración del ácido acético en una solución con \(\ce{[CH3CO2- ]}=0.050\:M\) y [OH−] = 2.5 × 10−6 M a equilibrio. La reacción es:
\[\ce{CH3CO2-}(aq)+\ce{H2O}(l)⇌\ce{CH3CO2H}(aq)+\ce{OH-}(aq)\]
Solución
Se nos dan dos de las tres concentraciones de equilibrio y se nos pide encontrar la concentración que falta. Si podemos encontrar la constante de equilibrio para la reacción, el proceso es sencillo.
El ion acetato se comporta como una base en esta reacción; los iones de hidróxido son un producto. Determinamos Kb de la siguiente manera:
\[\mathrm{\mathit{K}_b(for\:\ce{CH_3CO_2^-})=\dfrac{\mathit{K}_w}{\mathit{K}_a(for\:CH_3CO_2H)}=\dfrac{1.0×10^{−14}}{1.8×10^{−5}}=5.6×10^{−10}}\]
Ahora encuentre la concentración que falta:
\[K_\ce{b}=\ce{\dfrac{[CH3CO2H][OH- ]}{[CH3CO2- ]}}=5.6×10^{−10}\]
\[=\dfrac{[\ce{CH3CO2H}](2.5×10^{−6})}{(0.050)}=5.6×10^{−10}\]
Resolviendo esta ecuación nos da [CH3CO2H] = 1.1 × 10−5 M.
Ejercicio \(\PageIndex{2}\)
¿Cuál es el pH de una solución de CN- 0.083-M? Use 4.9 × 10−10 como la constante Ka para HCN. Sugerencia: Probablemente necesitemos convertir pOH a pH o encontrar [H3O+] usando [OH−] en las etapas finales de este problema.
- Respuesta
-
11.16
Equilibrio en una solución de una sal de un ácido débil y una base débil
En una solución de una sal formada por la reacción de un ácido débil y una base débil, para predecir el pH, debemos saber tanto el Ka del ácido débil como el Kb de la base débil. Si Ka> Kb, la solución es ácida, y si Kb> Ka, la solución es básica.
Ejemplo \(\PageIndex{3}\): Determinación de las características ácidas o básicas de las sales
Determine si una solución acuosa de las siguientes sales es ácidas, básicas, o neutras:
- KBr
- NaHCO3
- NH4Cl
- Na2HPO4
- NH4F
Solución
Considere cada uno de los iones separadamente en términos de su efecto sobre el pH de la solución, como se muestra aquí:
- El catión K+ y el anión Br− son espectadores, ya que son el catión de una base fuerte (KOH) y el anión de un ácido fuerte (HBr), respectivamente. La solución es neutral.
- El catión Na+ es un espectador y no afectará el pH de la solución; el anión \(\ce{HCO3-}\) es anfiprótico. El Ka de \(\ce{HCO3-}\) es 4.7 × 10−11, por lo que el Kb de su base conjugada es \(\dfrac{1.0 × 10^{-14}}{4.7 × 10^{-11}} = 2.1 × 10 ^{-4}\). Ya que Kb >> Ka, la solución es básica.
- El ion \(\ce{NH4+}\) es ácido y el ion Cl- es un espectador. La solución será ácida.
- El ion Na+ es un espectador y no afectará el pH de la solución, mientras que el ion \(\ce{HPO4^{2-}}\) es anfibrótico. El Ka de \(\ce{HPO_4^{2-}}\) es 4.2 × 10−13 y su Kb es \(\dfrac{1.0×10^{-14}}{4.2×10^{-13}}=2.4×10^{-2}\). Porque Kb >> Ka, la solución es básica.
- El ion \(\ce{NH4+}\) está listado como un ácido, y el ion F está listado como una base, por lo que debemos comparar directamente el Ka y el Kb de los dos iones. Ka de \(\ce{NH4+}\) es 5.6 × 10−10, lo que parece muy pequeño, pero el Kb de F− es 1.4 × 10−11, por lo que la solución es ácida, ya que Ka > Kb.
Ejercicio \(\PageIndex{3}\)
Determine si las soluciones acuosas de las siguientes sales son ácidas, básicas o neutras:
- K2CO3
- CaCl2
- KH2PO4
- (NH4)2CO3
- AlBr3
- Respuesta a
-
básica
- Respuesta b
-
neutra
- Respuesta c
-
ácida
- Respuesta d
-
básica
- Respuesta e
-
ácida
La ionización de los iones metálicos hidratados
Si medimos el pH de las soluciones de una variedad de iones metálicos, encontraremos que estos iones actúan como ácidos débiles cuando están en solución. El ion de aluminio es un ejemplo. Cuando el nitrato de aluminio se disuelve en el agua, el ion de aluminio reacciona con el agua para dar un ion de aluminio hidratado, \(\ce{Al(H2O)6^3+}\), disuelto en el agua a granel. Lo que esto significa es que el ion de aluminio tiene las interacciones más fuertes con las seis moléculas de agua más cercanas (la llamada primera capa de solvatación), a pesar de que interactúa con las otras moléculas de agua que rodean esta \(\ce{Al(H2O)6^3+}\) grupo también:
\[\ce{Al(NO3)3}(s)+\ce{6H2O}(l)⟶\ce{Al(H2O)6^3+}(aq)+\ce{3NO3-}(aq)\]
Con frecuencia vemos la fórmula de este ion simplemente como "Al3+(aq)", sin notando explícitamente las seis moléculas de agua que son las más cercanas al ion de aluminio y simplemente describiendo el ion como solvatado en el agua (hidratado). Esto es similar a la simplificación de la fórmula del ion hidronio, H3O+ a H+. Sin embargo, en este caso, el ion de aluminio hidratado es un ácido débil (Figura \(\PageIndex{2}\)) y dona un protón a una molécula de agua. Por lo tanto, la hidratación se vuelve importante y podemos usar fórmulas que muestran el grado de hidratación:
\[\ce{Al(H2O)6^3+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Al(H2O)5(OH)^2+}(aq) \hspace{20px} K_\ce{a}=1.4×10^{−5}\]
Al igual que con otros ácidos polipróticos, el ion de aluminio hidratado se ioniza en etapas, como se muestra aquí:
\[\ce{Al(H2O)6^3+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Al(H2O)5(OH)^2+}(aq)\]
\[\ce{Al(H2O)5(OH)^2+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Al(H2O)4(OH)2+}(aq)\]
\[\ce{Al(H2O)4(OH)2+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Al(H2O)3(OH)3}(aq)\]
Tenga en cuenta que algunas de estas especies de aluminio exhiben un comportamiento anfibrótico, ya que actúan como ácidos cuando aparecen en el lado izquierdo de las expresiones de equilibrio y como bases cuando aparecen en el lado derecho.
![A reaction is shown using ball and stick models. On the left, inside brackets with a superscript of 3 plus outside to the right is structure labeled “[ A l ( H subscript 2 O ) subscript 6 ] superscript 3 plus.” Inside the brackets is s central grey atom to which 6 red atoms are bonded in an arrangement that distributes them evenly about the central grey atom. Each red atom has two smaller white atoms attached in a forked or bent arrangement. Outside the brackets to the right is a space-filling model that includes a red central sphere with two smaller white spheres attached in a bent arrangement. Beneath this structure is the label “H subscript 2 O.” A double sided arrow follows. Another set of brackets follows to the right of the arrows which have a superscript of two plus outside to the right. The structure inside the brackets is similar to that on the left, except a white atom is removed from the structure. The label below is also changed to “[ A l ( H subscript 2 O ) subscript 5 O H ] superscript 2 plus.” To the right of this structure and outside the brackets is a space filling model with a central red sphere to which 3 smaller white spheres are attached. This structure is labeled “H subscript 3 O superscript plus.”](https://espanol.libretexts.org/@api/deki/files/9343/CNX_Chem_14_04_hydronium.jpg?revision=1&size=bestfit&width=594&height=202)
Sin embargo, la ionización de un catión que tiene más de una carga generalmente no es extensa más allá de la primera etapa. Ejemplos adicionales de la primera etapa de la ionización de los iones metálicos hidratados son:
\[\ce{Fe(H2O)6^3+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Fe(H2O)5(OH)^2+}(aq) \hspace{20px} K_\ce{a}=2.74\]
\[\ce{Cu(H2O)6^2+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Cu(H2O)5(OH)+}(aq) \hspace{20px} K_\ce{a}=~6.3\]
\[\ce{Zn(H2O)4^2+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Zn(H2O)3(OH)+}(aq) \hspace{20px} K_\ce{a}=9.6\]
Ejemplo \(\PageIndex{4}\): Hidrólisis de [Al(H2O)6]3+
Calcule el pH de una solución de cloruro de aluminio 0.10-M, que se disuelve completamente para hacer el ion de aluminio hidratado \(\ce{[Al(H2O)6]^3+}\) en la solución.
Solución
A pesar de la apariencia inusual del ácido, este es un problema típico de la ionización de los ácidos.
![A reaction is shown using ball and stick models. On the left, inside brackets with a superscript of 3 plus outside to the right is structure labeled “[ A l ( H subscript 2 O ) subscript 6 ] superscript 3 plus.” Inside the brackets is s central grey atom to which 6 red atoms are bonded in an arrangement that distributes them evenly about the central grey atom. Each red atom has two smaller white atoms attached in a forked or bent arrangement. Outside the brackets to the right is a space-filling model that includes a red central sphere with two smaller white spheres attached in a bent arrangement. Beneath this structure is the label “H subscript 2 O.” A double sided arrow follows. Another set of brackets follows to the right of the arrows which have a superscript of two plus outside to the right. The structure inside the brackets is similar to that on the left, except a white atom is removed from the structure. The label below is also changed to “[ A l ( H subscript 2 O ) subscript 5 O H ] superscript 2 plus.” To the right of this structure and outside the brackets is a space filling model with a central red sphere to which 3 smaller white spheres are attached. This structure is labeled “H subscript 3 O superscript plus.”](https://espanol.libretexts.org/@api/deki/files/9341/CNX_Chem_14_04_steps2_img.jpg?revision=1)
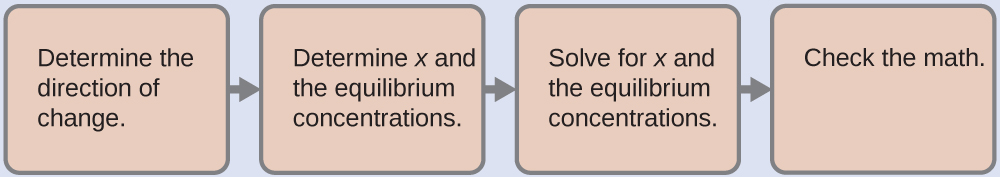
- Determine la dirección del cambio. La ecuación para la reacción y Ka son:
\(\ce{Al(H2O)6^3+}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{Al(H2O)5(OH)^2+}(aq) \hspace{20px} K_\ce{a}=1.4×10^{−5}\)
: 
3. Resuelve para x y las concentraciones de equilibrio. Sustituyendo las expresiones para las concentraciones de equilibrio en la ecuación para la constante de ionización nos da:
\[K_\ce{a}=\ce{\dfrac{[H3O+][Al(H2O)5(OH)^2+]}{[Al(H2O)6^3+]}}\]
\(=\dfrac{(x)(x)}{0.10−x}=1.4 \times 10^{−5}\)
Resolviendo esta ecuación nos da:
\[x=1.2×10^{−3}\:M\]
De esto encontramos:
\[\ce{[H3O+]}=0+x=1.2×10^{−3}\:M\]
\[\mathrm{pH=−log[H_3O^+]=2.92(an\: acidic\: solution)}\]
4.Verifique su trabajo. La aritmética es correcta; cuando 1.2 × 10−3 M se sustituye por x, el resultado = Ka.
Ejercicio \(\PageIndex{4}\)
¿Qué es \(\ce{[Al(H2O)5(OH)^2+]}\) en una solución de 0.15-M Al(NO3)3 que contiene suficiente ácido fuerte HNO3 para llevar [H3O+] a 0.10 M?
- Respuesta
-
2.1 × 10−5 M
Las constantes para las diferentes etapas de ionización no se saben para muchos iones metálicos, por lo que no podemos calcular el grado de su ionización. Sin embargo, prácticamente todos los iones metálicos hidratados distintos de los metales alcalinos se ionizan para hacer soluciones ácidas. La ionización aumenta a medida que aumenta la carga del ion metálico o disminuye el tamaño del ion metálico.
Resumen
Las propiedades características de las soluciones acuosas de los ácidos de Brønsted-Lowry se deben a la presencia de los iones hidronio; los de las soluciones acuosas de bases Brønsted-Lowry se deben a la presencia de los iones hidróxido. La neutralización que ocurre cuando se combinan las soluciones acuosas de los ácidos y las bases resulta de la reacción de los iones hidronio e hidróxido para formar el agua. Algunas sales formadas en las reacciones de neutralización pueden causar que las soluciones del producto sean un poco ácidas o un poco básicas. Las soluciones que contienen sales o iones metálicos hidratados tienen un pH determinado por el grado de hidrólisis de los iones en la solución. El pH de las soluciones se puede calcular utilizando técnicas de equilibrio familiares, o se puede determinar cualitativamente que es ácido, básico o neutro, dependiendo del Ka y Kb relativo de los iones involucrados.
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


