14.5: Ácidos polipróticos
- Page ID
- 1914
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Habilidades para desarrollar
- Extender conceptos de equilibrio introducidos previamente a los ácidos y las bases que pueden donar o aceptar más de un protón.
Podemos clasificar los ácidos por el número de protones por molécula que pueden ceder en una reacción. Los ácidos como \(\ce{HCl}\), \(\ce{HNO3}\) y \(\ce{HCN}\) que contienen un átomo de hidrógeno ionizable en cada molécula se llaman los ácidos monopróticos. Sus reacciones con el agua son:
\[\ce{HCl}(aq)+\ce{H2O}(l)⟶\ce{H3O+}(aq)+\ce{Cl-}(aq)\]
\[\ce{HNO3}(aq)+\ce{H2O}(l)⟶\ce{H3O+}(aq)+\ce{NO3-}(aq)\]
\[\ce{HCN}(aq)+\ce{H2O}(l)⟶\ce{H3O+}(aq)+\ce{CN-}(aq)\]
Aunque contiene cuatro átomos de hidrógeno, el ácido acético, \(\ce{CH3CO2H}\), también es monoprótico porque solo el átomo de hidrógeno del grupo carboxilo (\(\ce{-COOH}\)) reacciona con la base:
Del mismo modo, las bases monopróticas son bases que aceptarán un solo protón.
Ácidos dipróticos
Los ácidos dipróticos contienen dos átomos de hidrógeno ionizables por molécula; la ionización de tales ácidos ocurre en dos pasos. La primera ionización siempre tiene lugar en mayor medida que la segunda ionización. Por ejemplo, el ácido sulfúrico, un ácido fuerte, se ioniza de la siguiente manera:
- La primera ionización es
\[ \ce{H2SO4}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HSO4-}(aq)\]
con \(K_{\ce a1} > 10^2;\: {complete\: dissociation}\).
- La segunda ionización es
\[ \ce{HSO4-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{SO4^{2−}}(aq)\]
con \( K_{\ce a2}=1.2×10^{−2}\).
Este proceso de ionización gradual se produce para todos los ácidos polipróticos. Cuando hacemos una solución de un ácido diprótico débil, obtenemos una solución que contiene una mezcla de ácidos. El ácido carbónico, \(\ce{H2CO3}\), es un ejemplo de un ácido diprótico débil. La primera ionización del ácido carbónico produce iones de hidronio e iones de bicarbonato en pequeñas cantidades.
- La primera ionización
\[\ce{H2CO3}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO3-}(aq)\]
con
\[K_{\ce{H2CO3}}=\ce{\dfrac{[H3O+][HCO3- ]}{[H2CO3]}}=4.3×10^{−7}\]
El ion bicarbonato también puede actuar como un ácido. Se ioniza y forma iones hidronio e iones carbonato en cantidades hasta más pequeñas.
- La segunda ionización
\[\ce{HCO3-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CO3^2-}(aq)\]
con
\[ K_{\ce{HCO3-}}=\ce{\dfrac{[H3O+][CO3^2- ]}{[HCO3- ]}}=4.7×10^{−11}\]
\(K_{\ce{H2CO3}}\) es mas grande de \(K_{\ce{HCO3-}}\) por un factor de 104, entonces H2CO3 es el productor dominante del ion hidronio en la solución. Esto significa que solo un poco de \(\ce{HCO3-}\) formado por la ionización de H2CO3 se ioniza para producir iones de hidronio (y iones de carbonato), y las concentraciones de H3O+ y \(\ce{HCO3-}\) son prácticamente igual en una solución acuosa pura de H2CO3.
Si la primera constante de ionización de un ácido diprótico débil es más grande que la segunda en un factor de al menos 20, es apropiado tratar la primera ionización separadamente y calcular las concentraciones resultantes de ella antes de calcular las concentraciones de especies resultantes de la ionización posterior. Esto puede simplificar nuestro trabajo considerablemente porque podemos determinar la concentración de H3O+ y la base conjugada de la primera ionización, luego determinar la concentración de la base conjugada de la segunda ionización en una solución con concentraciones determinadas por la primera ionización.
Ejemplo \(\PageIndex{1}\): Ionización de un ácido diprótico
Cuando compramos el agua de soda (el agua carbonatada), estamos comprando una solución de dióxido de carbono en el agua. La solución es ácida porque el CO2 reacciona con el agua para formar el ácido carbónico, H2CO3. ¿Qué son \(\ce{[H3O+]}\), \(\ce{[HCO3-]}\) y \(\ce{[CO3^2-]}\) en una solución saturada de CO2 con un inicial [H2CO3] = 0.033 M?
\[\ce{H2CO3}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO3-}(aq) \hspace{20px} K_{\ce a1}=4.3×10^{−7} \label{step1} \tag{equilibrium step 1}\]
\[\ce{HCO3-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CO3^2-}(aq) \hspace{20px} K_{\ce a2}=4.7×10^{−11} \label{step2} \tag{equilibrium step 2}\]
Solución
Como se indicó por las constantes de ionización, H2CO3 es un ácido mucho más fuerte que \(\ce{HCO3-}\), entonces \(\ce{H2CO3}\) es el productor dominante del ion de hidronio en la solución. Así, hay dos pasos para resolver este problema:
1. Utilizando los cuatro pasos habituales, determinamos la concentración de H3O+ y \(\ce{HCO3-}\) producido por la ionización de H2CO3.
2. Luego, determinamos la concentración de \(\ce{CO3^2-}\) en una solución con la concentración de H3O+ y \(\ce{HCO3-}\) determinado en paso (1).
Para resumir:
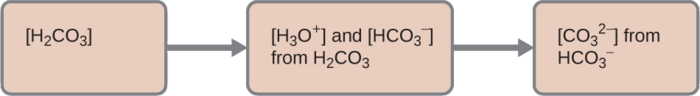
1. La primera ionización: Determinamos las concentraciones de \(\ce{H3O+}\) y \(\ce{HCO3-}\).
Ya que \ref{step1} tiene una \(K_{a1}=4.3×10^{−7}\) mucho más grande que \(K_{a2}=4.7×10^{−11}\) para \ref{step2}, podemos ignorar con confianza el segundo paso de ionización y podemos poner atención solo en el primer paso (pero abordarlo en la siguiente parte del problema).
\[\ce{H2CO3}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO3-}(aq) \hspace{20px} K_{\ce a1}=4.3×10^{−7} \nonumber\]
En cuanto a la ionización de cualquier otro ácido débil:
Una tabla abreviada de cambios y concentraciones muestra:
| Tabla ICE | \(\ce{H2CO3}(aq)\) | \(\ce{H2O}(l)\) | \( \ce{H3O+}(aq) \) | \(\ce{HCO3-}(aq)\) |
|---|---|---|---|---|
| Inicial (M) | \(0.033 \:M\) | - | \(0\) | \(0\) |
| Cambio (M) | \(- x\) | - | \(+x\) | \(+x\) |
| Equilibrio (M) | \(0.033 \:M - x\) | - | \(x\) | \( x\) |
Sustituyendo las concentraciones de equilibrio en la constante de equilibrio nos da:
\[K_{\ce{H2CO3}}=\ce{\dfrac{[H3O+][HCO3- ]}{[H2CO3]}}=\dfrac{(x)(x)}{0.033−x}=4.3×10^{−7} \nonumber\]
Resolviendo la ecuación anterior haciendo nuestras suposiciones estándar nos da:
\[x=1.2×10^{−4} \nonumber\]
Así:
\[\ce{[H2CO3]}=0.033\:M \nonumber\]
\[\ce{[H3O+]}=\ce{[HCO3- ]}=1.2×10^{−4}\:M \nonumber\]
2. La segunda ionización: Determine la concentración de \(CO_3^{2-}\) en una solución a equilibrio.
Ya que \ref{step1} tiene una \(K_a\) mucho más grande que \ref{step2}, podemos calcular las condiciones de equilibrio calculadas a partir de la primera parte del ejemplo como condiciones iniciales para una tabla ICER para \ref {step2}:
\[\ce{HCO3-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CO3^2-}(aq) \nonumber\]
| Tabla ICE | \(\ce{HCO3-}(aq)\) | \(\ce{H2O}(l)\) | \( \ce{H3O+}(aq) \) | \(\ce{CO3^2-}(aq)\) |
|---|---|---|---|---|
| Inicial (M) | \(1.2×10^{−4}\:M\) | - | \(1.2×10^{−4}\:M\) | \(0\) |
| Cambio (M) | \(- y\) | - | \(+y\) | \(+y\) |
| Equilibrio (M) | \(1.2×10^{−4}\:M - y\) | - | \(1.2×10^{−4}\:M + y\) | \( y\) |
\[ \begin{align*} K_{\ce{HCO3-}}&=\ce{\dfrac{[H3O+][CO3^2- ]}{[HCO3- ]}} \\[5pt] &=\dfrac{(1.2×10^{−4}\:M + y) (y)}{(1.2×10^{−4}\:M - y)} \end{align*}\]
Para evitar resolver una ecuación cuadrática, podemos suponer \(y \ll 1.2×10^{−4}\:M \) entonces
\[K_{\ce{HCO3-}} = 4.7×10^{−11} \approx \dfrac{(1.2×10^{−4}\:M ) (y)}{(1.2×10^{−4}\:M)} \nonumber\]
Reorganice para resolver para \(y\)
\[y \approx \dfrac{ (4.7×10^{−11})(1.2×10^{−4}\:M )}{ 1.2×10^{−4}\:M} \nonumber\]
\[[\ce{CO3^2-}]=y \approx 4.7×10^{−11} \nonumber\]
Para resumir:
En la primera parte de este ejemplo, encontramos que el \(\ce{H2CO3}\) en una solución 0.033-M se ioniza un poco y en equilibrio \([\ce{H2CO3}] = 0.033 \,M\), \( [\ce{H3O^{+}}] = 1.2×10^{-4}\), y \(\ce{[HCO3-]} = 1.2×10^{-4}\:M\). En la segunda parte del ejemplo, determinamos que \(\ce{[CO3^2-]} = 5.6×10^{-11}\:M\).
Ejercicio \(\PageIndex{2}\): El sulfuro de hidrógeno
La concentración de \(H_2S\) en una solución acuosa saturada a temperatura ambiente es de aproximadamente 0.1 M. Calcule \(\ce{[H3O+]}\), \(\ce{[HS^{-}]}\), y \(\ce{[S^{2-}]}\) en la solución:
\[\ce{H2S}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HS-}(aq) \hspace{20px} K_{\ce a1}=8.9×10^{−8} \nonumber\]
\[\ce{HS-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{S^2-}(aq) \hspace{20px} K_{\ce a2}=1.0×10^{−19} \nonumber\]
- Respuesta:
-
\([\ce{H2S}] = 0.1 M\), \(\ce{[H3O+]} = [HS^{−}] = 0.0001\, M\), \([S^{2−}] = 1 × 10^{−19}\, M\)
Notamos que la concentración del ion sulfuro es la misma que Ka2. Esto se debe al hecho de que cada disociación posterior ocurre en menor grado (a medida que el ácido se hace más débil).
El ácido triprótico
Un ácido triprótico es un ácido que tiene tres protones disociables que experimentan una ionización gradual: el ácido fosfórico es un ejemplo típico:
- La primera ionización es
\[\ce{H3PO4}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{H2PO4-}(aq) \]
con \(K_{\ce a1}=7.5×10^{−3} \).
- La segunda ionización es
\[\ce{H2PO4-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HPO4^2-}(aq)\]
con \( K_{\ce a2}=6.2×10^{−8} \).
- La tercera ionización es
\[\ce{HPO4^2-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{PO4^3-}(aq) \]
con \( K_{\ce a3}=4.2×10^{−13} \).
Al igual que con los ácidos dipróticos, las diferencias en las constantes de ionización de estas reacciones nos dicen que en cada paso sucesivo el grado de ionización es significativamente más débil. Esta es una característica general de los ácidos polipróticos y las constantes de ionización sucesivas a veces difieren en un factor de aproximadamente 105 a 106. Puede parecer que este conjunto de tres reacciones de disociación complica los cálculos de las concentraciones de equilibrio en una solución de H3PO4. Sin embargo, debido a que las constantes de ionización sucesivas difieren en un factor de 105 a 106, los cálculos se pueden dividir en una serie de partes similares a las de los ácidos dipróticos.
Las bases polipróticas pueden aceptar más de un ion de hidrógeno en solución. El ion de carbonato es un ejemplo de una base diprótica, ya que puede aceptar hasta dos protones. Las soluciones de carbonatos de metales alcalinos son bastante alcalinas, debido a las reacciones:
\[\ce{H2O}(l)+\ce{CO3^2-}(aq)⇌\ce{HCO3-}(aq)+\ce{OH-}(aq) \]
y
\[\ce{H2O}(l)+\ce{HCO3-}(aq)⇌\ce{H2CO3}(aq)+\ce{OH-}(aq)\]
Resumen
Un ácido que contiene más de un protón ionizable es un ácido poliprótico. Los protones de estos ácidos se ionizan en pasos. Las diferencias en las constantes de ionización ácida para las ionizaciones sucesivas de los protones en un ácido poliprótico generalmente varían en aproximadamente cinco órdenes de magnitud. Mientras la diferencia entre los valores sucesivos de Ka del ácido sea mayor que aproximadamente un factor de 20, es apropiado dividir los cálculos de las concentraciones de los iones en solución en una serie de pasos.
Glosario
- ácido diprótico
- ácido que contiene dos átomos de hidrógeno ionizables por molécula. Un ácido diprótico se ioniza en dos pasos
- base diprótica
- base capaz de aceptar dos protones. Los protones son aceptados en dos pasos.
- ácido monoprótico
- ácido que contiene un átomo de hidrógeno ionizable por molécula
- ionización gradual
- proceso en el que un ácido se ioniza al perder protones secuencialmente
- ácido triprótico
- ácido que contiene tres átomos de hidrógeno ionizables por molécula; la ionización de los ácidos tripróticos ocurre en tres pasos.
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


