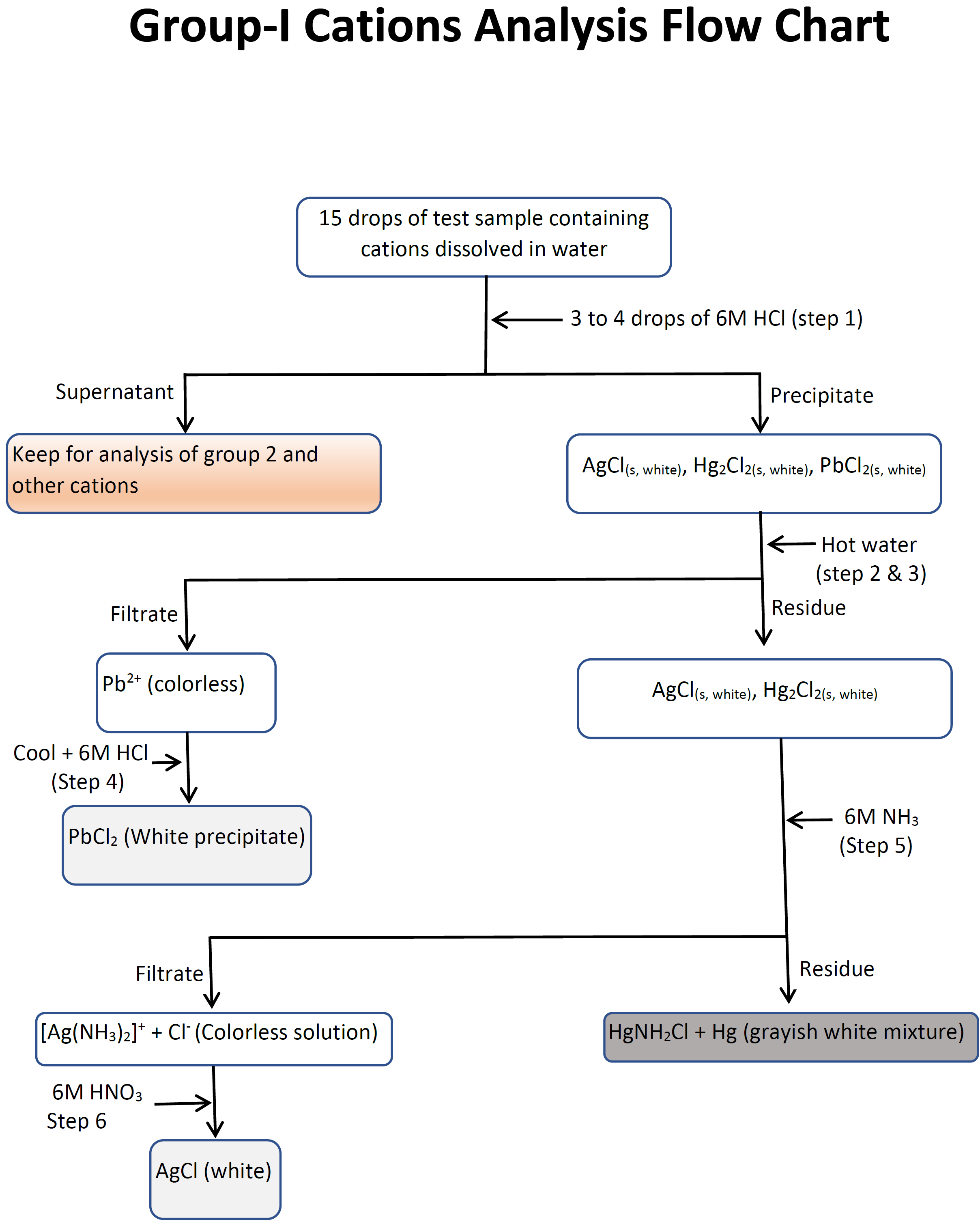
3.3: Procedimiento, diagrama de flujo y hojas de datos para la separación y confirmación de cationes del grupo I
- Page ID
- 76248
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \) \( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)\(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\) \(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\)\(\newcommand{\AA}{\unicode[.8,0]{x212B}}\)
|
Químico |
Peligro |
|---|---|
|
Nitrato de plomo (II) 0.1M en ácido nítrico 0.1M |
Tóxico, irritante y oxidante |
|
Nitrato de mercurio (I) 0.1M en ácido nítrico 0.1M |
Altamente tóxico y oxidante |
|
Nitrato de plata 0.1M en ácido nítrico 0.1M |
Tóxico, corrosivo y oxidante |
- *Los peligros de amoníaco 6M, ácido clorhídrico 6M y ácido nítrico 6M se enumeran en una tabla de reactivos común en el capítulo 2.
- Las soluciones o precipitados de iones de metales pesados usados se desechan en un contenedor de eliminación de desechos metálicos etiquetados, no drene estas soluciones por el desagüe o en la basura normal.
- Tomar 15 gotas de la solución desconocida en un tubo de ensayo y agregarle de 3 a 4 gotas de 6M gota\(\ce{HCl}\) a gota mientras se agita. Centrifugar por 2 min y sin decantación agregue 1 gota más de 6M\(\ce{HCl}\) para verificar que no haya más formación de precipitación. Si se forma más precipitado, centrifugue y vuelva a verificar hasta que no se forme más precipitado al agregar una gota 6M\(\ce{HCl}\) al sobrenadante. Decantar cuidadosamente y conservar el sobrenadante para el análisis de los cationes del grupo 2, y utilizar el precipitado en la siguiente etapa para la separación y conformación del catión del grupo 1, es decir,\(\ce{AgCl(s, white)}\),\(\ce{Hg2Cl2(s, white)}\),\(\ce{PbCl2(s, white)}\). Registrar las observaciones en la ficha técnica.
- Agregar 2 mL (40 gotas) de agua destilada al precipitado de la etapa 1 en un tubo de ensayo, agitarlo con una varilla de vidrio limpia para volver a suspender el precipitado, y calentar el tubo de ensayo en un baño de agua hirviendo durante 3 min mientras se agita. Añadir 15 mL de agua destilada a un 2º tubo de ensayo y calentarlo también en el baño de agua hirviendo.
- Prepare una configuración de filtración por gravedad y pase ~5 mL de agua caliente del segundo tubo de ensayo del paso 2 para convertirlo en una configuración de filtración por gravedad calentada. Deseche el filtrado que es solo agua caliente. Colocar un tubo de ensayo vacío etiquetado “Prueba de confirmación de plomo (II)” debajo del embudo de filtro calentado, filtrar el contenido del primer tubo de ensayo de la etapa 2 y recogerlo y mantener el filtrado para la\(\ce{Pb^{2+}}\) prueba en el tubo de ensayo etiquetado como “Prueba de confirmación de plomo (II)”. Conservar los residuos, si los hay, para\(\ce{Ag^{+}}\) y\(\ce{Hg2^{2+}}\) pruebas. Si no queda precipitado, las medias\(\ce{Ag^{+}}\) y\(\ce{Hg2^{2+}}\) los iones estuvieron ausentes en la muestra de prueba.
- Dejar que el filtrado de 2 mL, en el tubo de ensayo etiquetado como “Prueba de confirmación de plomo (II)”, se enfríe a temperatura ambiente colocando el tubo de ensayo en un baño de agua a temperatura ambiente. Si se formaban cristales/precipitados blancos en el filtrado al enfriarse\(\ce{Pb^{2+}}\) estaba presente en la muestra de prueba. Si no se forma ningún cristal al enfriar, agregue de 2 a 3 gotas de 6M\(\ce{HCl}\) al filtrado mientras se agita con una varilla de vidrio. Si los cristales blancos/precipitados\(\ce{Pb^{2+}}\) estaban presentes en la muestra de prueba. Si no se observa cristales/precipitado blanco en esta etapa\(\ce{Pb^{2+}}\) estuvo ausente en la muestra de prueba. Deseche la mezcla en el contenedor de desechos metálicos. Registrar la observación en la hoja de datos.
- Vuelva a suspender el residuo, si lo hay, del paso 3 en ~5 mL de agua caliente del segundo tubo de ensayo de la etapa 2 para disolver cualquier residuo\(\ce{PbCl2}\) y luego filtrarlo. Lavar el residuo con los ~5 mL restantes de agua caliente del segundo tubo de ensayo del paso 2. Deseche el filtrado que es solo el líquido de lavado con impurezas en él y deje el precipitado sobre el papel de filtro. Poner un tubo de ensayo limpio vacío bajo el embudo de filtración y agregar 40 gotas (2 mL) de 6M\(\ce{NH3}\) sobre el residuo gota a gota con agitación genal con una varilla de vidrio. Conservar el filtrado para la\(\ce{Ag^{+}}\) prueba. Si aún queda residuo en el papel de filtro y cambia de color de blanco a negro grisáceo\(\ce{Hg2^{2+}}\) estuvo presente en la muestra de prueba, de lo contrario,\(\ce{Hg2^{2+}}\) estuvo ausente en la muestra de prueba. Deseche el residuo gris en el contenedor de desechos metálicos. Registrar la observación en la hoja de datos.
- Agregar 6M\(\ce{HNO3}\) gota a gota al filtrado de 2 mL de la etapa 5, mientras se agita y se continúa probando con papel tornasol azul hasta que la solución pase de alcalina a ácida indicada por el cambio de color del papel tornasol de azul a rojo. Si se observa suspensión/precipitado blanco en esta etapa se confirma que\(\ce{Ag^{+}}\) estuvo presente en la muestra de prueba, de lo contrario, no\(\ce{Ag^{+}}\) estuvo presente en la muestra de prueba. desechar la mezcla en el contenedor de desechos metálicos. Registrar las observaciones en la ficha técnica.
- El número de paso se refiere al número de paso correspondiente en la subsección de procedimiento.
- En “la columna de reacción química esperada y observaciones esperadas”, escribir una ecuación iónica neta global de la reacción que sucederá si el ion que se procesa en el paso estuvo presente, escribir el cambio de color esperado de la solución, el precipitado esperado formado y su color esperado, etc.
- En la columna “las observaciones reales y conclusión” escribe el cambio de color, el precipitado formado y su color, etc. que realmente se observa como evidencia, y declara el ión específico como presente o ausente.
- En la fila “la conclusión general” escribe uno por uno símbolo de los iones que se están probando con una declaración “presente” o “ausente” seguida de evidencia/s para apoyar tu conclusión.