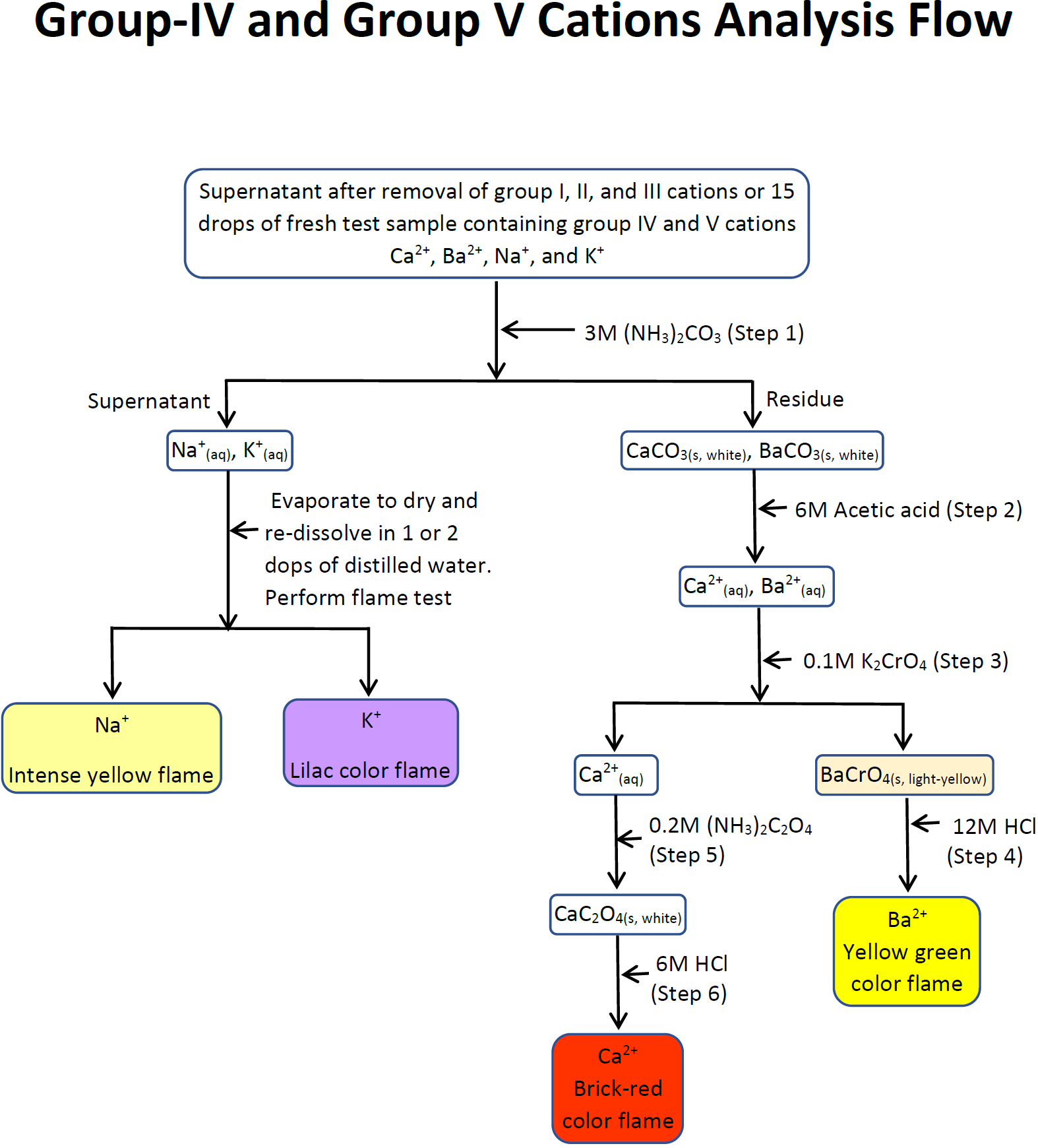
6.3: Procedimiento, diagrama de flujo y hojas de datos para la separación y confirmación de cationes del grupo IV y del grupo V
- Page ID
- 76253
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \) \( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)\(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\) \(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\)\(\newcommand{\AA}{\unicode[.8,0]{x212B}}\)
|
Químico |
Peligro |
|---|---|
|
Ácido acético 6M (\(\ce{CH3COOH}\)) |
Tóxico y corrosivo |
|
Oxalato de amonio 0.2M |
Irritante |
|
0.1M Cloruro de bario |
Altamente tóxico |
|
0.1M Cloruro de calcio |
Irritante |
|
0.1M Cromato de Potasio |
Sospecha de carcinógeno |
- *Los peligros de amoniaco 6M, ácido clorhídrico 6M, ácido nítrico 6M, peróxido de hidrógeno al 3% y tioacetamida 1M se enumeran en el capítulo 2 en la sección de reactivos de uso común. ¡Precaución! Las soluciones de iones de metales pesados usados se desechan en un contenedor de eliminación de desechos metálicos etiquetados, no drene estas soluciones por el desagüe.
- Las soluciones o precipitados de iones de metales pesados usados se desechan en un contenedor de eliminación de desechos metálicos etiquetados, no drene estas soluciones por el desagüe o en la basura normal.
- Tomar 15 gotas de la solución de prueba fresca si los cationes del grupo I a III no están presentes en la muestra o tomar el sobrenadante de la etapa 2 del análisis de cationes del grupo III. Agregar 15 gotas de 3M\(\ce{(NH4)2CO3}\), agitar para mezclar a fondo usando una varilla de vidrio limpia, centrifugar por 2 min, decantar y mantener el sobrenadante para las pruebas del grupo V, y mantener el precipitado para el análisis de cationes del grupo IV. Registrar las observaciones en la ficha técnica.
- Lavar el precipitado de la etapa 1 resuspendiéndolo en 15 gotas de agua destilada bajo agitación, centrifugar durante 2 min, decantar y mantener el precipitado y desechar el sobrenadante que es solo el líquido de lavado. Agregar 5 gotas de ácido acético 6M al precipitado y calentar por medio minuto mientras se agita para disolver el precipitado. Añadir 2 gotas más de ácido acético 6M mientras se calienta y se agita si es necesario para disolver completamente el precipitado. Después de que el precipitado se haya disuelto, agregue 3 gotas más de ácido acético 6M para hacer un\(\ce{CH3COOH}\)/\(\ce{CH3COO^{-}}\)tampón. Registrar las observaciones en la ficha técnica.
- Agrega 10 gotas de 0.1M\(\ce{K2CrO4}\), revuelve para mezclar y calentar por 1 min. Centrifugar inmediatamente por 2 min y decantar mientras está caliente. Conservar el sobrenadante para el análisis de\(\ce{Ca^{2+}}\). Si en esta etapa se forma un precipitado amarillo claro, lo más probable es que se\(\ce{BaCrO4}\) deba a que esté\(\ce{Ba^{2+}}\) presente en la muestra de prueba. Conservar el precipitado para la prueba de llama. Registrar las observaciones en la ficha técnica.
- Lavar el precipitado de la etapa 2 resuspendiéndolo en 15 gotas de agua destilada, centrifugar durante 2 min, decantar y desechar el agua sobrenadante que es solo el disolvente de lavado. Agrega 5 gotas de 12M\(\ce{HCl}\) al precipitado, revuelve para mezclar y calentar en un baño de agua hirviendo durante 2 min para disolver el precipitado. Realizar la prueba de llama, es decir, sumergir un bucle limpio de alambre de nicromo o platino en la solución y luego colocar el bucle en el borde exterior de una llama azul de un quemador Bunsen, aproximadamente a medio camino entre la parte superior e inferior de la llama y observar el color de la flama. Si la solución imparte color amarillo-verde a la llama, es debido al ion bario confirmando que\(\ce{Ba^{2+}}\) está presente en la muestra de prueba. El alambre de nicromo se puede reutilizar después de sumergirlo en 6M\(\ce{HCl}\) seguido de ponerlo al rojo vivo en una llama. Repita este proceso hasta que el cable no imparta color a la llama. Entonces el cable puede ser reutilizado. Otro enfoque es cortar la parte final del alambre que se sumergió en la sal, hacer un nuevo bucle en el extremo fresco y usarlo para la siguiente prueba de llama. Deseche la solución en un contenedor de residuos metálicos y registre las observaciones en la hoja de datos.
- Al sobrenadante de la etapa 3, agregar 10 gotas de oxalato amónico 0.2M (\(\ce{(NH4)2C2O4}\)), agitar para mezclar, centrifugar por 2 min, decantar, desechar el sobrenadante y observar el precipitado. La formación de precipitado blanco en esta etapa es la\(\ce{CaC2O4}\) que es una fuerte indicación de que\(\ce{Ca^{2+}}\) está presente en la solución de prueba. Conservar el precipitado para la prueba de llama. Registrar la observación en la ficha técnica.
- Disolver el precipitado de la etapa 5 en 3 gotas de 6M\(\ce{HCl}\). Realizar la prueba de llama, es decir, sumergir un bucle limpio de alambre de nicromo o platino en la solución y luego colocar el bucle en el borde exterior de una llama azul de un quemador Bunsen, aproximadamente a medio camino entre la parte superior e inferior de la llama y observar el color de la flama. Si la solución imparte color rojo ladrillo a la llama, se debe a iones de calcio confirmando que\(\ce{Ca^{2+}}\) está presente en la muestra de prueba. Deseche la solución en el contenedor de residuos metálicos y registre las observaciones en la hoja de datos.
- Cationes del Grupo V: Evaporar el exceso de agua del sobrenadante de la etapa 1 por calentamiento. Si queda algún residuo sólido se debe a cationes del grupo V, es decir, sodio, potasio, etc. agregar una gota o dos gotas de agua para disolver el precipitado. Realizar la prueba de llama, es decir, sumergir un bucle limpio de alambre de nicromo o platino en la solución y luego colocar el bucle en el borde exterior de una llama azul de un quemador Bunsen, aproximadamente a medio camino entre la parte superior e inferior de la llama y observar el color de la llama. Si la solución imparte algo de color a la llama, se debe a los cationes del grupo V: una llama de color amarillo intenso confirma que\(\ce{Na^{+}}\) está presente en la solución de prueba, y el color púrpura o lila a la llama confirma que\(\ce{K^{+}}\) está presente en la solución de prueba. Deseche la solución en el contenedor de desechos metálicos y registre sus observaciones en la hoja de datos.
- El número de paso se refiere al número de paso correspondiente en la subsección de procedimiento.
- En “la columna de reacción química esperada y observaciones esperadas”, escribir una ecuación iónica neta global de la reacción que sucederá si el ion que se procesa en el paso estuvo presente, escribir el cambio de color esperado de la solución, el precipitado esperado formado y su color esperado, etc.
- En la columna “las observaciones reales y conclusión” escribe el cambio de color, el precipitado formado y su color, etc. que realmente se observa como evidencia, y declara el ión específico como presente o ausente.
- En la fila “la conclusión general” escribe uno por uno símbolo de los iones que se están probando con una declaración “presente” o “ausente” seguida de evidencia/s para apoyar tu conclusión.