2.1: Análisis del punto de fusión
- Page ID
- 71109
El punto de fusión (Mp) es un análisis rápido y fácil que puede usarse para identificar cualitativamente muestras relativamente puras (aproximadamente < 10% de impurezas). También es posible utilizar este análisis para determinar cuantitativamente la pureza. El análisis del punto de fusión, como su nombre indica, caracteriza el punto de fusión, una propiedad física estable, de una muestra de manera directa, que luego puede ser utilizada para identificar la muestra.
Equipo
Aunque existen diferentes diseños de aparatos, todos tienen algún tipo de medio de calentamiento o transferencia de calor con un control, un termómetro, y a menudo una luz de fondo y una lente de aumento para ayudar a observar la fusión (Figura\(\PageIndex{1}\)). La mayoría de los modelos hoy en día utilizan tubos capilares que contienen la muestra sumergida en un baño de aceite calentado. La muestra se visualiza con una simple lupa. Algunos modelos nuevos cuentan con termómetros y controles digitales e incluso permiten la programación. La programación permite un control más preciso sobre la temperatura inicial, la temperatura final y la velocidad de cambio de la temperatura.

Preparación de Muestras
Para el análisis del punto de fusión, la preparación es sencilla. La muestra debe estar completamente seca y relativamente pura (< 10% de impurezas). Luego, la muestra seca se debe empaquetar en un tubo capilar de análisis de punto de fusión, que es simplemente un tubo capilar de vidrio con un solo extremo abierto. Solo se necesitan de 1 a 3 mm de muestra para un análisis suficiente. La muestra necesita ser empaquetada en el extremo cerrado del tubo. Esto se puede hacer golpeando suavemente el tubo o dejándolo caer en posición vertical sobre una superficie dura (Figura\(\PageIndex{2}\)). Algunos aparatos tienen un vibrador para ayudar a empacar la muestra. Finalmente el tubo se debe colocar en la máquina. Algunos modelos pueden acomodar múltiples muestras.
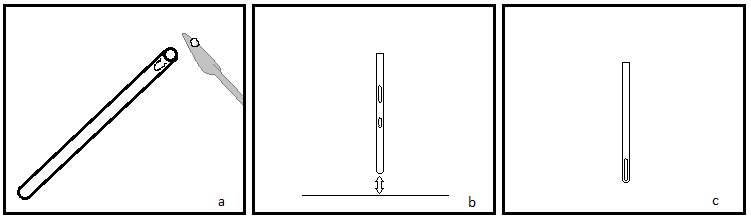
Datos de grabación
Realizar análisis es diferente de una máquina a otra, pero el proceso general es el mismo (Figura\(\PageIndex{3}\)). Si es posible, elija una temperatura inicial, una temperatura final y una tasa de cambio de temperatura. Si se conoce la identidad de la muestra, basar las temperaturas de inicio y finalización a partir del punto de fusión conocido del químico, proporcionando márgenes en ambos lados del rango. Si usa un modelo sin programación, simplemente encienda la máquina y monitoree la tasa de cambio de temperatura manualmente.
Figura\(\PageIndex{3}\) Un video que discute la preparación de muestras, registro de datos y análisis de punto de fusión en general. Hecho por Indiana University-Purdue University Indianapolis departamento de química.
Inspeccione visualmente la muestra a medida que se calienta. Una vez que comienza la fusión, anote la temperatura. Cuando la muestra esté completamente fundida, anote nuevamente la temperatura. Ese es el rango de punto de fusión para la muestra. Las muestras puras suelen tener un rango de punto de fusión de 1 - 2 °C, sin embargo, esto puede ampliarse debido a las propiedades coligativas.
Interpretación de datos
Hay dos usos principales de los datos de análisis del punto de fusión. El primero es para la identificación cualitativa de la muestra, y el segundo es para la caracterización cuantitativa de la pureza de la muestra.
Para su identificación, compare el rango de punto de fusión experimental de los valores desconocidos a la literatura. Existen varias bases de datos vastas de estos valores. Obtener una muestra pura del químico sospechoso y mezclar una pequeña cantidad de lo desconocido con él y realizar nuevamente el análisis del punto de fusión. Si se observa un rango de punto de fusión agudo a temperaturas similares a los valores de la literatura, entonces lo desconocido probablemente se haya identificado correctamente. Por el contrario, si el rango de punto de fusión se deprime o amplía, lo que sería debido a propiedades coligativas, entonces no se identificó con éxito lo desconocido.
Para caracterizar la pureza, primero es necesario conocer la identidad del disolvente (el constituyente principal de la muestra) y la identidad del soluto primario. Esto se puede hacer usando otras formas de análisis, como la cromatografía de gases-espectroscopía de masas acoplada a una base de datos. Debido a que la depresión del punto de fusión es única entre los productos químicos, es necesario obtener o preparar una curva de fusión mixta que compare las fracciones molares de los dos constituyentes con el punto de fusión (Figura\(\PageIndex{4}\)). Simplemente prepare estándares con relaciones de fracción molar conocidas, luego realice análisis del punto de fusión en cada estándar y grafique los resultados. Comparar el rango de punto de fusión de la muestra experimental con la curva para identificar las fracciones molares aproximadas de los constituyentes. Este tipo de caracterización de pureza no se puede realizar si hay más de dos componentes primarios en la muestra.
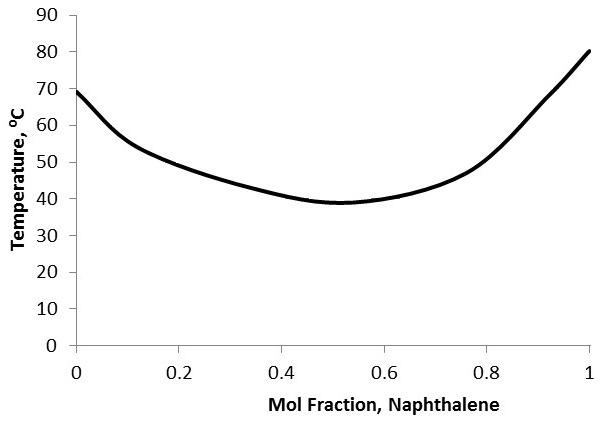
Especificidad y precisión
El análisis del punto de fusión es bastante específico y preciso dada su simplicidad. Debido a que el punto de fusión es una característica física única de una sustancia, el análisis del punto de fusión tiene una alta especificidad. Aunque, muchas sustancias tienen puntos de fusión similares, por lo que tener una idea de los posibles productos químicos en mente puede reducir enormemente las opciones. Los termómetros utilizados también son precisos. Sin embargo, el punto de fusión también depende de la presión, por lo que los resultados experimentales pueden variar de los valores de la literatura, especialmente en lugares extremos, es decir, lugares de gran altitud. La mayor fuente de error proviene de la detección visual de fusión por parte del experimentador. Controlar la tasa de cambio y ejecutar múltiples pruebas puede disminuir el grado de error introducido en este paso.
Ventajas del análisis de punto de fusión
El análisis del punto de fusión es un análisis preliminar rápido, relativamente fácil y económico si la muestra ya es mayoritariamente pura y tiene una identidad sospechosa. Adicionalmente, el análisis requiere solo muestras pequeñas.
Limitaciones del análisis del punto de fusión
Al igual que con cualquier análisis, existen ciertos inconvenientes en el análisis del punto de fusión. Si la muestra no es sólida, no se puede realizar el análisis del punto de fusión. Además, el análisis es destructivo de la muestra. Para el análisis de identificación cualitativa, ahora existen análisis más específicos y precisos, aunque suelen ser mucho más caros. Además, las muestras con más de un soluto no pueden analizarse cuantitativamente para determinar su pureza.


