2.3: Análisis de Área de Superficie BET de Nanopartículas
- Page ID
- 71122
Introducción
En los últimos años, la investigación en nanotecnología se ha expandido fuera del departamento de química y hacia los campos de la medicina, la energía, la aeroespacial e incluso la computación y la tecnología de la información. Con los materiales a granel, el área superficial a volumen es insignificante en relación con el número de átomos en el volumen, sin embargo cuando las partículas tienen solo 1 a 100 nm de ancho, comienzan a surgir diferentes propiedades. Por ejemplo, el óxido de zinc de calidad comercial tiene un rango de área superficial de 2.5 a 12 m 2 /g mientras que el óxido de zinc en nanopartículas puede tener áreas superficiales tan altas como 54 m 2 /g. Las nanopartículas tienen propiedades superiores de bloqueo UV en comparación con el material a granel, lo que las hace útiles en aplicaciones como protector solar. Muchas propiedades útiles de las nanopartículas se elevan a partir de su pequeño tamaño, por lo que es muy importante poder determinar su área superficial.
Descripción general de la teoría BET
La teoría BET fue desarrollada por Stephen Brunauer (Figura\(\PageIndex{1}\)), Paul Emmett (Figura\(\PageIndex{2}\)) y Edward Teller (Figura\(\PageIndex{3}\)) en 1938. Se tomó la primera letra del apellido de cada editor para nombrar esta teoría. La teoría BET fue una extensión de la teoría Langmuir, desarrollada por Irving Langmuir (Figura\(\PageIndex{4}\)) en 1916.




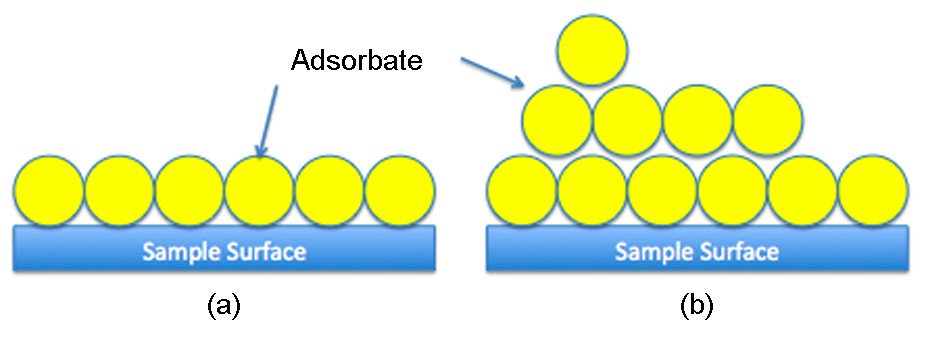
La teoría de Langmuir relaciona la adsorción monocapa de moléculas de gas (Figura\(\PageIndex{5}\)), también llamadas adsorbatos, sobre una superficie sólida con la presión de gas de un medio por encima de la superficie sólida a una temperatura fija a\ ref {1}, donde θ es la cubierta fraccional de la superficie, P es la presión del gas y α es una constante.
\[ \Theta \ =\ \frac{\alpha \cdot P}{1\ +\ (\alpha \cdot P)} \label{1} \]
La teoría de Langmuir se basa en los siguientes supuestos:
- Todos los sitios superficiales tienen la misma energía de adsorción para el adsorbato, que suele ser argón, criptón o gas nitrógeno. El sitio de la superficie se define como el área de la muestra donde una molécula puede adsorber.
- La adsorción del disolvente en un sitio ocurre independientemente de la adsorción en sitios vecinos.
- La actividad del adsorbato es directamente proporcional a su concentración.
- Los adsorbatos forman una monocapa.
- Cada sitio activo puede ser ocupado solo por una partícula.
La teoría Langmuir tiene algunos defectos que son abordados por la teoría BET. La teoría BET extiende la teoría de Langmuir a la adsorción multicapa (Figura\(\PageIndex{1}\)) con tres supuestos adicionales:
- Las moléculas de gas se adsorben físicamente sobre un sólido en capas infinitamente.
- Las diferentes capas de adsorción no interactúan.
- La teoría se puede aplicar a cada capa.
¿Cómo funciona BET?
La adsorción se define como la adhesión de átomos o moléculas de gas a una superficie. Cabe señalar que la adsorción no se confunde con la absorción, en la que un fluido permea un líquido o sólido. La cantidad de gas adsorbido depende de la superficie expuesta son pero también de la temperatura, la presión del gas y la fuerza de interacción entre el gas y el sólido. En el análisis de área superficial BET, se suele utilizar nitrógeno debido a su disponibilidad en alta pureza y su fuerte interacción con la mayoría de los sólidos. Debido a que la interacción entre las fases gaseosa y sólida suele ser débil, la superficie se enfría usando N 2 líquido para obtener cantidades detectables de adsorción. Las cantidades conocidas de gas nitrógeno se liberan entonces paso a paso en la celda de muestra. Presiones relativas menores a la presión atmosférica se logran creando condiciones de vacío parcial. Después de la presión de saturación, no se produce más adsorción independientemente de cualquier aumento adicional en la presión. Los transductores de presión altamente precisos y precisos monitorean los cambios de presión debidos al proceso de adsorción. Después de que se forman las capas de adsorción, la muestra se retira de la atmósfera de nitrógeno y se calienta para provocar que el nitrógeno adsorbido se libere del material y se cuantifique. Los datos recolectados se muestran en forma de isoterma BET, que representa la cantidad de gas adsorbido en función de la presión relativa. Existen cinco tipos de isotermas de adsorción posibles.
Isoterma Tipo I
El tipo I es una isoterma pseudo-langmuir porque representa la adsorción monocapa (Figura\(\PageIndex{6}\)). Se obtiene una isoterma de tipo I cuando P/P o < 1 and c > 1 en la ecuación BET, donde P/P o es el valor de presión parcial y c es la constante BET, la cual está relacionada con la energía de adsorción de la primera monocapa y varía de sólido a sólido. La caracterización de materiales microporosos, aquellos con diámetros de poro menores a 2 nm, da este tipo de isoterma.
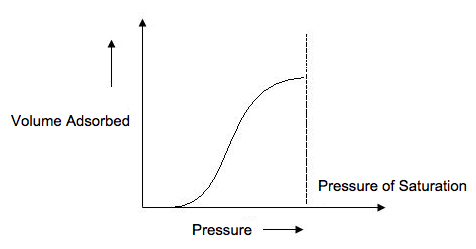
Isoterma Tipo II
Una isoterma de tipo II (Figura\(\PageIndex{7}\)) es muy diferente al modelo de Langmuir. La región más plana en el medio representa la formación de una monocapa. Se obtiene una isoterma de tipo II cuando c > 1 en la ecuación BET. Esta es la isoterma más común que se obtiene al utilizar la técnica BET. A presiones muy bajas, los microporos se llenan de gas nitrógeno. En la rodilla, comienza la formación de monocapa y la formación multicapa ocurre a presión media. A las presiones más altas, se produce la condensación capilar.
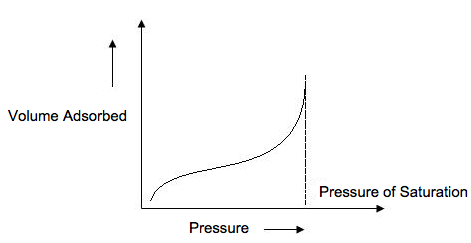
Isoterma Tipo III
Se obtiene una isoterma de tipo III (Figura\(\PageIndex{8}\)) cuando la c < 1 y muestra la formación de una multicapa. Debido a que no hay asíntota en la curva, no se forma ninguna monocapa y BET no es aplicable.
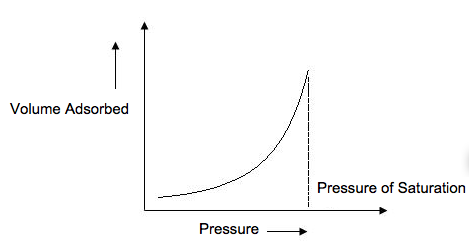
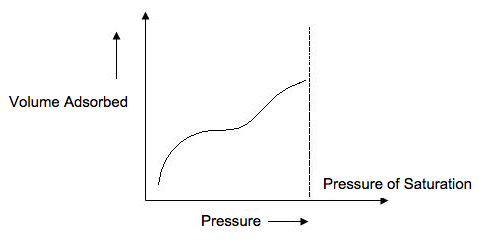
Isoterma Tipo IV
Las isotermas tipo IV (Figura\(\PageIndex{9}\)) ocurren cuando se produce la condensación capilar. Los gases se condensan en los diminutos poros capilares del sólido a presiones por debajo de la presión de saturación del gas. En las regiones de menor presión, muestra la formación de una monocapa seguida de una formación de multicapas. La caracterización del área superficial BET de materiales mesoporosos, que son materiales con diámetros de poro entre 2 - 50 nm, da este tipo de isoterma.
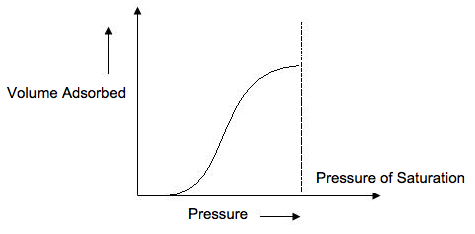
Isoterma Tipo V
Las isotermas de tipo V (Figura\(\PageIndex{10}\)) son muy similares a las isotermas de tipo IV y no son aplicables a BET.
Cálculos
La Ecuación BET,\ ref {2}, utiliza la información de la isoterma para determinar el área superficial de la muestra, donde X es el peso de nitrógeno adsorbido a una presión relativa dada (P/Po), X m es la capacidad monocapa, que es el volumen de gas adsorbido a temperatura y presión estándar (STP), y C es constante. STP se define como 273 K y 1 atm.
\[ \frac{1}{X[(P_{0}/P)-1]} = \frac{1}{X_{m}C} + \frac{C-1}{X_{m}C} (\frac{P}{P_{0}}) \label{2} \]
APUESTA multipunto
Idealmente se deben usar cinco puntos de datos, con un mínimo de tres puntos de datos, en el rango P/P 0 0.025 a 0.30 para determinar con éxito el área de superficie usando la ecuación BET. A presiones relativas superiores a 0.5, se produce el inicio de la condensación capilar, y a presiones relativas que son demasiado bajas, solo se produce la formación de monocapa. Cuando se traza la ecuación BET, la gráfica debe ser lineal con una pendiente positiva. Si no se obtiene dicha gráfica, entonces el método BET fue insuficiente para obtener el área de superficie.
- La pendiente y la intercepción se pueden obtener usando regresión de mínimos cuadrados.
- La capacidad monocapa X m se puede calcular con\ ref {3}.
- Una vez determinado X m, el área superficial total St se puede calcular con la siguiente ecuación, donde L av es el número de Avogadro, A m es el área de la sección transversal del adsorbato y es igual a 0.162 nm 2 para una molécula de nitrógeno absorbido, y M v es el volumen molar y equivale a 22414 mL,\ ref {4}.
\[ X_{m}\ = \frac{1}{s\ +\ i} = \frac{C-1}{C_{s}} \label{3} \]
\[S\ = \frac{X_{m} L_{av} A_{m}}{M_{v}} \label{4} \]
BET de punto único también se puede usar estableciendo la intercepción en 0 e ignorando el valor de C. El punto de datos a la presión relativa de 0.3 coincidirá con el mejor con una BET multipunto. BET de punto único se puede usar sobre la BET multipunto más precisa para determinar el rango de presión relativa apropiado para BET multipunto.
Preparación de muestras y configuración experimental
Antes de cualquier medición, la muestra debe desgasificarse para eliminar el agua y otros contaminantes antes de que la superficie se pueda medir con precisión. Las muestras se desgasifican al vacío a altas temperaturas. La temperatura más alta posible que no dañe la estructura de la muestra generalmente se elige para acortar el tiempo de desgasificación. La IUPAC recomienda que las muestras se desgasifiquen durante al menos 16 horas para asegurar que los vapores y gases no deseados se eliminen de la superficie de la muestra. Generalmente, las muestras que pueden soportar temperaturas más altas sin cambios estructurales tienen tiempos de desgasificación más pequeños. Se requiere un mínimo de 0.5 g de muestra para que la BET determine con éxito el área de superficie.
Las muestras se colocan en celdas de vidrio para ser desgasificadas y analizadas por la máquina BET. Las barras de vidrio se colocan dentro de la celda para minimizar el espacio muerto en la celda. Las celdas de muestra generalmente vienen en tamaños de 6, 9 y 12 mm y vienen en diferentes formas. Las celdas de 6 mm generalmente se usan para polvos finos, celdas de 9 mm para partículas más grandes y pellets pequeños y 12 mm se usan para piezas grandes que no se pueden reducir aún más. Las celdas se colocan en mantos calefactores y se conectan al puerto de salida de gas de la máquina.
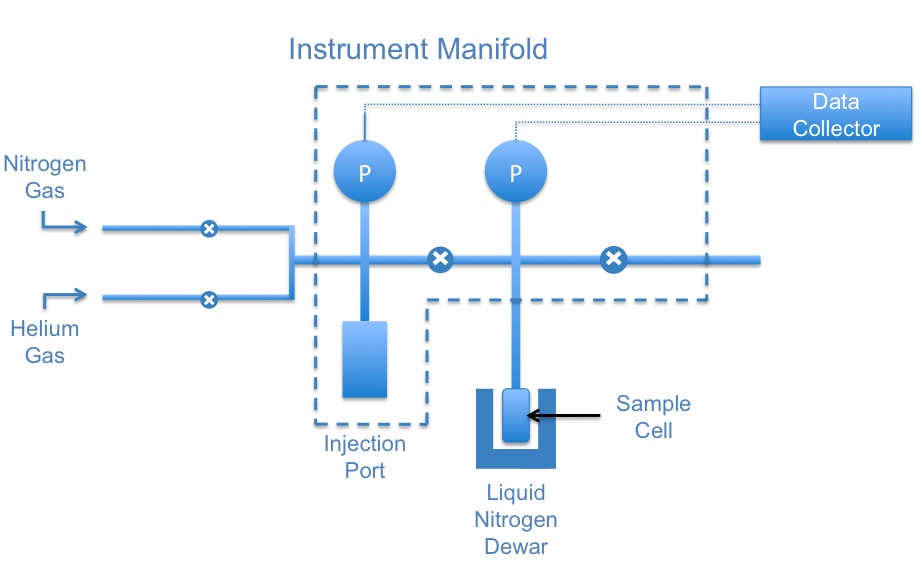
Después de desgasificar la muestra, la celda se mueve al puerto de análisis (Figura\(\PageIndex{11}\)). Se utilizan deguerras de nitrógeno líquido para enfriar la muestra y mantenerla a temperatura constante. Se debe mantener una temperatura baja para que la interacción entre las moléculas de gas y la superficie de la muestra sea lo suficientemente fuerte como para que se produzcan cantidades medibles de adsorción. El adsorbato, gas nitrógeno en este caso, se inyecta en la celda de muestra con un pistón calibrado. El volumen muerto en la celda de muestra debe ser calibrado antes y después de cada medición. Para ello, se utiliza gas helio para una corrida en blanco, ya que el helio no se adsorbe sobre la muestra.
Deficiencias de BET
La técnica BET presenta algunas desventajas cuando se compara con la RMN, que también se puede utilizar para medir la superficie de las nanopartículas. Las mediciones BET solo se pueden usar para determinar el área superficial de los polvos secos. Esta técnica requiere mucho tiempo para que se produzca la adsorción de moléculas de gas. Se requiere mucha preparación manual.
La determinación de la superficie de los marcos metalo-orgánicos
Se utilizó la técnica BET para determinar las áreas superficiales de marcos metal-orgánicos (MOF), los cuales son compuestos cristalinos de iones metálicos coordinados a moléculas orgánicas. Las posibles aplicaciones de los MOF, que son porosos, incluyen la purificación de gas y la catálisis. Se utilizó como ejemplo un MOF isoreticular (IRMOF) con la fórmula química Zn 4 O (pireno-1,2-dicarboxilato\(\PageIndex{12}\)) 3 (Figura) para ver si BET podía determinar con precisión el área superficial de los materiales microporosos. La superficie prevista se calculó directamente a partir de la geometría de los cristales y coincidió con los datos obtenidos de las isotermas BET. Los datos se recolectaron a una temperatura constante de 77 K y se obtuvo una isoterma tipo II (Figura\(\PageIndex{13}\)).
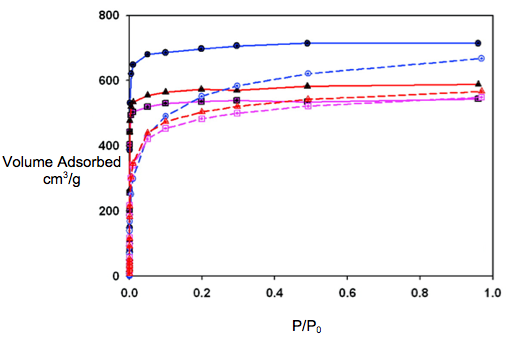
Los datos de isoterma obtenidos del rango de presión parcial de 0.05 a 0.3 se enchufa en la ecuación BET,\ ref {2}, para obtener la gráfica BET (Figura\(\PageIndex{14}\)).
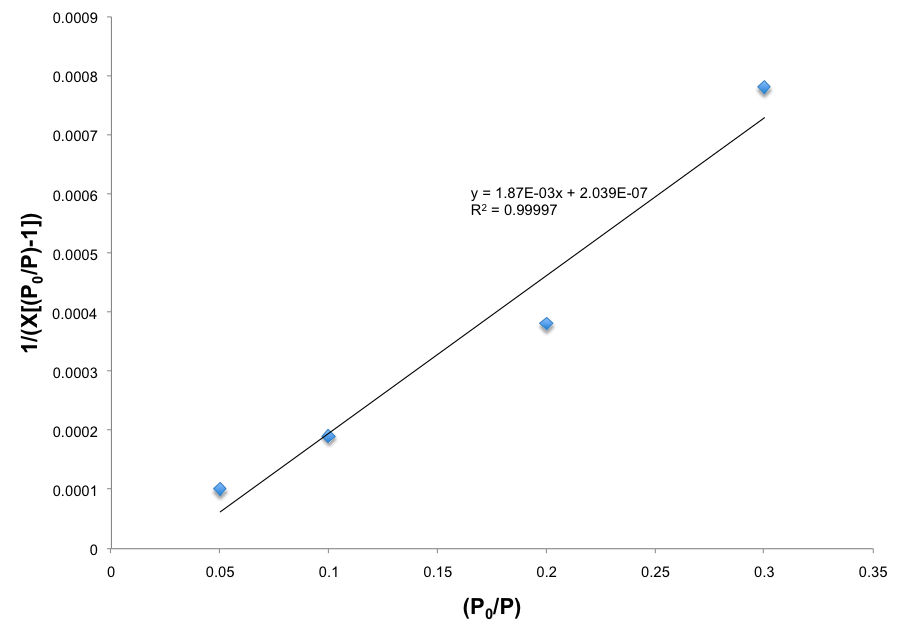
Usando\ ref {5}, se determina que la capacidad de monocapa es 391.2 cm 3 /g.
\[ X_{m}\ = \frac{1}{(2.66E\ -\ 3)\ +\ (-5.212E\ -\ 0.05)} \label{5} \]
Ahora que se conoce X m, entonces\ ref {6} se puede utilizar para determinar que la superficie es 1702.3 m 2 /g.
\[S\ =\frac{391.2cm^{2} \ast 0.162nm^{2} \ast 6.02\ast 10^{23}}{22.414:L} \label{6} \]


