4.4: Espectroscopia UV-Visible
- Page ID
- 71089
La espectroscopia ultravioleta-visible (UV-Vis) se utiliza para obtener los espectros de absorbancia de un compuesto en solución o como un sólido. Lo que en realidad se observa espectroscópicamente es la absorbancia de energía luminosa o radiación electromagnética, que excita electrones desde el estado fundamental hasta el primer estado excitado singlete del compuesto o material. La región UV-Vis de energía para el espectro electromagnético cubre 1.5 - 6.2 eV que se relaciona con un rango de longitud de onda de 800 - 200 nm. La Ley Beer-Lambert, Ecuación\ ref {1}, es el principio detrás de la espectroscopia de absorbancia. Para una sola longitud de onda, A es absorbancia (sin unidad, generalmente vista como unidades arb. o unidades arbitrarias), ε es la absortividad molar del compuesto o molécula en solución (M -1 cm -1), b es la longitud de la trayectoria de la cubeta o portamuestras (generalmente 1 cm), y c es la concentración de la solución (M).
\[ A\ =\ \varepsilon b c \label{1} \]
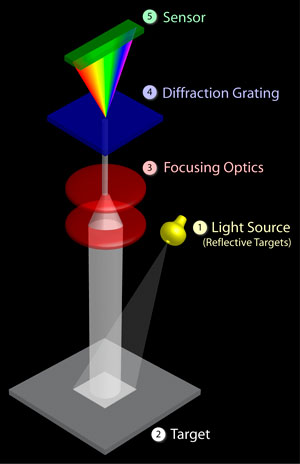
Todos estos instrumentos tienen una fuente de luz (generalmente una lámpara de deuterio o tungsteno), un portamuestras y un detector, pero algunos tienen un filtro para seleccionar una longitud de onda a la vez. El instrumento de haz único (Figura\(\PageIndex{1}\)) tiene un filtro o un monocromador entre la fuente y la muestra para analizar una longitud de onda a la vez. El instrumento de doble haz (Figura\(\PageIndex{2}\)) tiene una sola fuente y un monocromador y luego hay un divisor y una serie de espejos para llevar el haz a una muestra de referencia y la muestra a analizar, esto permite lecturas más precisas. En contraste, el instrumento simultáneo (Figura\(\PageIndex{3}\)) no tiene un monocromador entre la muestra y la fuente; en cambio, tiene un detector de matriz de diodos que permite al instrumento detectar simultáneamente la absorbancia en todas las longitudes de onda. El instrumento simultáneo suele ser mucho más rápido y eficiente, pero todos estos tipos de espectrómetros funcionan bien.
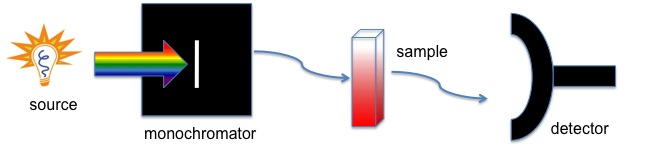
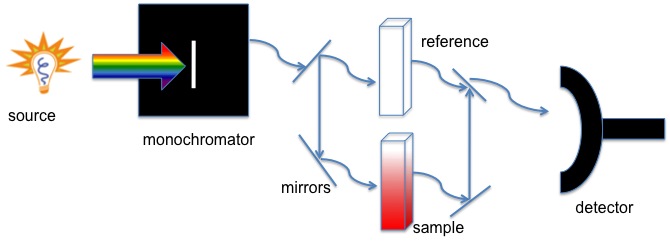
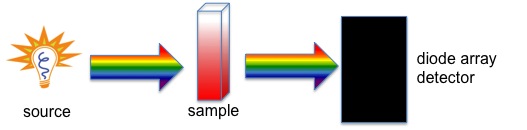
¿Qué información se puede obtener de los espectros UV-Vis?
Los datos espectroscópicos UV-Vis pueden proporcionar información cualitativa y cuantitativa de un compuesto o molécula dada. Independientemente de si se requiere información cuantitativa o cualitativa, es importante usar una celda de referencia para poner a cero el instrumento para el disolvente en el que se encuentra el compuesto. Para la información cuantitativa del compuesto, se requeriría calibrar el instrumento utilizando concentraciones conocidas del compuesto en cuestión en una solución con el mismo disolvente que la muestra desconocida. Si la información necesaria es solo una prueba de que un compuesto está en la muestra que se está analizando, no será necesaria una curva de calibración; sin embargo, si se está realizando un estudio de degradación o reacción, y se requiere concentración del compuesto en solución, por lo tanto, se necesita una curva de calibración.
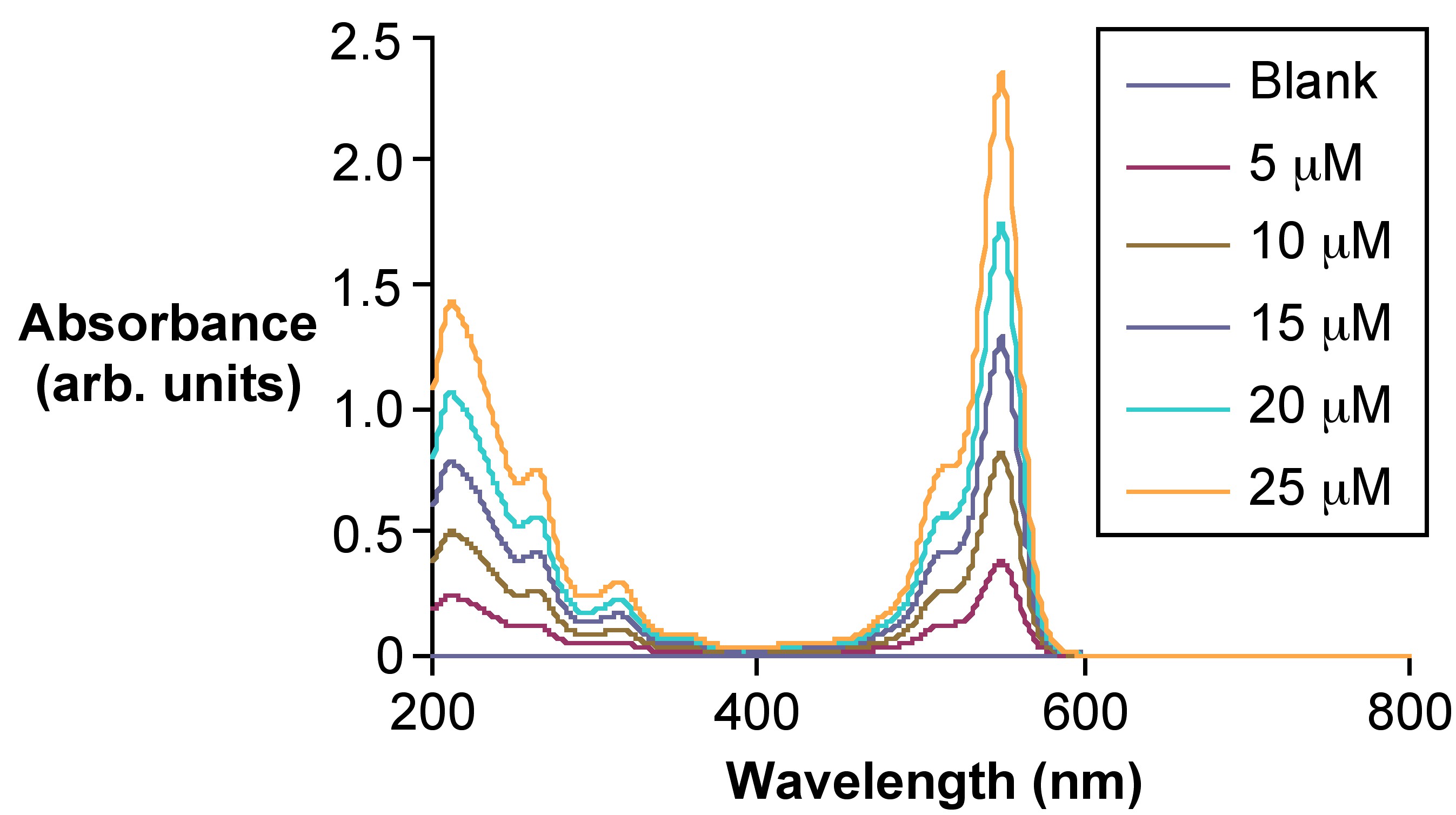
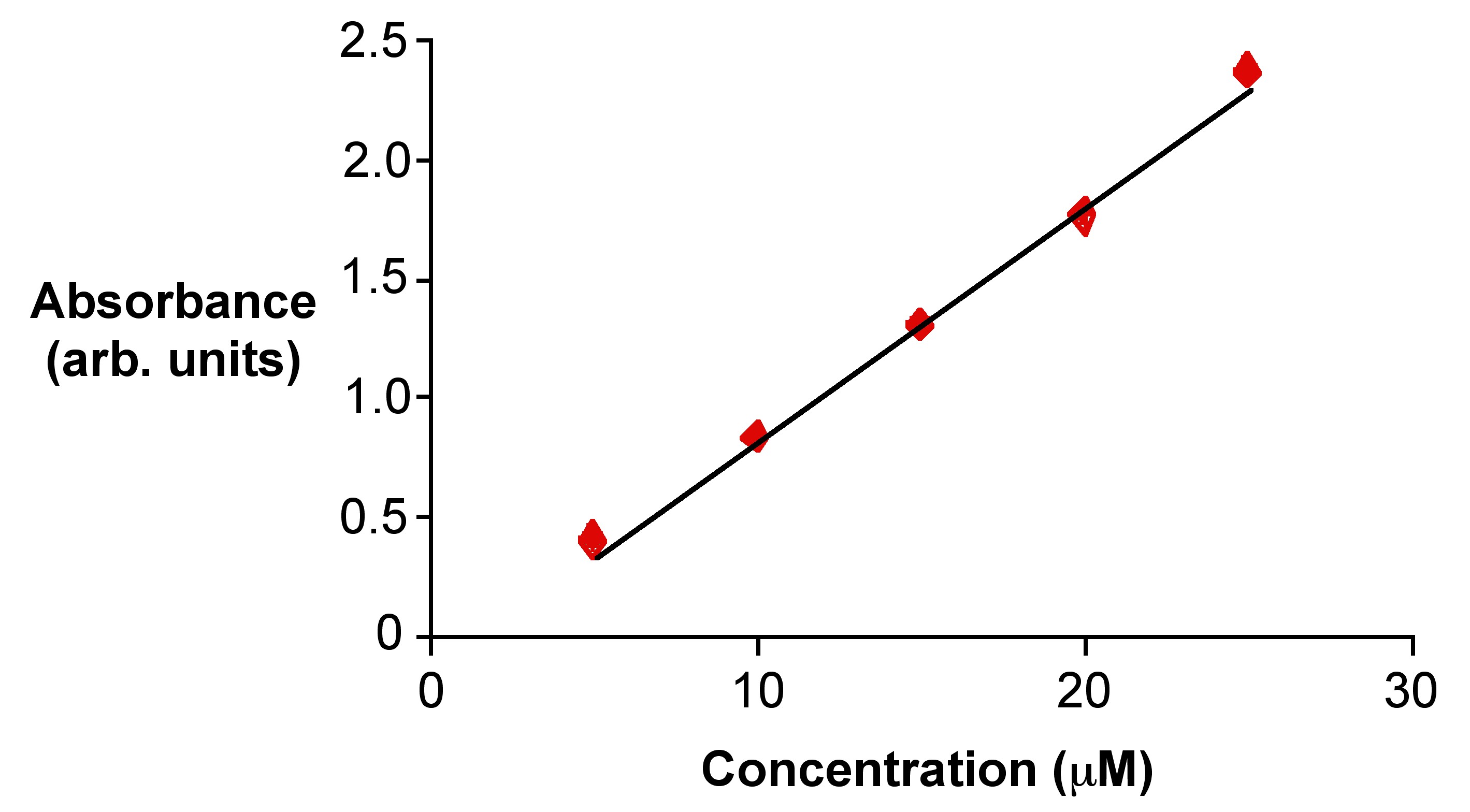
Para hacer una curva de calibración, se necesitarán al menos tres concentraciones del compuesto, pero cinco concentraciones serían las más ideales para una curva más precisa. Las concentraciones deben comenzar justo por encima de la concentración estimada de la muestra desconocida y deben bajar a aproximadamente un orden de magnitud menor que la concentración más alta. Las soluciones de calibración deben estar espaciadas relativamente por igual, y deben hacerse con la mayor precisión posible utilizando pipetas digitales y matraces volumétricos en lugar de cilindros graduados y vasos de precipitados. Un ejemplo de espectros de absorbancia de soluciones de calibración de Rosa de Bengala (4,5,6,7-tetracloro-2',4',5',7'-tetraiodofluoresceína, Figura\(\PageIndex{4}\), se puede observar en la Figura\(\PageIndex{5}\). Para realizar una curva de calibración, el valor para las absorbancias de cada una de las curvas espectrales a la longitud de onda de absorción más alta, se grafica en una gráfica similar a la\(\PageIndex{6}\) de la Figura de absorbancia versus concentración. El coeficiente de correlación de una calibración aceptable es 0.9 o mejor. Si el coeficiente de correlación es menor que eso, intente hacer las soluciones nuevamente ya que el problema puede ser un error humano. No obstante, si después de hacer las soluciones algunas veces la calibración sigue siendo pobre, algo puede estar mal con el instrumento; por ejemplo, las lámparas pueden estar yendo mal.
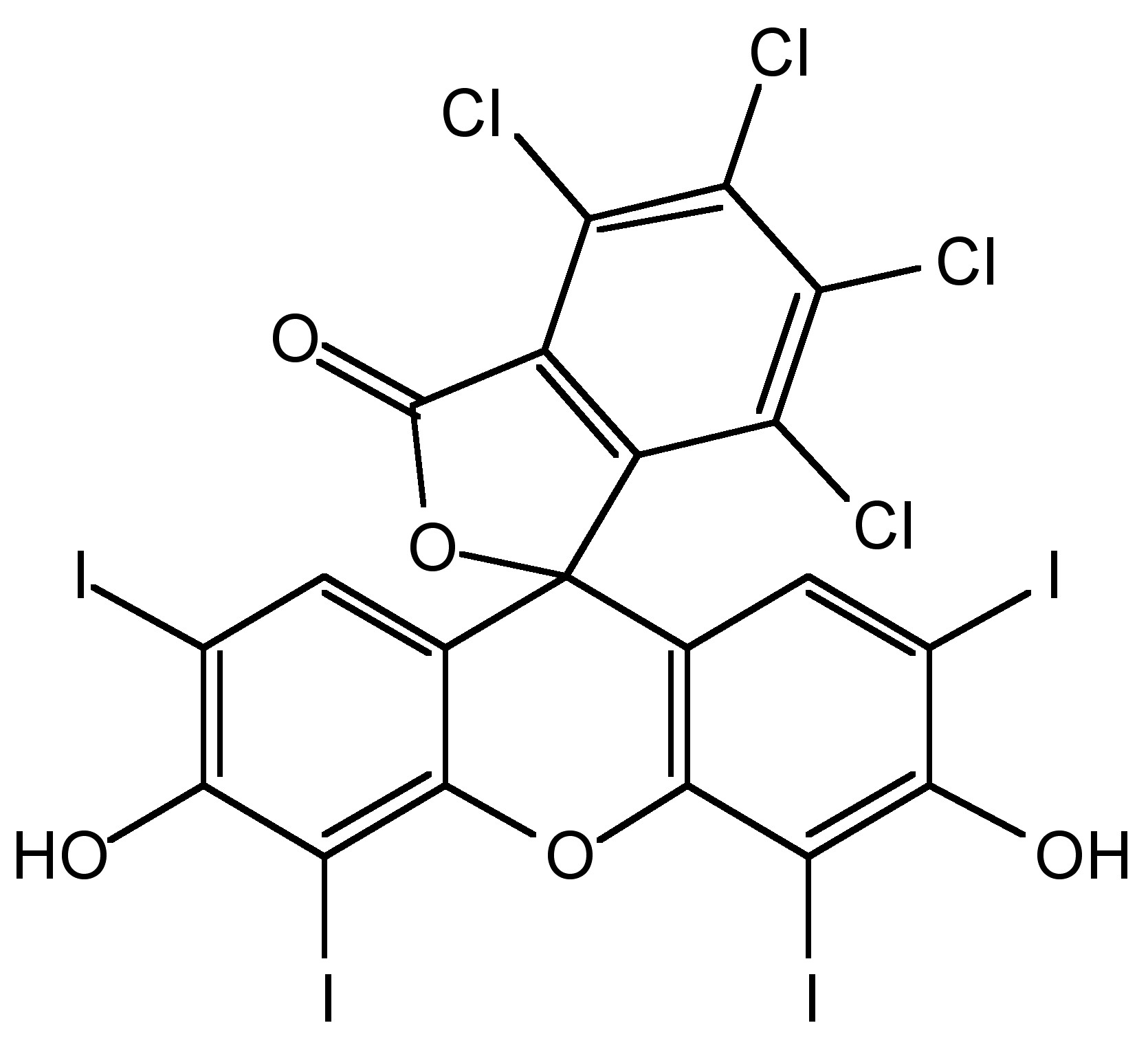
Limitaciones de la espectroscopia UV-Vis
Muestra
La espectroscopia UV-Vis funciona bien en líquidos y soluciones, pero si la muestra es más una suspensión de partículas sólidas en líquido, la muestra dispersará la luz más que absorberá la luz y los datos estarán muy sesgados. La mayoría de los instrumentos UV-Vis pueden analizar muestras sólidas o suspensiones con un aparato de difracción (Figura\(\PageIndex{7}\)), pero esto no es común. Los instrumentos UV-Vis generalmente analizan líquidos y soluciones de la manera más eficiente.
Calibración y Referencia
Se necesitará una referencia en blanco al comienzo del análisis del disolvente a utilizar (agua, hexanos, etc.), y si es necesario realizar análisis de concentración, las soluciones de calibración deben realizarse con precisión. Si las soluciones no se hacen con la suficiente precisión, no se determinará con precisión la concentración real de la muestra en cuestión.
Elección de Solvente o Contenedor
Cada disolvente tiene una longitud de onda de corte de absorbancia UV-Vis. El punto de corte del disolvente es la longitud de onda por debajo de la cual el propio disolvente absorbe toda la luz. Entonces, al elegir un solvente, tenga en cuenta su corte de absorbancia y donde se cree que el compuesto bajo investigación absorbe. Si están cerca, elija un solvente diferente. La tabla\(\PageIndex{1}\) proporciona un ejemplo de cortes de disolvente.
| Solvente | Corte de absorbancia UV (nm) |
|---|---|
| Acetona | 329 |
| Benceno | 278 |
| Dimetilformamida | 267 |
| Etanol | 205 |
| Tolueno | 285 |
| Agua | 180 |
El material del que está hecha la cubeta (el portamuestras) también tendrá un corte de absorbancia UV-Vis. El vidrio absorberá toda la luz mayor en energía comenzando en aproximadamente 300 nm, por lo que si la muestra absorbe en la UV, una cubeta de cuarzo será más práctica ya que el corte de absorbancia es de alrededor de 160 nm para el cuarzo (Tabla\(\PageIndex{2}\)).
| Material | Rango de longitud de onda (nm) |
|---|---|
| Vidrio | 380-780 |
| Plástico | 380-780 |
| Cuarzo Fundido | < 380 |
Concentración de Solución
Para obtener datos confiables, el pico de absorbancia de un compuesto dado debe ser al menos tres veces mayor en intensidad que el ruido de fondo del instrumento. Obviamente, el uso de concentraciones más altas del compuesto en solución puede combatir esto. Además, si la muestra es muy pequeña y diluirla no daría una señal aceptable, hay cubetas que contienen tamaños de muestra más pequeños que los 2.5 mL de una cubetas estándar. Algunas cubetas están hechas para contener solo 100 μL, lo que permitiría analizar una pequeña muestra sin tener que diluirla a un volumen mayor, disminuyendo la relación señal/ruido.


