19.4: Forma de Anfífilos Autoensamblados
- Page ID
- 69581
Empíricamente se observa que ciertas características de la estructura molecular de moléculas anfifílicas y surfactantes se correlacionan con la forma de las estructuras más grandes en las que se autoensamblan. Por ejemplo, las colas largas de hidrocarburos simples con un grupo sulfo (como SDS) tienden a agregarse en micelas esféricas, mientras que los fosfosfolípidos con dos cadenas hidrocarbonadas (como DMPC) prefieren formar bicapas. Dado que la formación de estructuras se rige en gran medida por el efecto hidrofóbico, condensando las colas hidrófobas y conduciendo los grupos cargados a una interfaz de agua, esto lleva a la conclusión de que el volumen y empaquetamiento de la cola hidrófoba juega un papel clave en la forma. Mientras que el volumen molecular y el tamaño del grupo principal y la carga son fijos, la naturaleza fluida de la cadena de hidrocarburos permite que la molécula se empaquete en diferentes configuraciones.
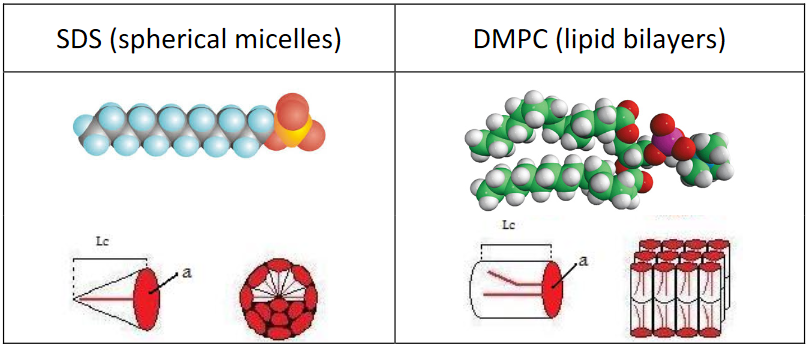
 Esta variabilidad estructural es capturada por el parámetro de empaque:
Esta variabilidad estructural es capturada por el parámetro de empaque:
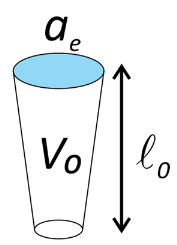
\( p = \dfrac{V_0}{a_e \ell_0} \)
donde V 0 y\(\ell_0\) son el volumen y longitud de la cadena hidrocarbonada, y a e es el área superficial promedio por grupo de cabeza cargado. \(V_0 / \ell_0 \)es relativamente constante a ~0.2 nm 2, pero la forma de la cadena puede variar de extendida (cilíndrica) a compacta (cónica), lo que favorecerá un empaque particular.
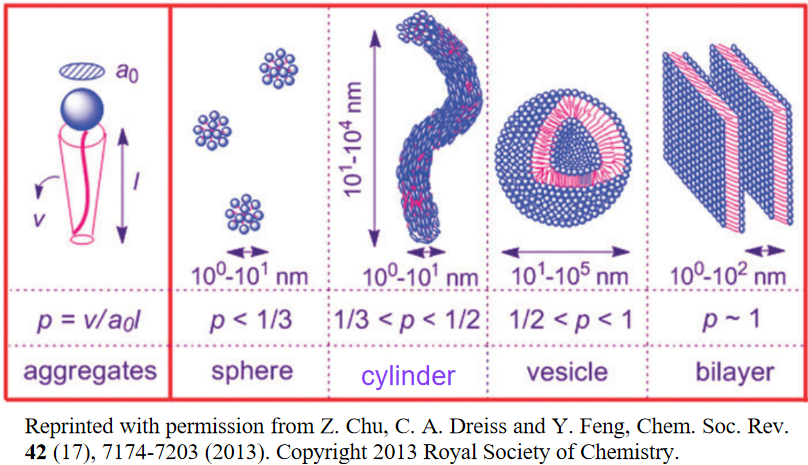
Empíricamente se encuentra que los sistemas con p < ⅓ típicamente forman micelas, para estructuras cilíndricas para ⅓ < p < ½, y para estructuras bicapa para ½ < p < 1. Se pueden hacer argumentos geométricos simples para racionalizar esta observación. Tomando como ejemplo un agregado esférico con radio R y número de agregación n, esperamos que la relación entre el volumen y el área de superficie sea
\[ \dfrac{V}{A} = \dfrac{nV_0}{na_e} = \dfrac{R}{3} \quad \rightarrow \quad V_0 = \dfrac{a_eR}{3} \]
Sustituyendo en el parámetro de empaque:
\[ p = \dfrac{V_0}{a_e \ell_0} = \dfrac{R}{3\ell_0} \]
Ahora bien, aunque no se conoce la conformación exacta de la cadena hidrocarbonada, la longitud de la cola de hidrocarburo no será mayor que el radio de la micela, es decir,\(\ell_0 \geq R \). Por lo tanto
\[ \therefore p \leq \dfrac{1}{3} \qquad (spheres) \]
Se pueden usar argumentos similares para explicar por qué las bicapas lipídicas extendidas tienen\(p \approx 1 \) y cilindros para p ≈ ½. En un sentido más general, observamos que el parámetro de empaquetamiento está relacionado con la curvatura de la superficie agregada. A medida que p disminuye por debajo de uno, el agregado forma una superficie cada vez más curva. (Por lo tanto, se espera que las vesículas tengan ½ < p < 1). También es posible tener p > 1. En este caso, la curvatura también aumenta con el aumento de p, aunque el signo de la curvatura se invierte (de convexo a cóncavo). Tales condiciones dan como resultado estructuras invertidas, como micelas inversas en las que el agua está confinada en una piscina esférica en contacto con los grupos principales cargados, y las colas de hidrocarburos se proyectan hacia afuera en un disolvente hidrófobo.
_____________________________________________________________________
Lecturas
J. N. Israelachvili, Fuerzas Intermoleculares y de Superficie, 3a ed. (Academic Press, Burlington, MA, 2011).

