9.1: Preludio a los Equilibrios Químicos
- Page ID
- 72263
Lo pequeño es grande, lo grande es pequeño; todo está en equilibrio en necesidad... - Víctor Hugo en “Los Miserables”
Como se discutió en el Capítulo 6, la tendencia natural de los sistemas químicos es buscar un estado de función mínima de Gibbs. Una vez alcanzado el mínimo, el movimiento en cualquier dirección química no será espontáneo. Es en este punto que el sistema alcanza un estado de equilibrio.
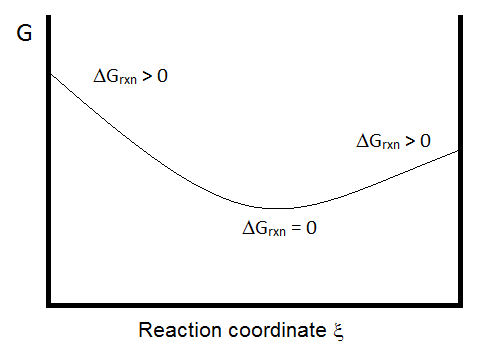
Del diagrama anterior, debe quedar claro que la dirección del cambio espontáneo se determina minimizando
\[\left(\frac{\partial G}{\partial \xi}\right)_{p,T}.\]
Si la pendiente de la curva es negativa, la reacción favorecerá un desplazamiento hacia los productos. Y si es positivo, la reacción favorecerá un cambio hacia los reactivos. Este es un punto no trivial, ya que subraya la importancia de la composición de la mezcla de reacción en la determinación de la dirección de la reacción.


