11.5: Ley de tasa de 1er orden
- Page ID
- 72226
Una ley de tasa de primer orden tomaría la forma
\[ \dfrac{d[A]}{dt} = k[A]\]
Nuevamente, separar las variables colocando todos los términos de concentración a la izquierda y todos los términos de tiempo a la derecha rinde
\[ \dfrac{d[A]}{[A]} =-k\,dt\]
Esta expresión también se integra fácilmente como antes
\[ \int_{[A]=0}^{[A]} \dfrac{d[A]}{[A]} =-k \int_{t=0}^{t=t}\,dt\]
Señalando que
\[ \dfrac{dx}{x} = d (\ln x)\]
La forma de la ley de tasa integrada se convierte
\[ \ln [A] - \ln [A]_o = kt\]
o
\[ \ln [A] = \ln [A]_o - kt \label{In1}\]
Esta forma implica que una gráfica del logaritmo natural de la concentración es una función lineal del tiempo. Y así una gráfica de ln [A] en función del tiempo debería producir una gráfica lineal, cuya pendiente es -k, y cuya intercepción es ln [A] 0.
Ejemplo\(\PageIndex{1}\):
Considera los siguientes datos cinéticos. Utilice una gráfica para demostrar que los datos son consistentes con la cinética de primer orden. Además, si los datos son de primer orden, determinar el valor de la constante de velocidad para la reacción.
| Tiempo (s) | 0 | 10 | 20 | 50 | 100 | 150 | 200 | 250 | 300 |
|---|---|---|---|---|---|---|---|---|---|
| [A] (M) | 0.873 | 0.752 | 0.648 | 0.414 | 0.196 | 0.093 | 0.044 | 0.021 | 0.010 |
Solución:
La trama se ve de la siguiente manera:
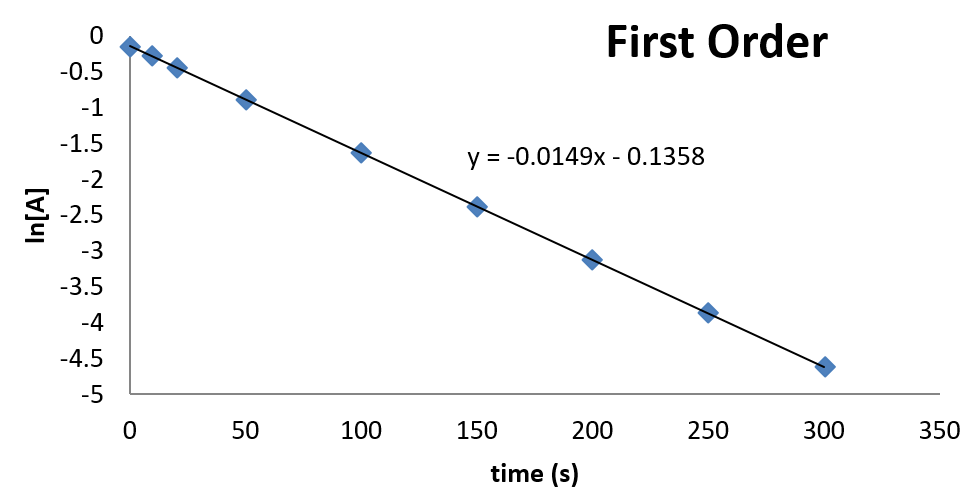
De esta parcela, se puede observar que la constante de velocidad es de 0.0149 s -1. La concentración en el momento también se\(t = 0\) puede inferir de la intercepción.
También hay que señalar que la ley de tasa integrada (Ecuación\ ref {In1}) se puede expresar en forma exponencial:
\[ [A] = [A]_o e^{-kt}\]
Debido a esta forma funcional, la cinética de primer orden a veces se denomina cinética de decaimiento exponencial. Muchos procesos, incluida la desintegración radiactiva de los nuclidos, siguen este tipo de ley de tasas.


