5.1: Q-NMR para la determinación de la pureza de los estándares de referencia de antibióticos macrólidos- Comparación con el método de balance
- Page ID
- 71095
Los antibióticos macrólidos se derivan de fermentaciones microbianas. Como clase los antibióticos macrólidos contienen una lactona macrocíclica de 14 o 16 integrantes, que contiene grupos amino y desoxiazúcares. La actividad antibiótica de estos compuestos resulta de la inhibición de la síntesis de proteínas bacterianas. Debido a que los macrólidos se acumulan dentro de los leucocitos, son transportados al sitio de infección. Algunos macrólidos también tienen efectos inmunomoduladores que pueden reducir la inflamación. Uno de los antibióticos macrólidos más conocidos es la eritromicina, cuya estructura se muestra aquí.
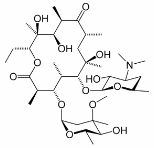
Esta aplicación examina el uso de mediciones cuantitativas de RMN 1H para determinar la pureza de los estándares de referencia de antibióticos macrólidos. Se probaron muestras de claritrmicina, roxitromicina, azitrimicina, diritromicina y midecamicina. Los experimentos de RMN Q se realizaron a 500 MHz utilizando 1,4-dinitrobenceno como patrón interno. En lugar de determinar los tiempos de relajación T 1, se seleccionó el retardo de relajación (64 s) comparando el área de pico para el estándar interno usando retardos d 1 de 1, 5,10, 20, 32, 64 y 256 s.
Los resultados de RMN Q se compararon con el enfoque más convencional de determinación del balance de masas, que se muestra en la Tabla 1 a continuación. En las determinaciones de balance de masas, el contenido se calcula como se muestra en la Ecuación\(\ref{E1}\).
\[\mathrm{Content\: \% = (1 - impurity\%)(1 - water\% - volatile\: material\: \% - sulfated\: ash\%) \times 100} \label{E1}\]
En esta determinación el% de impureza se determina por HPLC-UV. El contenido de agua se determina por valoración de Karl Fischer y los disolventes residuales se miden mediante cromatografía de gases. La cantidad de cenizas sulfatadas (principalmente una designación europea) corresponde a la cantidad de residuo restante después de la ignición de la muestra. Uno de los inconvenientes del HPLC-UV para estas mediciones es la falta de cromóforo con una longitud de onda de absorción característica. Además, un problema general con este enfoque es que el coeficiente de absorción UV de cada impureza es diferente, y en muchos casos desconocido.
Las determinaciones de pureza mediante RMN se basan en la comparación de las integrales medidas para las resonancias del analito (I x) con la integral de un patrón de cuantificación (I std). En este caso se utilizó un estándar interno. Debido a que se conocen las masas de la muestra (m x) y el estándar interno (m std), se puede determinar el contenido del analito. Tenga en cuenta que la suposición subyacente en este método es que las resonancias de las impurezas no se superponen con las resonancias utilizadas para medir el contenido de analito. La pureza del analito, Px, se calcula como se muestra en la Ecuación\(\ref{E2}\):
\[P_x = \dfrac{I_x}{I_{std}} \dfrac{N_{std}}{N_x} \dfrac{M_x}{M_{std}} \dfrac{m_{std}}{m_x} P_{std} \label{E2}\]
donde M x y M std son las masas molares del analito y el estándar, respectivamente, P std es la pureza del estándar, y N std y N x son el número de espines responsables de las señales integradas estándar y analito, respectivamente. Los resultados de contenido, resumidos en la Tabla 1, para los antibióticos macrólidos obtenidos con 1H NMR y por el método de balance de masas están en buena concordancia. La principal fuente de incertidumbre en el método Q-NMR estuvo en el peso de la muestra, alrededor de 15 mg en estos experimentos. El uso de una masa mayor disminuiría la incertidumbre en los resultados pero consumiría mayores cantidades de solventes deuterados. Una característica informativa de este informe es el análisis detallado de errores que contiene.
| Método Q-NMR 1 H (%) | Método de balance de masa (%) | |||||||
|---|---|---|---|---|---|---|---|---|
| Contenido promedio a | RSD | U expandido | Impureza/u 1 | Agua/U 2 b | Solventes residuales/U 3 b | Ceniza sulfatada/u 4 b | Contenido/ U expandido | |
| Claritromicina | 96.3 | 0.49 | 1.89 | 3.35/0.0299 | 1.4/0.0148 | <0.001/<8.4 x 10 -6 | 0/0 | 95.3/2.64 |
| Roxitromicina | 95.7 | 0.44 | 1.82 | 2.50/0.0223 | 2.2/0.0233 | <0.001/<8.4 x 10 -6 | 0/0 | 95.4/2.64 |
| Azitromicina | 94.3 | 0.50 | 1.36 | 1.59/0.0142 | 4.5/0.0486 | <0.001/<8.4 x 10 -6 | 0.02/0.0198 | 94.0/2.75 |
| Diritromicina | 96.9 | 0 | 1.81 | 3.30/0.0295 | 0.6/0.00636 | <0.001/<8.4 x 10 -6 | 0/0 | 96.1/2.67 |
| Midecamicina | 97.1 | 2.0 | 1.96 | 3.94/0.0352 | 0.16/0.000035 c | 0/0 | 95.9/1.71 | |
|
||||||||
Referencia
Liu, S.-Y.; Hu, C.-Q. “Un estudio comparativo de incertidumbre de la calibración de los estándares de referencia de antibióticos macrólidos utilizando métodos cuantitativos de resonancia magnética nuclear y balance de masas” Anal. Chim. Acta 2007, 602, 114-121.


