3.1: ¿Qué es un Solvente?
- Page ID
- 79362
Desde el punto de vista del alumno, la información presentada en una ecuación de una reacción puede resultar confusa. El material de partida y el producto están unidos por una flecha de reacción recta. El material de partida es el compuesto al inicio de la reacción; el producto es el compuesto al final. El reactivo suele mostrarse encima de la flecha. El reactivo es el compuesto necesario para convertir el material de partida en el producto.
Sin embargo, a menudo se enumera algo más junto con el reactivo: el solvente. Eso puede hacer que los estudiantes se pregunten: ¿qué hace esto? ¿Es una segunda reacción por la que debería preocuparme?
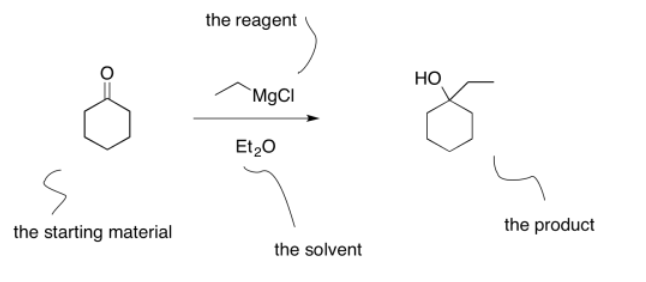
Los estudiantes a veces hacen la suposición de que el reactivo está escrito encima de la flecha y el solvente escrito debajo de la flecha. Esa es una buena observación, porque las reacciones suelen escribirse de esa manera, aunque no hay una regla que diga que tienen que serlo. No obstante, hay excepciones en las que se abandona esa forma típica de escribir las cosas. Algunas reacciones requieren muchos reactivos, aditivos y promotores diferentes, o bien hay una necesidad de reportar la temperatura o la presión. En estos casos, se escriben elementos adicionales debajo de la flecha, solo porque no hay suficiente espacio en la parte superior.
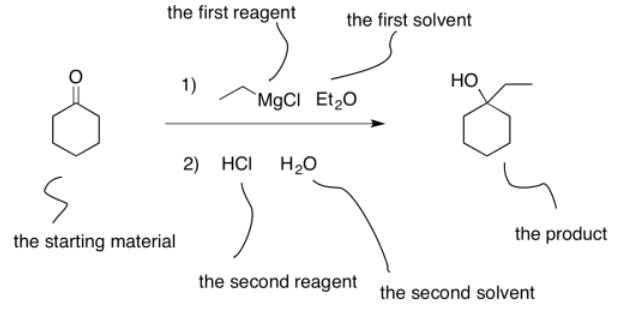
En otros casos, se ejecutan una serie de reacciones. Por ejemplo, en la reacción anterior se supone que hubo un tratamiento acuoso para neutralizar el producto. Podríamos escribir esa reacción explícitamente. En ese caso, los dos pasos diferentes están numerados, para que sepamos que se hicieron paso a paso, en lugar de tirar todo de una vez.
Los químicos suelen enumerar el solvente en la reacción porque el solvente es, prácticamente hablando, tremendamente importante. Realizar una reacción sin solvente es un poco como lavarse las manos sin agua. Podrías tomar una pastilla de jabón y pasarla entre tus dedos, pero no pasará mucho sin el poder del agua. El agua disuelve el jabón (o al menos lo suspende en micelas), lo mueve alrededor, lo pone en contacto con la suciedad y se lo lleva.
De hecho, el agua es literalmente el solvente en el proceso físico de lavado. También puede ser un solvente en muchas reacciones químicas. El solvente tiene muchos papeles que desempeñar en una reacción. Ante todo, disuelve los reactivos. En ese estado, los reactivos son muy móviles. Sin el solvente, los reactivos pueden ser sólidos, o si son líquidos, pueden ser demasiado gruesos para que las moléculas se muevan muy rápidamente; pueden ser más como aceites. Dependiendo de la naturaleza del disolvente, los intermedios pueden estabilizarse, permitiendo que se formen más fácilmente y ayudándose al curso de la reacción. Los solventes también actúan como baños, moderando el flujo de calor dentro o fuera de la reacción según sea necesario.
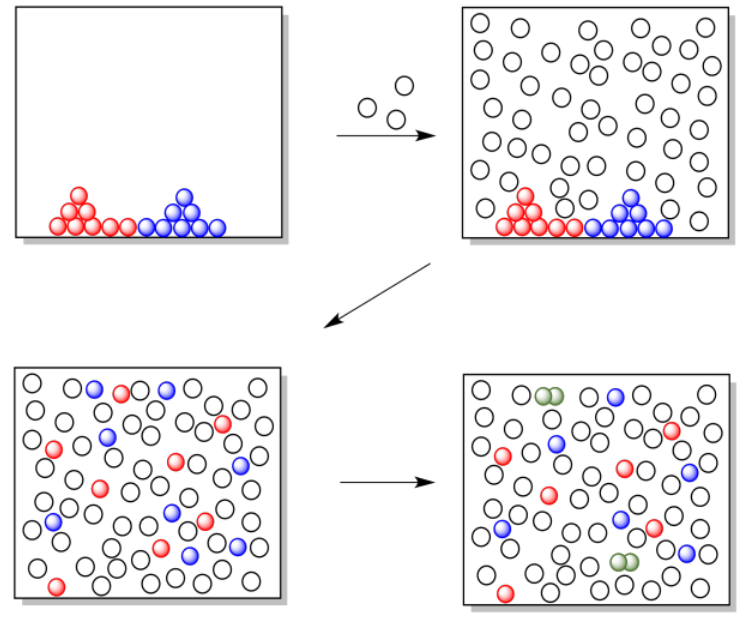
En la caricatura de abajo, no pasa nada cuando los dos reactivos se vierten juntos. Cuando se agrega un disolvente, los dos reactivos comienzan a disolverse, y a medida que se mueven en la solución los dos reactivos se encuentran entre sí y comienzan a reaccionar.
Al principio, es posible que no quieras preocuparte demasiado por el papel del solvente. Sin embargo, es posible que aún desee saber qué tipo de cosas es probable que sean solventes, aunque solo sea para que pueda ignorarlas de manera segura al intentar ordenar cómo llega el reactivo al producto.
La siguiente tabla resume una serie de los solventes más comunes, mostrados desde los más polares en la parte superior hasta los menos polares en la parte inferior.
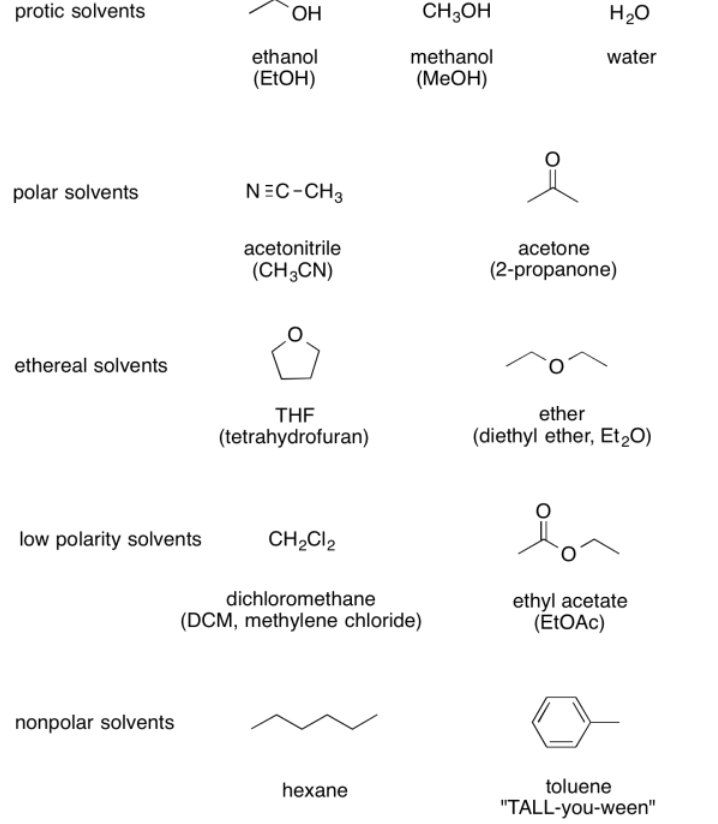
Tenga en cuenta que, el hecho de que algo actúe como solvente en una reacción no significa que deba ser uno en otro. Por ejemplo, la acetona es un solvente bastante común, pero también pasa a ser una cetona. Es probable que sufra reacciones de adición de carbonilo si se presenta con buenos nucleófilos. Por esa razón, las reacciones de adición de carbonilo no se llevarían a cabo con acetona, porque el nucleófilo simplemente reaccionaría con el disolvente en lugar del electrófilo pretendido.

