10.6: Cicloadición fotoquímica
- Page ID
- 79260
Como se señaló anteriormente, la reacción de Diels Alder es un ejemplo clásico de una reacción pericíclica.

Una reacción de Diels Alder a veces se denomina reacción de adición [2+4]. Una unidad de 2 carbonos en una molécula interactúa con una unidad de 4 carbonos en otra molécula.
En contraste, la adición de un alqueno regular a otro alqueno regular se llamaría reacción de adición [2+2]. Si esta reacción ocurriera, dos alquenos se unirían para formar un anillo de cuatro miembros.
Sin embargo, las reacciones de adición [2+2] no ocurren sin circunstancias especiales. Hay un par de razones por las que, y es posible que puedas sugerir algunas en este momento.
Se podría decir que el anillo de cuatro miembros estaría mucho más tenso que el anillo de seis miembros formado por la reacción de Diels Alder. Eso es cierto, pero puede que no sea razón suficiente para evitar que ocurra la reacción. Los anillos de cuatro miembros ocurren en la naturaleza a pesar de su energía de tensión.
También podría decirse que el estado de transición similar al benceno que estabiliza la vía a través de una reacción de Cope o Diels Alder no es posible en una adición [2+2]. De hecho, el estado de transición sería más parecido al ciclobutadieno antiaromático. El estado de transición sería muy alto en energía.
Otro problema aparece si observamos las interacciones orbitales en una reacción de adición [2+2]. El HOMO en un alqueno y LUMO en el otro alqueno no se superponen para que se puedan formar enlaces entre los dos extremos. Si los orbitales p en un extremo están en fase, los orbitales p en el otro extremo deben estar desfasados. La reorganización concertada del vínculo posible para la reacción de Diels Alder no puede suceder aquí.
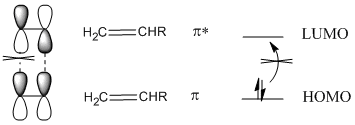
De hecho, hay una forma de evitar ese problema. Irradiar un alqueno con luz UV conduce a la promoción de un electrón del LUMO al HOMO. El alqueno se encuentra ahora en un “estado excitado”.
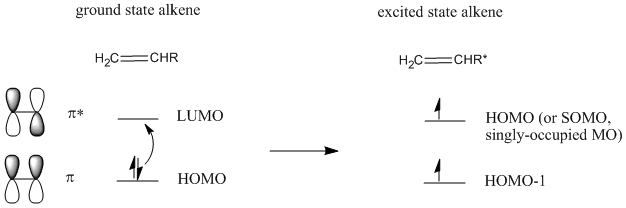
Esto no sucede con una eficiencia del 100%, por lo que solo algunos de los alquenos se emocionarán. En el alqueno estado excitado, el HOMO ahora se asemeja al LUMO del alqueno del estado base. Debido a la simetría coincidente entre estos orbitales, la reacción de adición puede continuar.

Una reacción [4+2] a veces se conoce como “permitida térmicamente”, mientras que una adición de [2+2] a veces se conoce como “permitida fotolíticamente”. Esta distinción se refiere a la necesidad de excitación electrónica para lograr este último tipo de reacción.

