1.2: Lo que hacen los químicos
- Page ID
- 76232
![Por Kurt Barnett (UNSW Canberra) [CC BY-SA 3.0 (http://creativecommons.org/licenses/by-sa/3.0)], vía Wikimedia Commons](https://upload.wikimedia.org/Wikipedia/commons/d/d2/Chemistry_Lab.jpg) ¿Cuáles son algunas de las cosas que hacen los químicos? Como la mayoría de los científicos, observan y miden componentes del mundo natural. A partir de estas observaciones intentan colocar las cosas en categorías útiles y apropiadas y formular leyes científicas que resuman los resultados de muchas observaciones. En efecto, es una creencia fundamental de toda la ciencia que los eventos naturales no ocurren de una manera completamente impredecible. En cambio, obedecen las leyes naturales. Por lo tanto, las observaciones y medidas realizadas en una ocasión pueden ser duplicadas por la misma u otra persona en otra ocasión. La comunicación de dichos resultados, otra actividad importante, brinda una oportunidad para que toda la comunidad científica pruebe el trabajo de un individuo. Eventualmente se llega a un consenso, y hay acuerdo sobre una nueva ley.
¿Cuáles son algunas de las cosas que hacen los químicos? Como la mayoría de los científicos, observan y miden componentes del mundo natural. A partir de estas observaciones intentan colocar las cosas en categorías útiles y apropiadas y formular leyes científicas que resuman los resultados de muchas observaciones. En efecto, es una creencia fundamental de toda la ciencia que los eventos naturales no ocurren de una manera completamente impredecible. En cambio, obedecen las leyes naturales. Por lo tanto, las observaciones y medidas realizadas en una ocasión pueden ser duplicadas por la misma u otra persona en otra ocasión. La comunicación de dichos resultados, otra actividad importante, brinda una oportunidad para que toda la comunidad científica pruebe el trabajo de un individuo. Eventualmente se llega a un consenso, y hay acuerdo sobre una nueva ley.
Al igual que otros científicos, los químicos tratan de explicar sus observaciones y leyes por medio de teorías o modelos. Constantemente hacen uso de átomos, moléculas y otras partículas muy pequeñas. Usando tales teorías como sus guías, los químicos sintetizan nuevos materiales. Ahora se conocen más de 3 millones de compuestos, y más de 9000 se encuentran en producción comercial a gran escala. Incluso un mochilero que “vuelve a la naturaleza” lleva consigo materiales sintéticos como nylon, aluminio y aspirina.
Los químicos también analizan las sustancias que elaboran y las que se encuentran en la naturaleza. Determinar la composición de una sustancia es el primer paso para comprender sus propiedades químicas, y la detección de cantidades muy pequeñas de algunos materiales en el mundo natural es esencial para controlar la contaminación del aire y del agua. Otro papel que juegan los químicos es en el estudio de los procesos (reacciones químicas) por los cuales una sustancia puede transformarse en otra. ¿Las reacciones ocurrirán sin pinchar? Si es así, ¿qué tan rápido? ¿Se desprende energía? ¿Se pueden controlar las reacciones, hacer que ocurran solo cuando queremos que lo hagan?
Estos y muchos otros problemas que interesan a los químicos son el tema de este libro de texto en línea. Volveremos a cada una varias veces y en cada vez mayor detalle. No olvides, sin embargo, que la química es más que solo lo que hacen los químicos. Muchas personas en otras ciencias así como en la vida cotidiana están constantemente haciendo química, ya sea que la llamen por su nombre o no. De hecho, cada uno de nosotros es una intrincada combinación de químicos, y todo lo que hacemos depende de las reacciones químicas. Aunque las limitaciones de espacio nos impedirán explorar todas menos una fracción de las aplicaciones de la química a otros campos, hemos incluido tales excursiones tantas veces como nos parecieron apropiadas. De ellos esperamos que puedas aprender a aplicar hechos y principios químicos a los problemas que enfrentarás en el futuro. Muchos de los problemas probablemente aún no se conocen, y no podríamos anticiparlos. Si has aprendido a pensar “químicamente” o “científicamente”, sin embargo, creemos que estarás mejor preparado para enfrentarlos.
Elementos, Compuestos y Mezclas
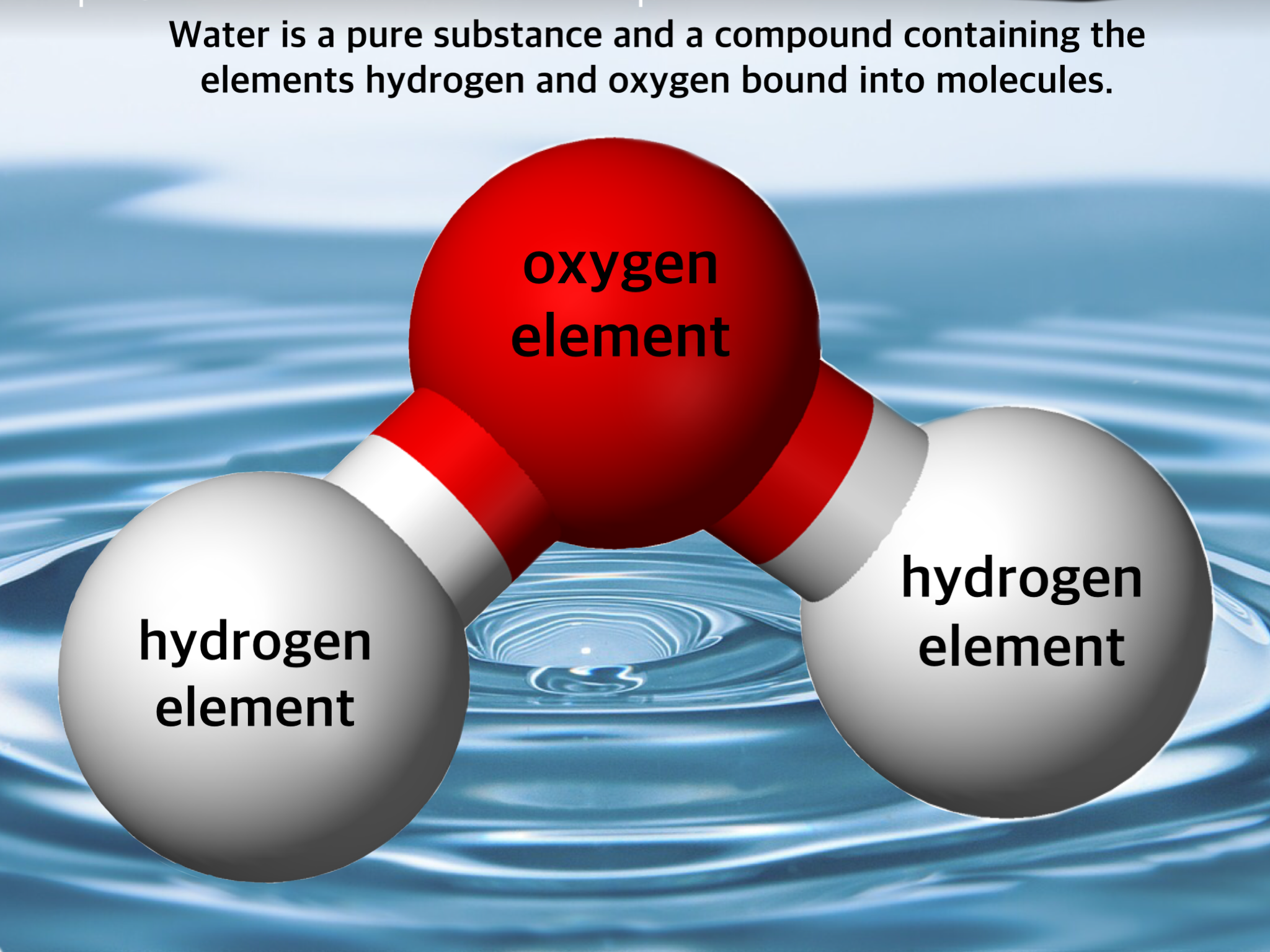 Los químicos tienen una manera única de caracterizar los objetos de su estudio. Para un químico, la materia que contiene un tipo de átomo o molécula se considera una sustancia pura, por lo que el agua (H 2 O) y el aluminio metálico (Al) son sustancias puras. Para un químico, el aluminio es un elemento, el tipo más simple de sustancia pura que contiene solo un tipo de átomo (un físico podría considerar al aluminio una “mezcla” muy compleja de cosas como leptones, protones, quarks).
Los químicos tienen una manera única de caracterizar los objetos de su estudio. Para un químico, la materia que contiene un tipo de átomo o molécula se considera una sustancia pura, por lo que el agua (H 2 O) y el aluminio metálico (Al) son sustancias puras. Para un químico, el aluminio es un elemento, el tipo más simple de sustancia pura que contiene solo un tipo de átomo (un físico podría considerar al aluminio una “mezcla” muy compleja de cosas como leptones, protones, quarks).
Para un químico, la sustancia pura agua es un compuesto (contiene dos tipos de átomos unidos entre sí en un solo tipo de molécula). Un ambientalista podría considerar que el agua es “pura” aunque contenga la cantidad normal de oxígeno disuelto y dióxido de carbono, pero no otros “contaminantes”. Para un químico, el agua que contiene oxígeno ya no es una sustancia pura, sino una mezcla. En agua pura, la relación de hidrógeno a átomos de oxígeno es siempre 2:1, pero tan pronto como el oxígeno se disuelve en el agua, la relación ya no es fija (porque el oxígeno no forma una nueva molécula al reaccionar con H 2 O), un signo seguro de impureza a un químico.
Reacciones Químicas
 Debido a que el oxígeno disuelto no reacciona con el agua para formar un nuevo compuesto, consideramos que “disolver” es un proceso físico (uno que no se entiende en términos de átomos o moléculas y formación o ruptura de enlaces). Cambios como la disolución, evaporación y condensación se consideran “cambios físicos” porque, si bien son cambios claramente interesantes, pueden ser estudiados en física sin referencia a recombinaciones atómicas. Sin embargo, si el oxígeno disuelto es utilizado por un pez para convertir los alimentos en dióxido de carbono (CO 2) y agua (H 2 O), se ha producido una reacción química, porque el proceso se entiende mejor a nivel de átomos, moléculas y enlaces entre ellos. El proceso por el cual el oxígeno disuelto es absorbido por los peces podría considerarse un “proceso biológico” porque el conocimiento de la estructura celular de las branquias de los peces es importante en su comprensión. Una vez más, el modo de entender es más importante que el tema de estudio para determinar si un proceso es considerado “químico”, “físico” o “biológico”. Más adelante en este libro, utilizaremos conceptos atómicos y moleculares como la formación de enlaces no covalentes para entender la disolución, y entonces probablemente debería considerarse un proceso químico, y quedará claro que ninguna distinción absoluta entre procesos físicos y químicos es posible (o necesaria).
Debido a que el oxígeno disuelto no reacciona con el agua para formar un nuevo compuesto, consideramos que “disolver” es un proceso físico (uno que no se entiende en términos de átomos o moléculas y formación o ruptura de enlaces). Cambios como la disolución, evaporación y condensación se consideran “cambios físicos” porque, si bien son cambios claramente interesantes, pueden ser estudiados en física sin referencia a recombinaciones atómicas. Sin embargo, si el oxígeno disuelto es utilizado por un pez para convertir los alimentos en dióxido de carbono (CO 2) y agua (H 2 O), se ha producido una reacción química, porque el proceso se entiende mejor a nivel de átomos, moléculas y enlaces entre ellos. El proceso por el cual el oxígeno disuelto es absorbido por los peces podría considerarse un “proceso biológico” porque el conocimiento de la estructura celular de las branquias de los peces es importante en su comprensión. Una vez más, el modo de entender es más importante que el tema de estudio para determinar si un proceso es considerado “químico”, “físico” o “biológico”. Más adelante en este libro, utilizaremos conceptos atómicos y moleculares como la formación de enlaces no covalentes para entender la disolución, y entonces probablemente debería considerarse un proceso químico, y quedará claro que ninguna distinción absoluta entre procesos físicos y químicos es posible (o necesaria).
Homogéneos y heterogéneos
Es interesante que el agua que contiene cubitos de hielo es una sustancia pura para un químico (solo las moléculas H 2 O están presentes), pero es heterogénea. A un químico, “heterogéneo” no indica “impureza”, ni “homogéneo” indica pureza. El oxígeno (o sal) disuelto en el agua es una mezcla homogénea, porque cada parte de ella se parece a cada otra parte. Por supuesto, cuando decimos “homogéneo” solemos suponer que la sustancia no se está observando con nada con mayor aumento que un microscopio crudo.


