1.4: Una descripción de la materia
- Page ID
- 78202
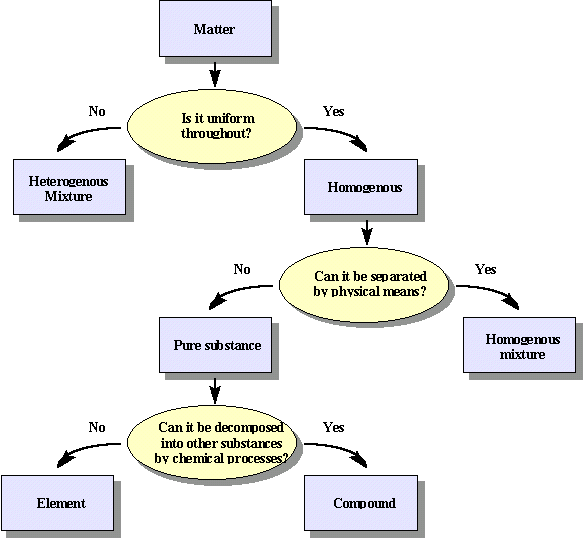
Las sustancias puras tienen una composición invariable y están compuestas por elementos o compuestos.
- Elementos: “Sustancias que no pueden descomponerse en sustancias más simples por medios químicos”.
- Compuestos: Se pueden descomponer en dos o más elementos.
Elementos
Los elementos son las sustancias básicas a partir de las cuales se compone toda la materia.
- Todo en el mundo está conformado por sólo 109 elementos diferentes.
- El 90% del cuerpo humano está compuesto por solo tres elementos: Oxígeno, Carbono e Hidrógeno
Los elementos son conocidos por nombres comunes así como por sus abreviaturas. Éstas constan de una o dos letras, con la primera en mayúscula. Estas abreviaturas se derivan de palabras inglesas o extranjeras (por ejemplo, latín, alemán).
| Element | Abreviatura |
| Carbono | C |
| Flúor | F |
| Hidrógeno | H |
| Yodo | I |
| Nitrógeno | N |
| Oxígeno | O |
| Fosforo | P |
| Azufre | S |
| Aluminio | Al |
| Bario | Ba |
| Calcio | Ca |
| Cloro | Cl |
| Helio | Él |
| Magnesio | Mg |
| Platino | Pt |
| Silicio | Si |
| Cobre | Cu (de cuprum) |
| Hierro | Fe (de ferrum) |
| Plomo | Pb (de plumbum) |
| Mercurio | Hg (de hidrargiro) |
| Potasio | K (de kalium) |
| Plata | Ag (de argentum) |
| Sodio | Na (de natrium) |
| Estaño | Sn (de stannum) |
Diferentes Definiciones de Materia: https://youtu.be/qi_qLHc8wLk
Compuestos
Los compuestos son sustancias de dos o más elementos unidos químicamente en proporciones definidas en masa. Por ejemplo, el agua pura está compuesta por los elementos hidrógeno (H) y oxígeno (O) en la relación definida de 11% de hidrógeno y 89% de oxígeno en masa.
La observación de que la composición elemental de un compuesto puro es siempre la misma se conoce como la ley de la composición constante (o la ley de proporciones definidas). Se le atribuye al químico francés Joseph Louis Proust (1754-1826).


