4.2: Clasificación de reacciones químicas
- Page ID
- 75877
- Definir tres tipos comunes de reacciones químicas (precipitación, ácido-base y oxidación-reducción)
- Clasificar las reacciones químicas como uno de estos tres tipos dadas las descripciones apropiadas o ecuaciones químicas
- Identificar ácidos y bases comunes
- Predecir la solubilidad de compuestos inorgánicos comunes mediante el uso de reglas de solubilidad
- Calcular los estados de oxidación para elementos en compuestos
Los humanos interactúan entre sí de formas diversas y complejas, y clasificamos estas interacciones de acuerdo con patrones comunes de comportamiento. Cuando dos humanos intercambian información, decimos que se están comunicando. Cuando intercambian golpes con sus puños o pies, decimos que están peleando. Ante una amplia gama de interacciones variadas entre sustancias químicas, los científicos también han encontrado conveniente (o incluso necesario) clasificar las interacciones químicas mediante la identificación de patrones comunes de reactividad. Este módulo proporcionará una introducción a tres de los tipos de reacciones químicas más prevalentes: precipitación, ácido-base y oxidación-reducción.
Reacciones de precipitación y reglas de solubilidad
Una reacción de precipitación es aquella en la que las sustancias disueltas reaccionan para formar uno (o más) productos sólidos. Muchas reacciones de este tipo implican el intercambio de iones entre compuestos iónicos en solución acuosa y a veces se denominan reacciones de doble desplazamiento, doble reemplazo o metátesis. Estas reacciones son comunes en la naturaleza y son responsables de la formación de arrecifes de coral en aguas oceánicas y cálculos renales en animales. Se utilizan ampliamente en la industria para la producción de una serie de productos básicos y productos químicos especiales. Las reacciones de precipitación también juegan un papel central en muchas técnicas de análisis químico, incluyendo pruebas puntuales utilizadas para identificar iones metálicos y métodos gravimétricos para determinar la composición de la materia (ver el último módulo de este capítulo).
El grado en que una sustancia puede disolverse en agua, o cualquier disolvente, se expresa cuantitativamente como su solubilidad, definida como la concentración máxima de una sustancia que se puede lograr en condiciones especificadas. Se dice que las sustancias con solubilidades relativamente grandes son solubles. Una sustancia precipitará cuando las condiciones de la solución sean tales que su concentración exceda su solubilidad. Se dice que las sustancias con solubilidades relativamente bajas son insolubles, y estas son las sustancias que precipitan fácilmente de la solución. Se brinda más información sobre estos importantes conceptos en el capítulo de texto sobre soluciones. Para fines de predecir las identidades de los sólidos formados por las reacciones de precipitación, se puede referir simplemente a patrones de solubilidad que se han observado para muchos compuestos iónicos (Tabla\(\PageIndex{1}\)).
| Los compuestos solubles contienen | Las excepciones a estas reglas de solubilidad incluyen |
|
|
| Los compuestos insolubles contienen | Las excepciones a estas reglas de insolubilidad incluyen |
|
|
Un vívido ejemplo de precipitación se observa cuando se mezclan soluciones de yoduro de potasio y nitrato de plomo, dando como resultado la formación de yoduro de plomo sólido:
\[\ce{2KI}(aq)+\ce{Pb(NO3)2}(aq)\rightarrow \ce{PbI2}(s)+\ce{2KNO3}(aq) \nonumber \]
Esta observación es consistente con las pautas de solubilidad: El único compuesto insoluble entre todos los involucrados es el yoduro de plomo, una de las excepciones a la solubilidad general de las sales yoduro.
La ecuación iónica neta que representa esta reacción es:
\[\ce{Pb^2+}(aq)+\ce{2I-}(aq)\rightarrow \ce{PbI2}(s) \nonumber \]
El yoduro de plomo es un sólido amarillo brillante que anteriormente se usaba como pigmento de artista conocido como amarillo yodo (Figura\(\PageIndex{1}\)). Las propiedades de los cristales puros de PbI 2 los hacen útiles para la fabricación de detectores de rayos X y rayos gamma.

Las pautas de solubilidad en la Tabla\(\PageIndex{1}\) pueden usarse para predecir si ocurrirá una reacción de precipitación cuando se mezclen soluciones de compuestos iónicos solubles. Uno simplemente necesita identificar todos los iones presentes en la solución y luego considerar si es posible el emparejamiento catión/anión podría resultar en un compuesto insoluble. Por ejemplo, la mezcla de soluciones de nitrato de plata y fluoruro de sodio producirá una solución que contiene iones Ag +\(\ce{NO3-}\), Na + y F −. Aparte de los dos compuestos iónicos originalmente presentes en las soluciones, AgnO 3 y NaF, se pueden derivar dos compuestos iónicos adicionales de esta colección de iones: NaNO 3 y AgF. Las pautas de solubilidad indican que todas las sales de nitrato son solubles pero que el AgF es una de las excepciones a la solubilidad general de las sales de fluoruro. Por lo tanto, se predice que se produzca una reacción de precipitación, como se describe en las siguientes ecuaciones:
\[\ce{NaF}(aq)+\ce{AgNO3}(aq)\rightarrow \ce{AgF}(s)+\ce{NaNO3}(aq)\hspace{20px}\ce{(molecular)} \nonumber \]
\[\ce{Ag+}(aq)+\ce{F-}(aq)\rightarrow \ce{AgF}(s)\hspace{20px}\ce{(net\: ionic)} \nonumber \]
Predecir el resultado de mezclar soluciones razonablemente concentradas de los siguientes compuestos iónicos. Si se espera precipitación, escriba una ecuación iónica neta equilibrada para la reacción.
- sulfato de potasio y nitrato de bario
- cloruro de litio y acetato de plata
- nitrato de plomo y carbonato de amonio
Solución
(a) Los dos posibles productos para esta combinación son KNO 3 y BaSO 4. Las pautas de solubilidad indican que BaSO 4 es insoluble, por lo que se espera una reacción de precipitación. La ecuación iónica neta para esta reacción, derivada de la manera detallada en el módulo anterior, es
\[\ce{Ba^2+}(aq)+\ce{SO4^2-}(aq)\rightarrow \ce{BaSO4}(s) \nonumber \]
(b) Los dos posibles productos para esta combinación son LiC 2 H 3 O 2 y AgCl. Las pautas de solubilidad indican que AgCl es insoluble, por lo que se espera una reacción de precipitación. La ecuación iónica neta para esta reacción, derivada de la manera detallada en el módulo anterior, es
\[\ce{Ag+}(aq)+\ce{Cl-}(aq)\rightarrow \ce{AgCl}(s) \nonumber \]
(c) Los dos posibles productos para esta combinación son PbCo 3 y NH 4 NO 3. Las pautas de solubilidad indican que PbCO 3 es insoluble, por lo que se espera una reacción de precipitación. La ecuación iónica neta para esta reacción, derivada de la manera detallada en el módulo anterior, es
\[\ce{Pb^2+}(aq)+\ce{CO3^2-}(aq)\rightarrow \ce{PbCO3}(s) \nonumber \]
¿Qué solución podría usarse para precipitar el ion bario, Ba 2 +, en una muestra de agua: cloruro de sodio, hidróxido de sodio o sulfato de sodio? ¿Cuál es la fórmula para el precipitado esperado?
- Contestar
-
sulfato de sodio, BaSO 4
Reacciones ácido-base
Una reacción ácido-base es aquella en la que un ión hidrógeno, H +, se transfiere de una especie química a otra. Tales reacciones son de importancia central para numerosos procesos naturales y tecnológicos, que van desde las transformaciones químicas que tienen lugar dentro de las células y los lagos y océanos, hasta la producción a escala industrial de fertilizantes, productos farmacéuticos y otras sustancias esenciales para la sociedad. El tema de la química ácido-base, por lo tanto, es digno de una discusión a fondo, y se dedica un capítulo completo a este tema más adelante en el texto.
Para propósitos de esta breve introducción, consideraremos solo los tipos más comunes de reacciones ácido-base que tienen lugar en soluciones acuosas. En este contexto, un ácido es una sustancia que se disolverá en agua para producir iones hidronio, H 3 O +. Como ejemplo, considere la ecuación que se muestra aquí:
\[\ce{HCl}(aq)+\ce{H2O}(aq)\rightarrow \ce{Cl-}(aq)+\ce{H3O+}(aq) \nonumber \]
El proceso representado por esta ecuación confirma que el cloruro de hidrógeno es un ácido. Cuando se disuelven en agua, los iones H 3 O + se producen mediante una reacción química en la que los iones H + se transfieren de moléculas de HCl a moléculas de H 2 O (Figura\(\PageIndex{2}\)).
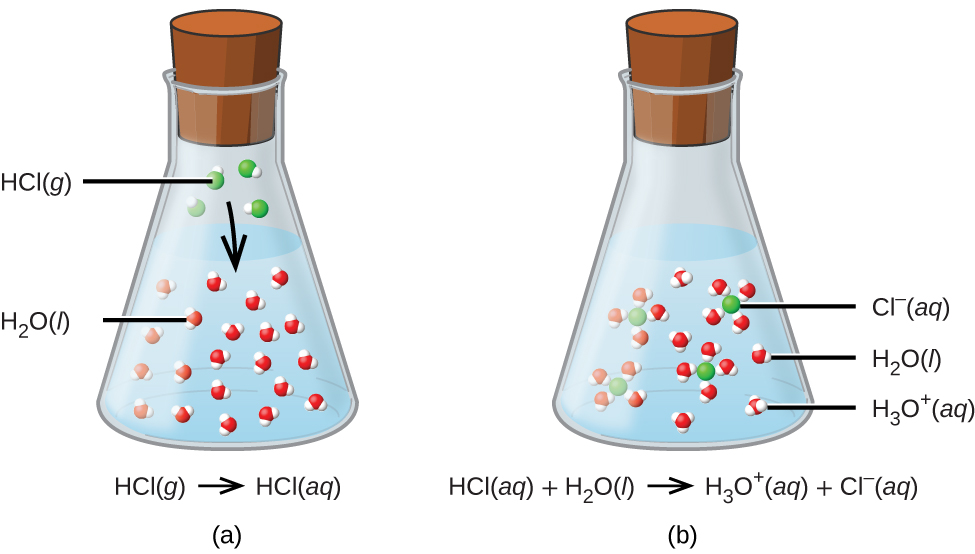
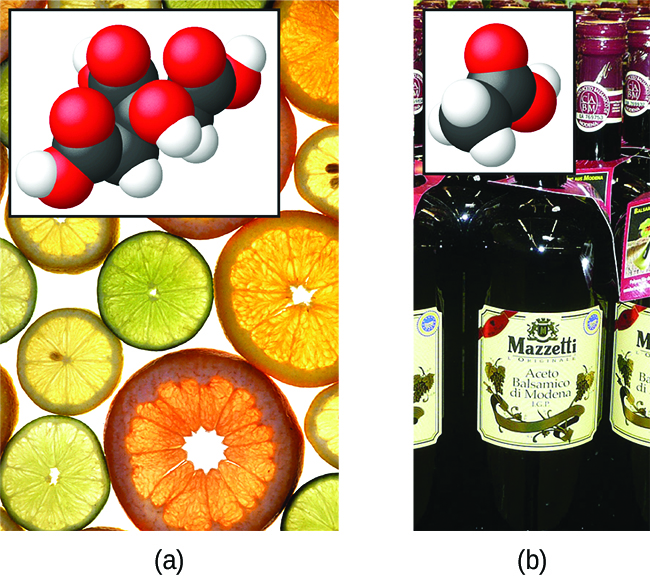
La naturaleza del HCl es tal que su reacción con agua como se acaba de describir es esencialmente 100% eficiente: Prácticamente todas las moléculas de HCl que se disuelvan en agua sufrirán esta reacción. Los ácidos que reaccionan completamente de esta manera se denominan ácidos fuertes, y el HCl es uno entre solo un puñado de compuestos ácidos comunes que se clasifican como fuertes (Tabla\(\PageIndex{1}\)). Un número mucho mayor de compuestos se comportan como ácidos débiles y solo reaccionan parcialmente con el agua, dejando una gran mayoría de moléculas disueltas en su forma original y generando una cantidad relativamente pequeña de iones hidronio. Los ácidos débiles se encuentran comúnmente en la naturaleza, siendo las sustancias en parte responsables del sabor picante de los cítricos, la sensación punzante de las picaduras de insectos y los olores desagradables asociados con el olor corporal. Un ejemplo familiar de un ácido débil es el ácido acético, el ingrediente principal de los vinagres alimentarios:
\[\ce{CH3CO2H}(aq)+\ce{H2O}(l)\rightleftharpoons \ce{CH3CO2-}(aq)+\ce{H3O+}(aq) \nonumber \]
Cuando se disuelve en agua en condiciones típicas, solo alrededor del 1% de las moléculas de ácido acético están presentes en la forma ionizada,\(\ce{CH3CO2-}\) (Figura\(\PageIndex{3}\)). (El uso de una doble flecha en la ecuación anterior denota el aspecto de reacción parcial de este proceso, concepto abordado completamente en los capítulos sobre equilibrio químico).
| Fórmula del compuesto | Nombre en Solución Acuosa |
|---|---|
| HBr | ácido bromhídrico |
| HCl | ácido clorhídrico |
| HI | ácido yodhídrico |
| HNO 3 | ácido nítrico |
| HClO 4 | ácido perclórico |
| H 2 SO 4 | ácido sulfúrico |
Una base es una sustancia que se disolverá en agua para producir iones hidróxido, OH −. Las bases más comunes son los compuestos iónicos compuestos por cationes de metales alcalinos o alcalinotérreos (grupos 1 y 2) combinados con el ion hidróxido, por ejemplo, NaOH y Ca (OH) 2. Cuando estos compuestos se disuelven en agua, los iones hidróxido se liberan directamente en la solución. Por ejemplo, KOH y Ba (OH) 2 se disuelven en agua y se disocian completamente para producir cationes (K + y Ba 2 +, respectivamente) e iones hidróxido, OH −. Estas bases, junto con otros hidróxidos que se disocian completamente en el agua, se consideran bases fuertes.
Consideremos como ejemplo la disolución de lejía (hidróxido de sodio) en agua:
\[\ce{NaOH}(s)\rightarrow \ce{Na+}(aq)+\ce{OH-}(aq) \nonumber \]
Esta ecuación confirma que el hidróxido de sodio es una base. Cuando se disuelve en agua, el NaOH se disocia para producir iones Na + y OH −. Esto también es cierto para cualquier otro compuesto iónico que contenga iones hidróxido. Dado que el proceso de disociación es esencialmente completo cuando los compuestos iónicos se disuelven en agua en condiciones típicas, el NaOH y otros hidróxidos iónicos se clasifican como bases fuertes.
A diferencia de los hidróxidos iónicos, algunos compuestos producen iones hidróxido cuando se disuelven al reaccionar químicamente con moléculas de agua. En todos los casos, estos compuestos reaccionan sólo parcialmente y así se clasifican como bases débiles. Estos tipos de compuestos también son abundantes en la naturaleza e importantes productos básicos en diversas tecnologías. Por ejemplo, la producción global del amoníaco de base débil suele superar las 100 toneladas métricas anuales, siendo ampliamente utilizada como fertilizante agrícola, materia prima para la síntesis química de otros compuestos y ingrediente activo en limpiadores domésticos (Figura\(\PageIndex{4}\)). Cuando se disuelve en agua, el amoníaco reacciona parcialmente para producir iones hidróxido, como se muestra aquí:
\[\ce{NH3}(aq)+\ce{H2O}(l)\rightleftharpoons \ce{NH4+}(aq)+\ce{OH-}(aq) \nonumber \]
Se trata, por definición, de una reacción ácido-base, en este caso implicando la transferencia de iones H + de moléculas de agua a moléculas de amoníaco. En condiciones típicas, solo alrededor del 1% del amoníaco disuelto está presente como\(\ce{NH4+}\) iones.

Las reacciones químicas descritas en las que ácidos y bases disueltas en agua producen iones hidronio e hidróxido, respectivamente, son, por definición, reacciones ácido-base. En estas reacciones, el agua sirve tanto como disolvente como reactivo. Una reacción de neutralización es un tipo específico de reacción ácido-base en la que los reactivos son un ácido y una base, los productos son a menudo una sal y agua, y ninguno de los reactivos es el agua misma:
\[\mathrm{acid+base\rightarrow salt+water} \nonumber \]
Para ilustrar una reacción de neutralización, considere lo que sucede cuando se ingiere un antiácido típico como la leche de magnesia (una suspensión acuosa de Mg (OH) 2 sólido) para aliviar los síntomas asociados al exceso de ácido estomacal (HCl):
\[\ce{Mg(OH)2}(s)+\ce{2HCl}(aq)\rightarrow \ce{MgCl2}(aq)+\ce{2H2O}(l). \nonumber \]
Tenga en cuenta que además del agua, esta reacción produce una sal, cloruro de magnesio.
Escriba ecuaciones químicas balanceadas para las reacciones ácido-base descritas aquí:
- el hipoclorito de hidrógeno ácido débil reacciona con el agua
- una solución de hidróxido de bario se neutraliza con una solución de ácido nítrico
Solución
(a) Se proporcionan los dos reactivos, HOCl y H 2 O. Dado que se reporta que la sustancia es un ácido, su reacción con agua implicará la transferencia de H + de HOCl a H 2 O para generar iones hidronio, H 3 O + e iones hipoclorito, OCl − .
\[\ce{HOCl}(aq)+\ce{H2O}(l)\rightleftharpoons \ce{OCl-}(aq)+\ce{H3O+}(aq) \nonumber \]
Una flecha doble es apropiada en esta ecuación porque indica que el HOCl es un ácido débil que no ha reaccionado completamente.
(b) Se proporcionan los dos reactivos, Ba (OH) 2 y HNO 3. Al tratarse de una reacción de neutralización, los dos productos serán agua y una sal compuesta por el catión del hidróxido iónico (Ba 2 +) y el anión generado cuando el ácido transfiere su ión hidrógeno\(\ce{(NO3- )}\).
\[\ce{Ba(OH)2}(aq)+\ce{2HNO3}(aq)\rightarrow \ce{Ba(NO3)2}(aq)+\ce{2H2O}(l) \nonumber \]
Escriba la ecuación iónica neta que representa la neutralización de cualquier ácido fuerte con un hidróxido iónico. (Pista: Considere los iones producidos cuando un ácido fuerte se disuelve en agua.)
- Contestar
-
\[\ce{H3O+}(aq)+\ce{OH-}(aq)\rightarrow \ce{2H2O}(l) \nonumber \]
Explore la visión microscópica de ácidos y bases fuertes y débiles.
Reacciones de oxidación-reducción
La atmósfera terrestre contiene alrededor de 20% de oxígeno molecular, O 2, un gas químicamente reactivo que juega un papel esencial en el metabolismo de los organismos aeróbicos y en muchos procesos ambientales que dan forma al mundo. El término oxidación se utilizó originalmente para describir reacciones químicas que involucran O 2, pero su significado ha evolucionado para referirse a una amplia e importante clase de reacción conocida como reacciones de oxidación-reducción (redox). Se emplearán algunos ejemplos de tales reacciones para desarrollar una imagen clara de esta clasificación.
Algunas reacciones redox implican la transferencia de electrones entre especies reaccionantes para producir productos iónicos, como la reacción entre sodio y cloro para producir cloruro de sodio:
\[\ce{2Na}(s)+\ce{Cl2}(g)\rightarrow \ce{2NaCl}(s) \nonumber \]
Es útil ver el proceso con respecto a cada reactivo individual, es decir, representar el destino de cada reactivo en forma de una ecuación llamada media reacción:
\[ \begin{align*} \ce{2Na}(s) &\rightarrow \ce{2Na+}(s)+\ce{2e-} \\[4pt] \ce{Cl2}(g)+\ce{2e-} &\rightarrow \ce{2Cl-}(s) \end{align*} \nonumber \]
Estas ecuaciones muestran que los átomos de Na pierden electrones mientras que los átomos de Cl (en la molécula de Cl 2) ganan electrones, los subíndices “s” para los iones resultantes significan que están presentes en forma de un compuesto iónico sólido. Para reacciones redox de este tipo, la pérdida y ganancia de electrones definen los procesos complementarios que ocurren:
\ (\ begin {align}
\ textbf {oxidación} &=\ textrm {pérdida de electrones}\\
\ textbf {reducción} &=\ textrm {ganancia de electrones}
\ end {align}\)
En esta reacción, entonces, el sodio se oxida y el cloro sufre reducción. Visto desde una perspectiva más activa, el sodio funciona como un agente reductor (reductor), ya que proporciona electrones a (o reduce) el cloro. Asimismo, el cloro funciona como un agente oxidante (oxidante), ya que efectivamente elimina electrones del (oxida) sodio.
\ (\ begin {align}
\ textbf {agente reductor} &=\ textrm {especie que se oxida}\
\ textbf {agente oxidante} &=\ textrm {especie que se reduce}
\ end {align}\)
Algunos procesos redox, sin embargo, no implican la transferencia de electrones. Consideremos, por ejemplo, una reacción similar a la que produce\(\ce{NaCl}\):
\[\ce{H2}(g)+\ce{Cl2}(g)\rightarrow \ce{2HCl}(g) \nonumber \]
El producto de esta reacción es un compuesto covalente, por lo que la transferencia de electrones en el sentido explícito no está involucrada. Para aclarar la similitud de esta reacción con la anterior y permitir una definición inequívoca de las reacciones redox, se ha definido una propiedad llamada número de oxidación. El número de oxidación (o estado de oxidación) de un elemento en un compuesto es la carga que poseerían sus átomos si el compuesto fuera iónico. Las siguientes pautas se utilizan para asignar números de oxidación a cada elemento en una molécula o ion.
- El número de oxidación de un átomo en una sustancia elemental es cero.
- El número de oxidación de un ion monoatómico es igual a la carga del ion.
- Los números de oxidación para los no metales comunes generalmente se asignan de la siguiente manera:
- Hidrógeno: +1 cuando se combina con no metales, −1 cuando se combina con metales
- Oxígeno: −2 en la mayoría de los compuestos, a veces −1 (los llamados peróxidos,\(\ce{O2^2-}\)), muy raramente\(-\dfrac{1}{2}\) (los llamados superóxidos,\(\ce{O2-}\)), valores positivos cuando se combinan con F (los valores varían)
- Halógenos: −1 para F siempre, −1 para otros halógenos excepto cuando se combinan con oxígeno u otros halógenos (números de oxidación positivos en estos casos, valores variables)
- La suma de los números de oxidación para todos los átomos en una molécula o ion poliatómico es igual a la carga en la molécula o ion.
Nota: La convención apropiada para reportar cargos es escribir primero el número, seguido del signo (e.g., 2+), mientras que el número de oxidación se escribe con la secuencia invertida, signo seguido por número (e.g., +2). Esta convención tiene como objetivo enfatizar la distinción entre estas dos propiedades relacionadas.
Siga las pautas de esta sección del texto para asignar números de oxidación a todos los elementos de las siguientes especies:
- H 2 S
- \(\ce{SO3^2-}\)
- Na 2 SO 4
Solución
a) De acuerdo con la directriz 1, el número de oxidación para H es +1.
Usando este número de oxidación y la fórmula del compuesto, se puede usar la directriz 4 para calcular el número de oxidación para el azufre:
\(\ce{charge\: on\: H2S}=0=(2\times +1)+(1\times x)\)
\(x=0-(2\times +1)=-2\)
(b) La directriz 3 sugiere que el número de oxidación para el oxígeno es −2.
Usando este número de oxidación y la fórmula del ion, se puede usar la directriz 4 para calcular el número de oxidación para el azufre:
\(\ce{charge\: on\: SO3^2-}=-2=(3\times -2)+(1\times x)\)
\(x=-2-(3\times -2)=+4\)
(c) Para los compuestos iónicos, es conveniente asignar números de oxidación para el catión y anión por separado.
De acuerdo con la directriz 2, el número de oxidación para el sodio es +1.
Suponiendo el número de oxidación habitual para el oxígeno (−2 por la directriz 3), el número de oxidación para el azufre se calcula según las indicaciones de la directriz 4:
\(x=-2-(4\times -2)=+6\)
Asignar estados de oxidación a los elementos cuyos átomos están subrayados en cada uno de los siguientes compuestos o iones:
- K N O 3
- Al H 3
- \(\mathrm{\underline{N}H_4^+}\)
- \(\mathrm{\sideset{ }{_{\large{4}}^{-}}{H_2\underline{P}O}}\)
- Contestar a
-
N, +5
- Respuesta b
-
Al, +3
- Respuesta c
-
N, −3
- Respuesta d
-
P, +5
Usando el concepto de número de oxidación, se ha establecido una definición integral de reacción redox. Las reacciones de oxidación-reducción (redox) son aquellas en las que uno o más elementos involucrados experimentan un cambio en el número de oxidación. Si bien la gran mayoría de las reacciones redox implican cambios en el número de oxidación para dos o más elementos, existen algunas excepciones interesantes a esta regla como se muestra a continuación\). Las definiciones para los procesos complementarios de esta clase de reacción se revisan correspondientemente como se muestra aquí:
\ [\ begin {align}
\ textbf {oxidación} &=\ textrm {aumento en el número de oxidación}\\
\ textbf {reducción} &=\ textrm {disminución en el número de oxidación}
\ end {align}\ nonumber\]
Volviendo a las reacciones utilizadas para introducir este tema, ahora ambas pueden ser identificadas como procesos redox. En la reacción entre sodio y cloro para producir cloruro de sodio, el sodio se oxida (su número de oxidación aumenta de 0 en Na a +1 en NaCl) y el cloro se reduce (su número de oxidación disminuye de 0 en Cl 2 a -1 en NaCl). En la reacción entre hidrógeno molecular y cloro, el hidrógeno se oxida (su número de oxidación aumenta de 0 en H 2 a +1 en HCl) y el cloro se reduce (su número de oxidación disminuye de 0 en Cl 2 a -1 en HCl).
Se reconocen varias subclases de reacciones redox, incluyendo reacciones de combustión en las que el reductor (también llamado combustible) y el oxidante (a menudo, pero no necesariamente, oxígeno molecular) reaccionan vigorosamente y producen cantidades significativas de calor, y a menudo luz, en forma de llama. Las reacciones sólidas de cohete-combustible como la que se muestra a continuación son procesos de combustión. Una reacción propulsante típica en la que el aluminio sólido se oxida por perclorato de amonio se representa por esta ecuación:
\[\ce{10Al}(s)+\ce{6NH4ClO4}(s)\rightarrow \ce{4Al2O3}(s)+\ce{2AlCl3}(s)+\ce{12H2O}(g)+\ce{3N2}(g) \nonumber \]
Vea un breve video que muestra el disparo de prueba de un motor de cohete híbrido prototipo a pequeña escala planeado para su uso en el nuevo Sistema de Lanzamiento Espacial que está desarrollando la NASA. Los primeros motores que disparan a 3 s (llama verde) usan una mezcla de combustible líquido/oxidante, y el segundo, los motores más potentes que disparan a 4 s (llama amarilla) usan una mezcla sólida.
Las reacciones de desplazamiento único (reemplazo) son reacciones redox en las que un ion en solución se desplaza (o reemplaza) a través de la oxidación de un elemento metálico. Un ejemplo común de este tipo de reacción es la oxidación ácida de ciertos metales:
\[\ce{Zn}(s)+\ce{2HCl}(aq)\rightarrow \ce{ZnCl2}(aq)+\ce{H2}(g) \nonumber \]
Los elementos metálicos también pueden oxidarse mediante soluciones de otras sales metálicas; por ejemplo:
\[\ce{Cu}(s)+\ce{2AgNO3}(aq)\rightarrow \ce{Cu(NO3)2}(aq)+\ce{2Ag}(s) \nonumber \]
Esta reacción se puede observar colocando alambre de cobre en una solución que contiene una sal de plata disuelta. Los iones de plata en solución se reducen a plata elemental en la superficie del alambre de cobre, y los iones Cu 2 + resultantes se disuelven en la solución para producir un color azul característico (Figura\(\PageIndex{4}\)).

Identificar qué ecuaciones representan reacciones redox, proporcionando un nombre para la reacción si es apropiado. Para aquellas reacciones identificadas como redox, nombrar el oxidante y reductor.
- \(\ce{ZnCO3}(s)\rightarrow \ce{ZnO}(s)+\ce{CO2}(g)\)
- \(\ce{2Ga}(l)+\ce{3Br2}(l)\rightarrow \ce{2GaBr3}(s)\)
- \(\ce{2H2O2}(aq)\rightarrow \ce{2H2O}(l)+\ce{O2}(g)\)
- \(\ce{BaCl2}(aq)+\ce{K2SO4}(aq)\rightarrow \ce{BaSO4}(s)+\ce{2KCl}(aq)\)
- \(\ce{C2H4}(g)+\ce{3O2}(g)\rightarrow \ce{2CO2}(g)+\ce{2H2O}(l)\)
S olución
Las reacciones redox se identifican por definición si uno o más elementos experimentan un cambio en el número de oxidación.
- Esta no es una reacción redox, ya que los números de oxidación permanecen sin cambios para todos los elementos.
- Esta es una reacción redox. El galio se oxida, su número de oxidación aumenta de 0 en Ga (l) a +3 en GaBr 3 (s). El agente reductor es Ga (l). El bromo se reduce, su número de oxidación disminuye de 0 en Br 2 (l) a −1 en GaBr 3 (s). El agente oxidante es Br 2 (l).
- Esta es una reacción redox. Es un proceso particularmente interesante, ya que involucra al mismo elemento, el oxígeno, experimentando tanto oxidación como reducción (una llamada reacción de desproporción). El oxígeno se oxida, aumentando su número de oxidación de −1 en H 2 O 2 (aq) a 0 en O 2 (g). También se reduce el oxígeno, disminuyendo su número de oxidación de −1 en H 2 O 2 (aq) a −2 en H 2 O (l). Para las reacciones de desproporción, la misma sustancia funciona como oxidante y reductor.
- Esta no es una reacción redox, ya que los números de oxidación permanecen sin cambios para todos los elementos.
- Esta es una reacción redox (combustión). El carbono se oxida, su número de oxidación aumenta de −2 en C 2 H 4 (g) a +4 en CO 2 (g). El agente reductor (combustible) es C 2 H 4 (g). El oxígeno se reduce, su número de oxidación disminuye de 0 en O 2 (g) a −2 en H 2 O (l). El agente oxidante es O 2 (g).
Esta ecuación describe la producción de cloruro de estaño (II):
\[\ce{Sn}(s)+\ce{2HCl}(g)\rightarrow \ce{SnCl2}(s)+\ce{H2}(g) \nonumber \]
¿Es esta una reacción redox? Si es así, proporcione un nombre más específico para la reacción en su caso, e identifique el oxidante y el reductor.
- Contestar
-
Sí, una reacción de reemplazo único. Sn (s) es el reductor, HCl (g) es el oxidante.
Equilibrar las reacciones redox mediante el método de media reacción
Las reacciones redox que tienen lugar en medios acuosos a menudo involucran agua, iones hidronio e iones hidróxido como reactivos o productos. Aunque estas especies no se oxidan ni se reducen, sí participan en el cambio químico de otras maneras (por ejemplo, proporcionando los elementos necesarios para formar oxianiones). Las ecuaciones que representan estas reacciones son a veces muy difíciles de equilibrar por inspección, por lo que se han desarrollado enfoques sistemáticos para ayudar en el proceso. Un enfoque muy útil es utilizar el método de medias reacciones, que implica los siguientes pasos:
- Escribe las dos medias reacciones que representan el proceso redox.
- Equilibrar todos los elementos excepto oxígeno e hidrógeno.
- Equilibrar los átomos de oxígeno añadiendo moléculas de H 2 O.
- Equilibrar los átomos de hidrógeno añadiendo iones H +.
- Equilibra la carga 1 mediante la adición de electrones.
- Si es necesario, multiplique los coeficientes de cada media reacción por los números enteros más pequeños posibles para producir números iguales de electrones en cada uno.
- Sumar las medias reacciones equilibradas y simplificar eliminando especies que aparecen en ambos lados de la ecuación.
- Para las reacciones que ocurren en medios básicos (exceso de iones hidróxido), lleve a cabo estas etapas adicionales:
- Agregue iones OH − a ambos lados de la ecuación en números iguales al número de iones H +.
- En el lado de la ecuación que contiene iones H + y OH −, combine estos iones para producir moléculas de agua.
- Simplifique la ecuación eliminando cualquier molécula de agua redundante.
- Por último, comprobar para ver que tanto el número de átomos como las cargas totales 2 están equilibradas.
Escribir una ecuación equilibrada para la reacción entre el ion dicromato y el hierro (II) para producir hierro (III) y cromo (III) en solución ácida.
\[\ce{Cr2O7^2- + Fe^2+ \rightarrow Cr^3+ + Fe^3+} \nonumber \]
S olución
Escribe las dos medias reacciones.
Cada media reacción contendrá un reactivo y un producto con un elemento en común.
\(\ce{Cr2O7^2- \rightarrow Cr^3+}\)
Equilibrar todos los elementos excepto oxígeno e hidrógeno. La semi-reacción de hierro ya está equilibrada, pero la semirreacción de cromo muestra dos átomos de Cr a la izquierda y un átomo de Cr a la derecha. Al cambiar el coeficiente en el lado derecho de la ecuación a 2 se logra el equilibrio con respecto a los átomos de Cr.
\(\ce{Cr2O7^2- \rightarrow 2Cr^3+}\)
Equilibrar los átomos de oxígeno añadiendo moléculas de H 2 O. La semi-reacción de hierro no contiene átomos de O. La semirreacción de cromo muestra siete átomos de O a la izquierda y ninguno a la derecha, por lo que se agregan siete moléculas de agua al lado derecho.
\(\ce{Cr2O7^2- \rightarrow 2Cr^3+ + 7H2O}\)
Equilibrar los átomos de hidrógeno añadiendo iones H +. La semirreacción de hierro no contiene átomos de H. La semirreacción de cromo muestra 14 átomos de H a la derecha y ninguno a la izquierda, por lo que se agregan 14 iones hidrógeno al lado izquierdo.
\(\ce{Cr2O7^2- + 14H+ \rightarrow 2Cr^3+ + 7H2O}\)
Equilibrar la carga mediante la adición de electrones. La semi-reacción de hierro muestra una carga total de 2+ en el lado izquierdo (1 ion Fe 2 +) y 3+ en el lado derecho (1 ion Fe 3 +). Agregar un electrón al lado derecho lleva la carga total de ese lado a (3+) + (1−) = 2+, y se logra el equilibrio de carga.
La semirreacción de cromo muestra una carga total de (1 × 2−) + (14 × 1+) = 12+ en el lado izquierdo (\(\ce{1 Cr2O7^2-}\)iones y 14 iones H +). La carga total en el lado derecho es (2 × 3+) = 6 + (2 iones Cr 3 +). Agregar seis electrones al lado izquierdo traerá la carga total de ese lado a (12+ + 6−) = 6+, y se logra el equilibrio de carga.
\(\ce{Fe^2+ \rightarrow Fe^3+ + e-}\)
\(\ce{Cr2O7^2- + 14H+ + 6e- \rightarrow 2Cr^3+ + 7H2O}\)
Multiplique las dos medias reacciones para que el número de electrones en una reacción sea igual al número de electrones en la otra reacción. Para ser congruentes con la conservación de masas, y la idea de que las reacciones redox implican la transferencia (no creación o destrucción) de electrones, el coeficiente de la media reacción de hierro debe multiplicarse por 6.
\(\ce{6Fe^2+ \rightarrow 6Fe^3+ + 6e-}\)
\(\ce{Cr2O7^2- + 6e- + 14H+ \rightarrow 2Cr^3+ + 7H2O}\)
Agregar las medias reacciones equilibradas y cancelar las especies que aparecen en ambos lados de la ecuación.
\[\ce{6Fe^2+ + Cr2O7^2- + 6e- + 14H+ \rightarrow 6Fe^3+ + 6e- + 2Cr^3+ + 7H2O} \nonumber \]
Sólo los seis electrones son especies redundantes. Al eliminarlos de cada lado de la ecuación se obtiene la ecuación simplificada y equilibrada aquí:
\[\ce{6Fe^2+ + Cr2O7^2- + 14H+ \rightarrow 6Fe^3+ + 2Cr^3+ + 7H2O} \nonumber \]
Una comprobación final del balance de átomos y carga confirma que la ecuación está equilibrada.
| Reactivos | Productos | |
|---|---|---|
| Fe | 6 | 6 |
| Cr | 2 | 2 |
| O | 7 | 7 |
| H | 14 | 14 |
| cargar | 24+ | 24+ |
En solución ácida, el peróxido de hidrógeno reacciona con Fe 2 + para producir Fe 3 + y H 2 O. Escribe una ecuación equilibrada para esta reacción.
- Contestar
-
\[\ce{H2O2}(aq)+\ce{2H+}(aq)+\ce{2Fe^2+} \rightarrow \ce{2H2O}(l)+\ce{2Fe^3+} \nonumber \]
Resumen
Las reacciones químicas se clasifican de acuerdo con patrones de comportamiento similares. Un gran número de reacciones importantes se incluyen en tres categorías: precipitación, ácido-base y oxidación-reducción (redox). Las reacciones de precipitación implican la formación de uno o más productos insolubles. Las reacciones ácido-base implican la transferencia de iones de hidrógeno entre los reactivos. Las reacciones redox implican un cambio en el número de oxidación para uno o más elementos reactivos. Escribir ecuaciones equilibradas para algunas reacciones redox que ocurren en soluciones acuosas se simplifica mediante un enfoque sistemático llamado método de media reacción.
Notas al pie
- 1 El requisito de “equilibrio de carga” es solo un tipo específico de “balance de masa” en el que las especies en cuestión son electrones. Una ecuación debe representar números iguales de electrones en los lados del reactivo y del producto, por lo que tanto los átomos como las cargas deben estar equilibrados.
- 2 El requisito de “equilibrio de carga” es solo un tipo específico de “balance de masa” en el que las especies en cuestión son electrones. Una ecuación debe representar números iguales de electrones en los lados del reactivo y del producto, por lo que tanto los átomos como las cargas deben estar equilibrados.
Glosario
- ácido
- sustancia que produce H 3 O + cuando se disuelve en agua
- reacción ácido-base
- reacción que implica la transferencia de un ión hidrógeno entre especies reaccionantes
- base
- sustancia que produce OH − cuando se disuelve en agua
- reacción de combustión
- vigorosa reacción redox produciendo cantidades significativas de energía en forma de calor y, a veces, luz
- media reacción
- una ecuación que muestra si cada reactante pierde o gana electrones en una reacción.
- insoluble
- de solubilidad relativamente baja; disolviendo solo en un grado leve
- reacción de neutralización
- reacción entre un ácido y una base para producir sal y agua
- oxidación
- proceso en el que el número de oxidación de un elemento se incrementa por la pérdida de electrones
- reacción de oxidación-reducción
- (también, reacción redox) que implica un cambio en el número de oxidación para uno o más elementos reactivos
- número de oxidación
- (también, estado de oxidación) la carga que cada átomo de un elemento tendría en un compuesto si el compuesto fuera iónico
- agente oxidante
- (también, oxidante) sustancia que provoca la oxidación de otra sustancia, y en el proceso se reduce
- precipitar
- producto insoluble que se forma a partir de la reacción de reactivos solubles
- reacción de precipitación
- reacción que produce uno o más productos insolubles; cuando los reactivos son compuestos iónicos, a veces llamados doble desplazamiento o metátesis
- reducción
- proceso en el que el número de oxidación de un elemento se reduce por la ganancia de electrones
- agente reductor
- (también, reductor) sustancia que provoca la reducción de otra sustancia, y en el proceso se oxida
- sal
- compuesto iónico que se puede formar por la reacción de un ácido con una base que contiene un catión y un anión distinto de hidróxido u óxido
- reacción de desplazamiento único
- (también, reemplazo) reacción redox que implica la oxidación de una sustancia elemental por una especie iónica
- soluble
- de solubilidad relativamente alta; disolución en un grado relativamente grande
- solubilidad
- la medida en que una sustancia puede disolverse en agua, o cualquier disolvente
- ácido fuerte
- ácido que reacciona completamente cuando se disuelve en agua para producir iones hidronio
- base fuerte
- base que reacciona completamente cuando se disuelve en agua para producir iones hidróxido
- ácido débil
- ácido que reacciona solo en una pequeña medida cuando se disuelve en agua para producir iones hidronio
- base débil
- base que reacciona solo en un grado leve cuando se disuelve en agua para producir iones hidróxido

