6.15: Fundamentos de la Nomenclatura Orgánica
- Page ID
- 78806
41
Fundamentos de la Nomenclatura Orgánica
Alcanos
La Unión Internacional de Química Pura y Aplicada (IUPAC) ha ideado un sistema de nomenclatura que comienza con los nombres de los alcanos y se puede ajustar a partir de ahí para dar cuenta de estructuras más complicadas. La nomenclatura para alcanos se basa en dos reglas:
- Para nombrar un alcano, primero identificar la cadena más larga de átomos de carbono en su estructura. Una cadena de dos carbonos se llama etano; una cadena de tres carbonos, propano; y una cadena de cuatro carbonos, butano. Las cadenas más largas se nombran de la siguiente manera: pentano (cadena de cinco carbonos), hexano (6), heptano (7), octano (8), nonano (9) y decano (10).
- Agrega prefijos al nombre de la cadena más larga para indicar las posiciones y nombres de los sustituyentes. Los sustituyentes son ramificaciones o grupos funcionales que reemplazan a los átomos de hidrógeno en una cadena. La posición de un sustituyente o ramificación se identifica por el número del átomo de carbono al que está unido en la cadena. Numeramos los átomos de carbono en la cadena contando desde el extremo de la cadena más cercano a los sustituyentes. Los sustituyentes múltiples se nombran individualmente y se colocan en orden alfabético al frente del nombre.
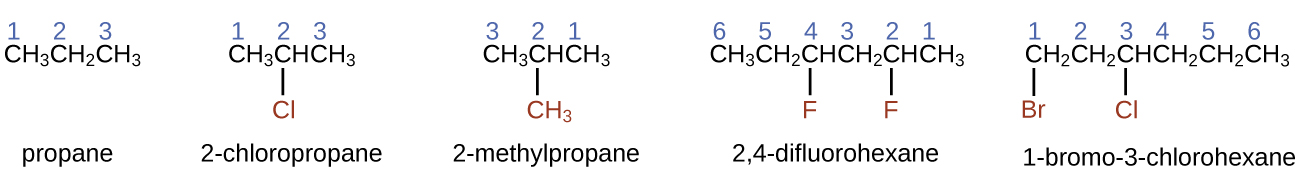
Cuando está presente más de un sustituyente, ya sea en el mismo átomo de carbono o en diferentes átomos de carbono, los sustituyentes se enumeran alfabéticamente. Debido a que la numeración de los átomos de carbono comienza en el extremo más cercano a un sustituyente, la cadena más larga de átomos de carbono está numerada de tal manera que produce el número más bajo para los sustituyentes. El extremo -o reemplaza a -ide al final del nombre de un sustituyente electronegativo (en compuestos iónicos, el ion cargado negativamente termina con -ide como cloruro; en compuestos orgánicos, dichos átomos se tratan como sustituyentes y se usa la terminación -o). El número de sustituyentes del mismo tipo está indicado por los prefijos di- (dos), tri- (tres), tetra- (cuatro), y así sucesivamente (por ejemplo, difluoro- indica dos sustituyentes fluoruro).
Ejemplo 1
Nombramiento de alcanos sustituidos con halógeno
Nombra la molécula cuya estructura se muestra aquí:
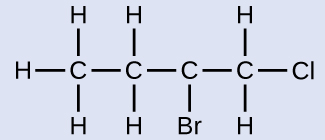
Solución
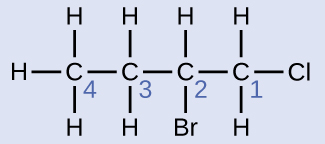
La cadena de cuatro carbonos está numerada desde el extremo con el átomo de cloro. Esto pone los sustituyentes en las posiciones 1 y 2 (la numeración desde el otro extremo pondría los sustituyentes en las posiciones 3 y 4). Cuatro átomos de carbono significa que el nombre base de este compuesto será butano. El bromo en la posición 2 se describirá añadiendo 2-bromo-; esto vendrá al inicio del nombre, ya que bromo- viene antes que cloro- alfabéticamente. El cloro en la posición 1 se describirá añadiendo 1-cloro-, dando como resultado que el nombre de la molécula sea 2-bromo-1-clorobutano.
Verifique su
nombre de aprendizaje la siguiente molécula:
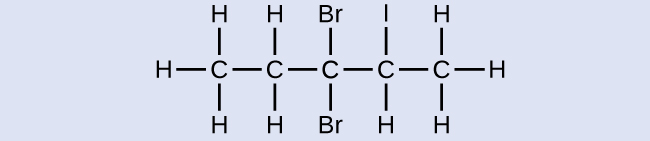
Respuesta:
3,3-dibromo-2-yodopentano
Llamamos a un sustituyente que contiene uno menos hidrógeno que el alcano correspondiente un grupo alquilo. El nombre de un grupo alquilo se obtiene dejando caer el sufijo -ano del nombre alcano y añadiendo -ilo:
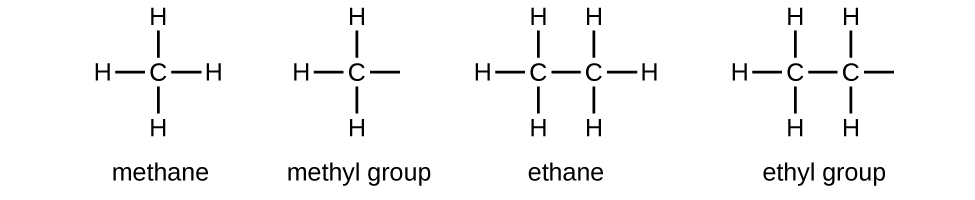
Los enlaces abiertos en los grupos metilo y etilo indican que estos grupos alquilo están unidos a otro átomo.
Ejemplo 2
Denominación de alcanos sustituidos
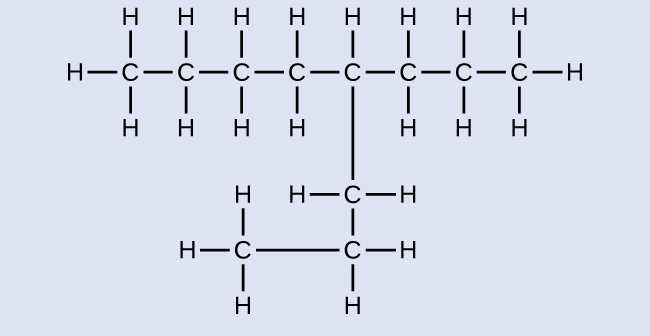
Nombra la molécula cuya estructura se muestra aquí:
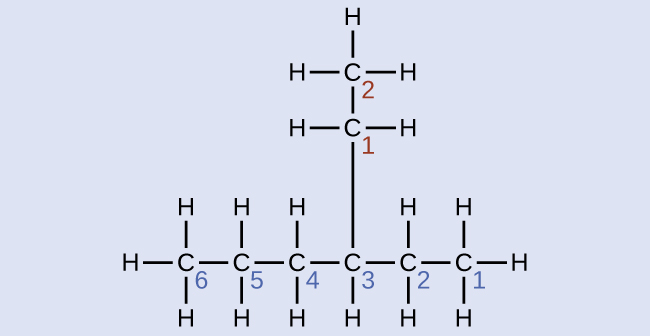
Solución
La cadena de carbono más larga corre horizontalmente por toda la página y contiene seis átomos de carbono (esto hace que la base del nombre hexano, pero también necesitaremos incorporar el nombre de la rama). En este caso, queremos numerar de derecha a izquierda (como lo muestran los números azules) para que la rama esté conectada al carbono 3 (imagínese los números de izquierda a derecha, esto pondría la rama en el carbono 4, violando nuestras reglas). La rama unida a la posición 3 de nuestra cadena contiene dos átomos de carbono (numerados en rojo) —así que tomamos nuestro nombre por dos carbonos eth- y unimos -ilo al final para significar que estamos describiendo una rama. Al juntar todas las piezas, esta molécula es 3-etilhexano.
Verifique su
nombre de aprendizaje la siguiente molécula:
Respuesta:
4-propiloctano
Algunos hidrocarburos pueden formar más de un tipo de grupo alquilo cuando los átomos de hidrógeno que se eliminarían tienen diferentes “ambientes” en la molécula. Esta diversidad de posibles grupos alquilo se puede identificar de la siguiente manera: Los cuatro átomos de hidrógeno en una molécula de metano son equivalentes; todos tienen el mismo ambiente. Son equivalentes porque cada uno está unido a un átomo de carbono (el mismo átomo de carbono) que está unido a tres átomos de hidrógeno. La eliminación de cualquiera de los cuatro átomos de hidrógeno del metano forma un grupo metilo. De igual manera, los seis átomos de hidrógeno en etano son equivalentes y la eliminación de cualquiera de estos átomos de hidrógeno produce un grupo etilo. Cada uno de los seis átomos de hidrógeno está unido a un átomo de carbono que está unido a otros dos átomos de hidrógeno y un átomo de carbono. Sin embargo, tanto en propano como en 2-metilpropano, hay átomos de hidrógeno en dos ambientes diferentes, que se distinguen por los átomos o grupos de átomos adyacentes:
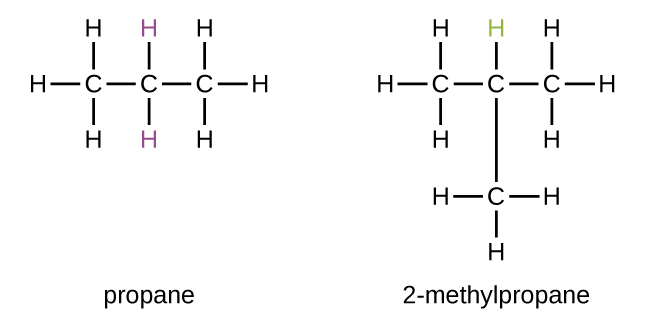
Cada uno de los seis átomos de hidrógeno equivalentes del primer tipo en propano y cada uno de los nueve átomos de hidrógeno equivalentes de ese tipo en 2-metilpropano (todos mostrados en negro) están unidos a un átomo de carbono que está unido solo a otro átomo de carbono. Los dos átomos de hidrógeno púrpura en el propano son de un segundo tipo. Se diferencian de los seis átomos de hidrógeno del primer tipo en que están unidos a un átomo de carbono unido a otros dos átomos de carbono. El átomo de hidrógeno verde en el 2-metilpropano difiere de los otros nueve átomos de hidrógeno en esa molécula y de los átomos de hidrógeno púrpura en el propano. El átomo de hidrógeno verde en 2-metilpropano está unido a un átomo de carbono unido a otros tres átomos de carbono. Se pueden formar dos grupos alquilo diferentes a partir de cada una de estas moléculas, dependiendo de qué átomo de hidrógeno se elimine. Los nombres y estructuras de estos y varios otros grupos alquilo se enumeran en la Figura 1.
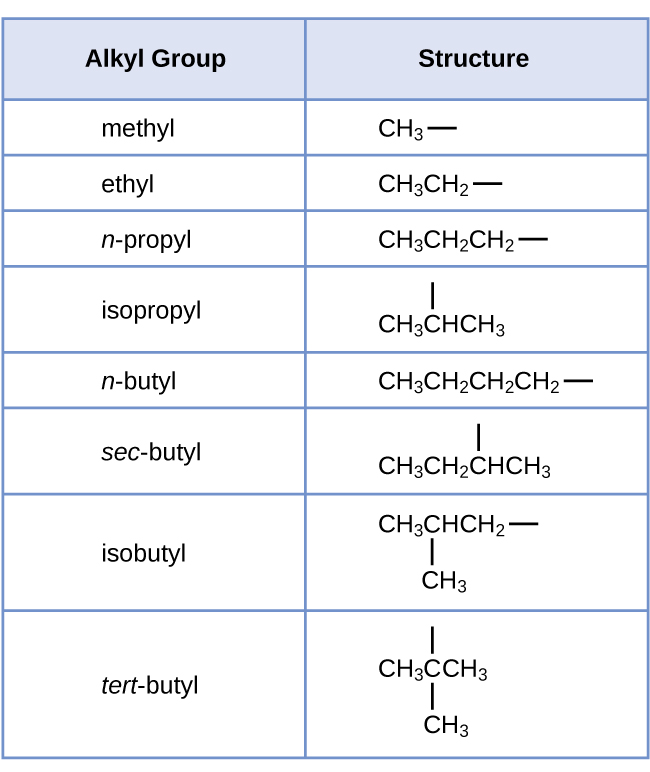
Nótese que los grupos alquilo no existen como entidades independientes estables. Siempre son parte de alguna molécula más grande. La ubicación de un grupo alquilo en una cadena hidrocarbonada se indica de la misma manera que cualquier otro sustituyente:
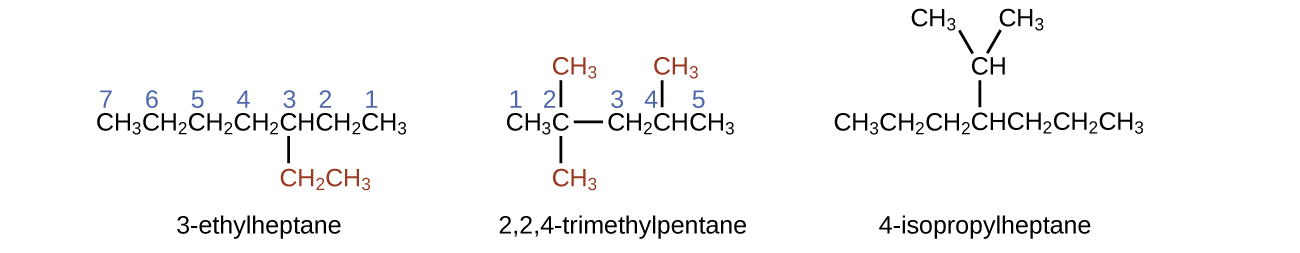
Alcoholes
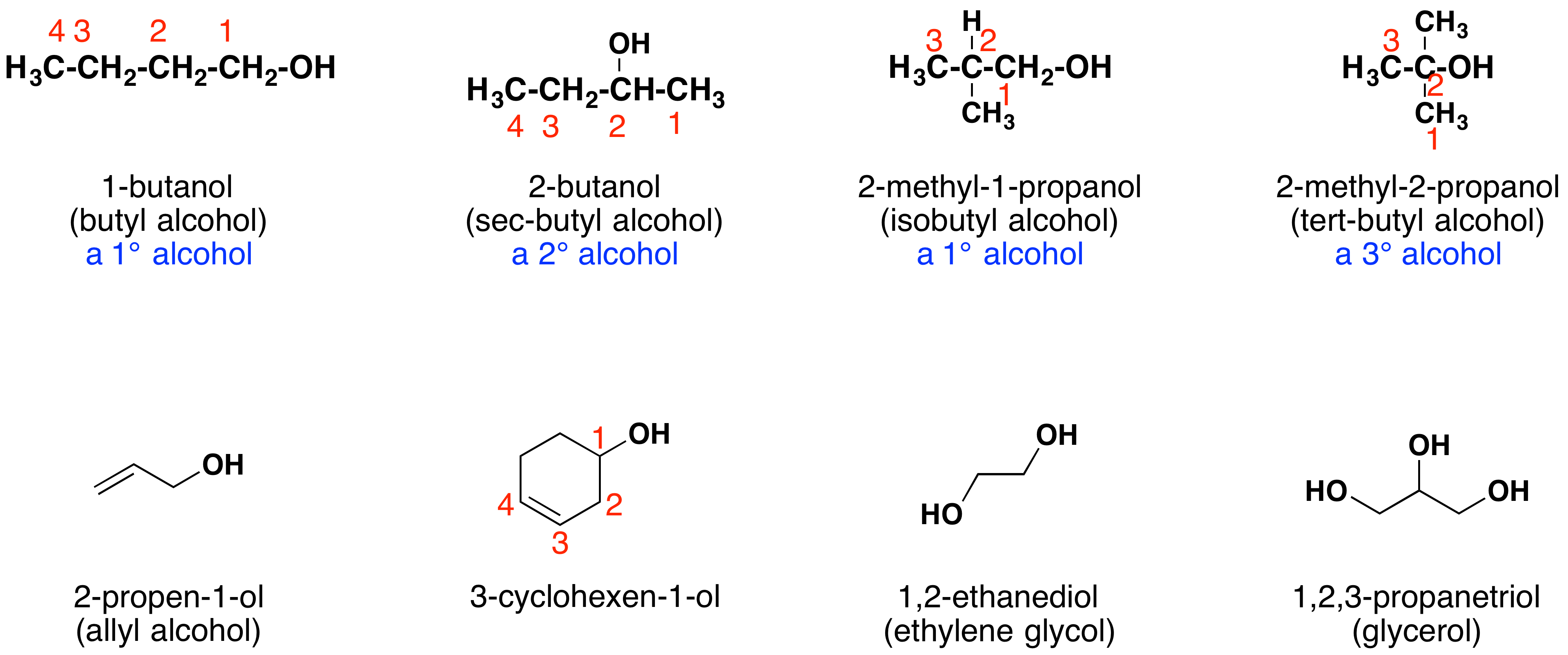
El nombre de un alcohol proviene del hidrocarburo del que se derivó. El -e final en el nombre del hidrocarburo se reemplaza por -ol, y el átomo de carbono al que está unido el grupo —OH se indica con un número colocado antes del nombre.
Considera el siguiente ejemplo:

La cadena carbonada contiene cinco átomos de carbono. Si el grupo hidroxilo no estuviera presente, habríamos nombrado a esta molécula pentano. Para abordar el hecho de que el grupo hidroxilo está presente, cambiamos el final del nombre a -ol. En este caso, dado que el —OH está unido al carbono 2 en la cadena, llamaríamos a esta molécula 2-pentanol.
Otros ejemplos de nomenclatura IUPAC se muestran a continuación, junto con los nombres comunes que a menudo se usan para algunos de los compuestos más simples. Para los alcoholes mono-funcionales, este sistema común consiste en nombrar al grupo alquilo seguido de la palabra alcohol. Los alcoholes también pueden clasificarse como primarios, 1º, secundarios, 2º y terciarios, 3º. Esta terminología se refiere a la sustitución alquílica del átomo de carbono que lleva el grupo hidroxilo (de color azul en la ilustración).
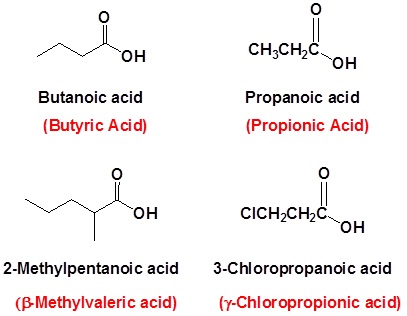
Ácidos Carboxílicos
La terminación —e se elimina del nombre de la cadena carbonada parental y se reemplaza el ácido -anoico. Dado que un grupo ácido carboxílico siempre debe estar al final de una cadena carbonada, siempre se le da la posición de ubicación #1 en la numeración y no es necesario incluirlo en el nombre. Muchos ácidos carboxílicos son llamados por los nombres comunes que fueron elegidos por los químicos para describir generalmente el origen del compuesto.
| Fórmula | Nombre común | Fuente | Nombre de la IUPAC |
|---|---|---|---|
| HCO 2 H | ácido fórmico | hormigas (L. formica) | ácido metanoico |
| CH 3 CO 2 H | ácido acético | vinagre (L. acetum) | ácido etanoico |
| CH 3 CH 2 CO 2 H | ácido propiónico | leche (Gk. protus prion) | ácido propanoico |
| CH 3 (CH 2) 2 CO 2 H | ácido butírico | mantequilla (L. butyrum) | ácido butanoico |
| CH 3 (CH 2) 3 CO 2 H | ácido valérico | raíz de valeriana | ácido pentanoico |
| CH 3 (CH 2) 4 CO 2 H | ácido caproico | cabras (L. alcaparras) | ácido hexanoico |
| CH 3 (CH 2) 5 CO 2 H | ácido enantico | vides (Gk. oenanthe) | ácido heptanoico |
| CH 3 (CH 2) 6 CO 2 H | ácido caprílico | cabras (L. alcaparra) | ácido octanoico |
| CH 3 (CH 2) 7 CO 2 H | ácido pelargónico | pelargonium (una hierba) | ácido nonanoico |
| CH 3 (CH 2) 8 CO 2 H | ácido cáprico | cabras (L. alcaparra) | ácido decanoico |
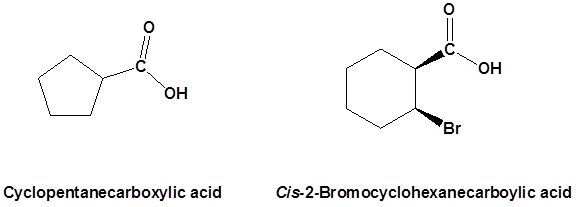
Cuando se agrega un grupo carboxilo a un anillo, se agrega el sufijo -ácido carboxílico al nombre del compuesto cíclico. Al carbono del anillo unido al grupo carboxilo se le da el número de ubicación #1.
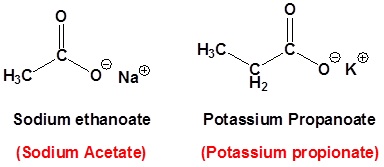
Las sales de ácidos carboxílicos se nombran escribiendo el nombre del catión seguido del nombre del ácido con la terminación —ácido ic reemplazada por una terminación —ato. Esto es cierto tanto para la IUPAC como para los sistemas de nomenclatura común.
Para los ácidos dicarboxílicos se omiten los números de localización para ambos grupos carboxilo porque se espera que ambos grupos funcionales ocupen los extremos de la cadena parental. El extremo —ácido dioico se agrega al final de la cadena parental.
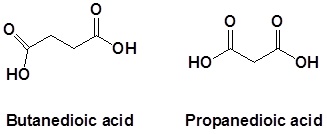
Ésteres
Los ésteres se nombran como si la cadena alquílica del alcohol es un sustituyente. No se asigna ningún número a esta cadena alquílica. A esto le sigue el nombre de la cadena parental de la parte de ácido carboxílico del éster con un —e remove y se reemplaza con el extremo —oato.
Por ejemplo:
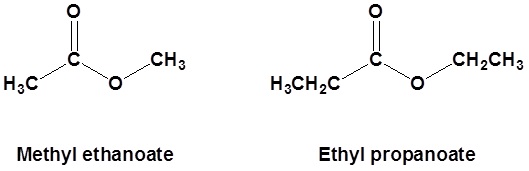
- Primero, identificar el oxígeno que forma parte de la cadena continua y unido al carbono en ambos lados. (En un lado de este oxígeno habrá un carbonilo presente pero en el otro lado no habrá.)
- Segundo, comenzar a numerar las cadenas de carbono a cada lado del oxígeno identificado en el paso 1.
- A continuación, utilice este formato: [alquilo en el lado más alejado del carbonilo] (espacio) [alcano en el lado con el carbonilo]
- Finalmente, cambiar la terminación del alcano en el mismo lado que el carbonilo de -e a -oato.
- Cuando un grupo éster está unido a un anillo, el éster se nombra como sustituyente en el anillo.
Tanto en la nomenclatura común como en la Unión Internacional de Química Pura y Aplicada (IUPAC), la terminación — ic del ácido parental se sustituye por el sufijo — ate.
| Fórmula estructural condensada | Nombre común | Nombre de la IUPAC |
|---|---|---|
| HCOOCH | formiato de metilo | metanoato de metilo |
| CH 3 COOCH 3 | acetato de metilo | etanoato de metilo |
| CH 3 COOCH 2 CH 3 | acetato de etilo | etanoato de etilo |
| CH 3 CH 2 COOCH 2 CH 3 | propionato de etilo | propanoato de etilo |
| CH 3 CH 2 CH 2 COOCH (CH 3) 2 | butirato de isopropilo | butanoato de isopropilo |
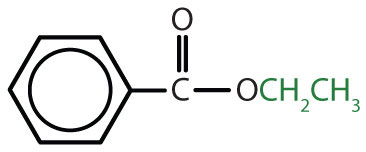 |
benzoato de etilo | benzoato de etilo |
Aminas
La palabra “amina” se deriva del amoníaco, y la clase de compuestos conocidos como aminas, por lo tanto, se denominan comúnmente como amonías sustituidas. En este sistema, las aminas primarias (RNH 2), que tienen solo un sustituyente en el nitrógeno, se nombran con el sustituyente como prefijo. Una nomenclatura más sistemática agrega -amina a la cadena más larga, como para los alcoholes:
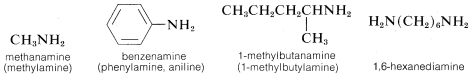
Las aminas secundarias (R2 NH) y terciarias (R3 N), que tienen dos y tres sustituyentes en el nitrógeno, comúnmente se denominan aminas N-sustituidas. N se incluye para indicar que el sustituyente está en el átomo de nitrógeno a menos que no haya ambigüedad en cuanto a dónde se encuentra el sustituyente. Cada uno de los grupos R se nombra como una palabra separada, excepto cuando los grupos son idénticos, en cuyo caso se puede usar el prefijo di o bis (di se usa para grupos simples, bis para grupos sustituidos):
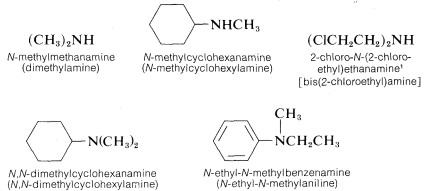
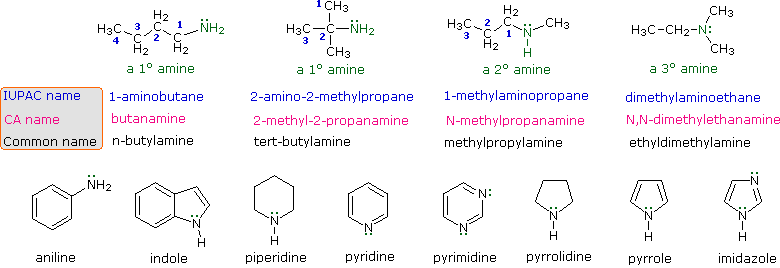
La nomenclatura de las aminas se complica por el hecho de que existen varios sistemas de nomenclatura diferentes. Los cuatro compuestos mostrados en la fila superior del siguiente diagrama son todos isómeros C 4 H 11 N.
- Los nombres de la IUPAC se enumeran primero y se colorean en azul. Este sistema nombra funciones amina como sustituyentes en el grupo alquilo más grande. El sustituyente -NH simple que se encuentra en las 1º-aminas se denomina grupo amino. Para las aminas 2º y 3º-un prefijo compuesto (por ejemplo, dimetilamino en el cuarto ejemplo) incluye los nombres de todos menos el grupo alquilo raíz.
- El Chemical Abstract Service ha adoptado un sistema de nomenclatura en el que el sufijo -amina se une al nombre alquilo raíz. Para 1º-aminas como la butanamina (primer ejemplo) esto es análogo a la nomenclatura del alcohol IUPAC (sufijo -ol). Los sustituyentes de nitrógeno adicionales en las aminas 2º y 3º-se designan con el prefijo N- antes del nombre del grupo. Estos nombres de CA son de color magenta en el diagrama.
- Finalmente, un sistema común para aminas simples nombra a cada sustituyente alquilo en nitrógeno en orden alfabético, seguido del sufijo -amina. Estos son los nombres dados en la última fila (de color negro).
Muchas aminas aromáticas y heterocíclicas son conocidas por nombres comunes únicos, cuyos orígenes a menudo son desconocidos para los químicos que las utilizan con frecuencia ya que estos nombres no se basan en un sistema racional.
Amidas
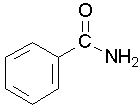
Las amidas primarias se nombran cambiando el nombre del ácido dejando caer las terminaciones de ácido -oico o ácido -ic y agregando -amida. Al carbono carbonílico se le da el número de ubicación #1. No es necesario incluir el número de ubicación en el nombre porque se supone que el grupo funcional estará al final de la cadena padre. Por ejemplo, las siguientes tres amidas se denominan metanamida o formamida, etanamida o acetamida, y benzamida.
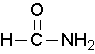

A continuación se muestran ejemplos adicionales:
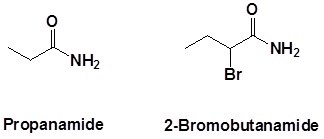
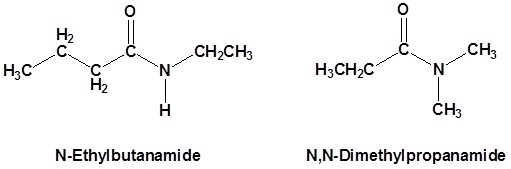
Las amidas secundarias se nombran usando un N mayúscula para designar que el grupo alquilo está en el átomo de nitrógeno. Los grupos alquilo unidos al nitrógeno se nombran como sustituyentes. Se utiliza la letra N para indicar que están adheridas al nitrógeno. Por ejemplo, la molécula a continuación se llama N-metilpropanamida:
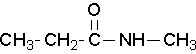
Las amidas terciarias se nombran de la misma manera que las amidas secundarias, pero con dos N's