5.1: Espectros COSY
- Page ID
- 79167
En la RMN 2D, se utilizan picos de correlación para ayudar a establecer la estructura.
Empecemos con un compuesto simple, el acetato de etilo.
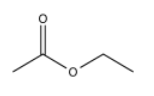
El espectro de RMN 1H no es muy complicado.
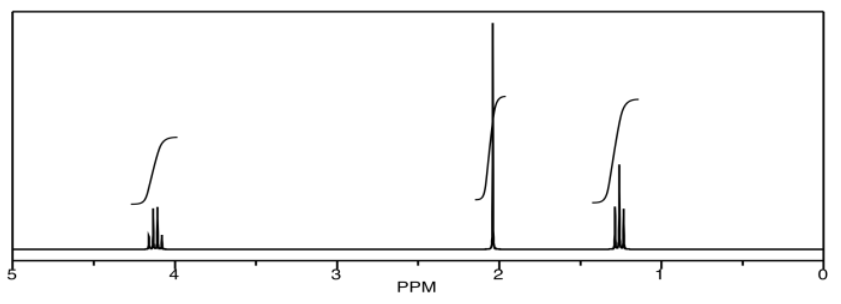
En la espectroscopia de correlación homonuclear (COSY), podemos buscar hidrógenos que se acoplan entre sí. En acetato de etilo, está bastante claro dónde están. Hay un cuarteto y un triplete; los hidrógenos correspondientes a esos dos picos probablemente están uno al lado del otro en la estructura.
El espectro COSY simplemente toma ese espectro de 1 H y lo extiende en dos dimensiones. En lugar de mostrarse como una fila de picos, los picos se extienden en una matriz. En el siguiente espectro COSY simulado, los picos se muestran a lo largo de un eje. Los mismos picos también se muestran a lo largo del otro eje. En la mitad de la gráfica, los picos se muestran trazados uno contra el otro, es decir, hay un pico a 1.25 ppm en el eje y y a lo largo del eje x, por lo que hay un punto de datos en la parcela en (1.25, 1.25). Otros picos similares aparecen a lo largo de la diagonal que se extiende desde la parte superior derecha hasta la parte inferior izquierda a través de la mitad de la parcela. Hay tres picos que aparecen a lo largo de esa línea diagonal; estos tres picos básicamente nos muestran lo que ya vimos en el espectro de RMN de 1H regular.
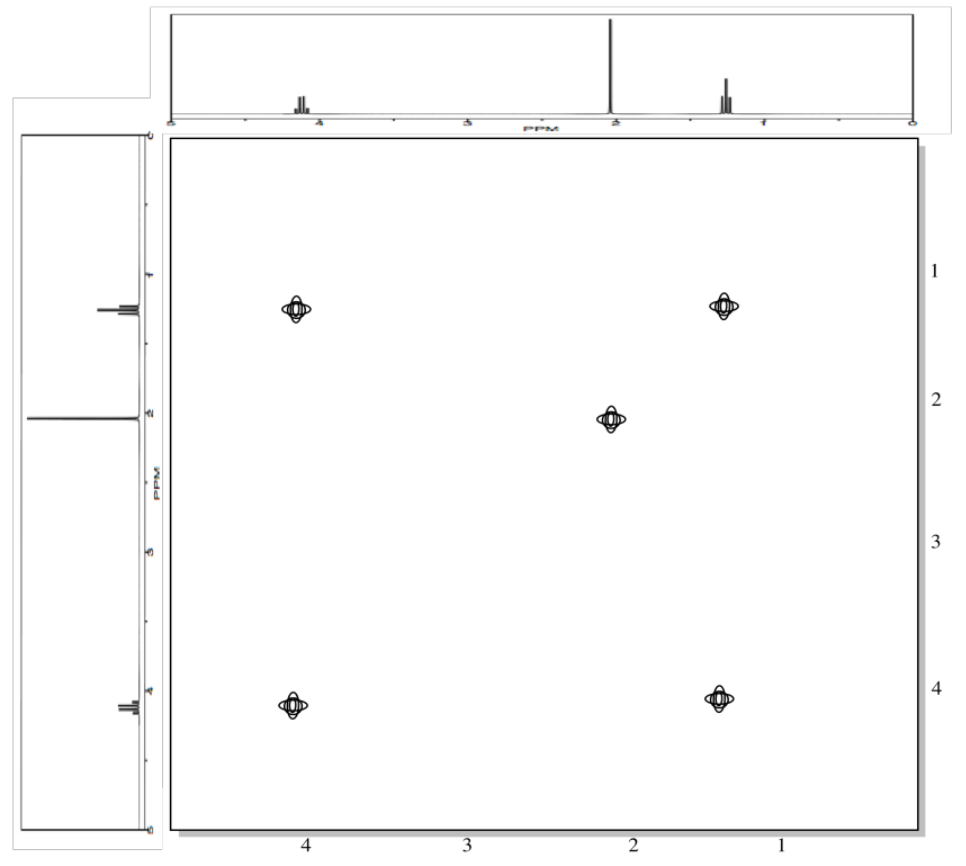
Los picos interesantes son los que no aparecen a lo largo de la diagonal. Esos picos indican qué hidrógenos están acoplados a qué otros hidrógenos. Los hidrógenos a 1.25 ppm se acoplan a los de 4.2 ppm, y eso da un “pico cruzado” a (1.25, 4.20). También hay un pico cruzado en (4.20, 1.25), porque esa relación va en ambos sentidos.
¿Qué significa estar acoplado? Significa que la información magnética se transmite entre los átomos. ¿Cómo lo podemos decir? Esencialmente, podemos enviar un pulso de radiación electromagnética a un conjunto de hidrógenos y buscar una respuesta en otro lugar. Por supuesto, si enviamos un pulso de ondas de radio a una frecuencia que será absorbida por un hidrógeno en particular, veremos una respuesta en ese mismo hidrógeno. Por eso vemos los picos en la diagonal. Sin embargo, también vemos respuestas de otros hidrógenos que están vinculados magnéticamente al original.
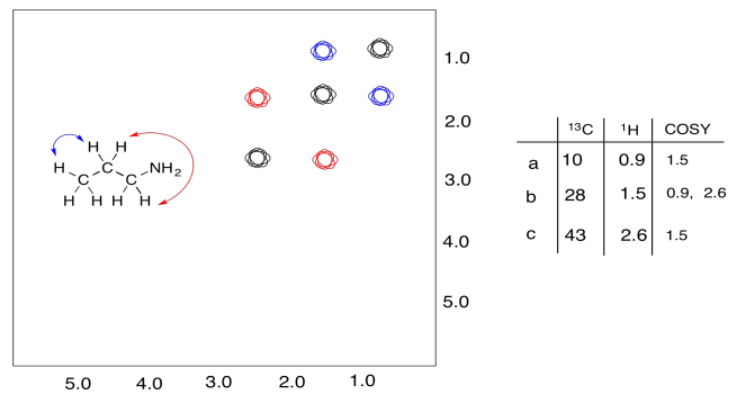
A continuación se muestra un segundo ejemplo. Esta vez, el compuesto es propanamina. En propanamina, nuevamente habría un conjunto diagonal de picos, mostrados en negro, correspondientes a los picos en el espectro de protones regular. Además, se acoplan dos conjuntos diferentes de protones. El grupo metilo se acopla al metileno en el centro de la molécula; ese pico cruzado se muestra en azul. El metileno en el medio también se acopla al metileno junto al nitrógeno; ese pico cruzado se muestra en rojo.
Ejercicio\(\PageIndex{1}\)
Proporcionar análisis de los siguientes espectros y proponer una estructura para el compuesto.
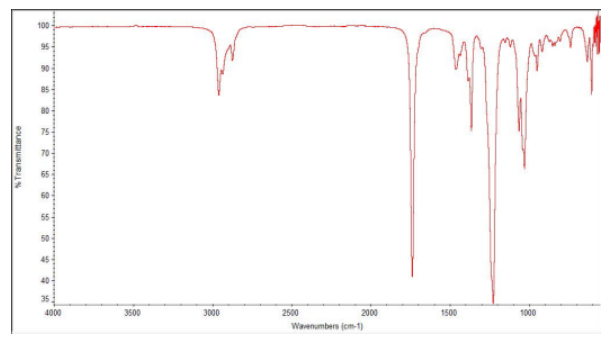
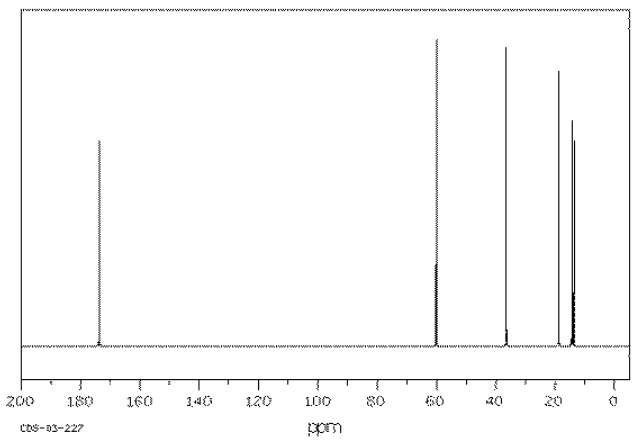
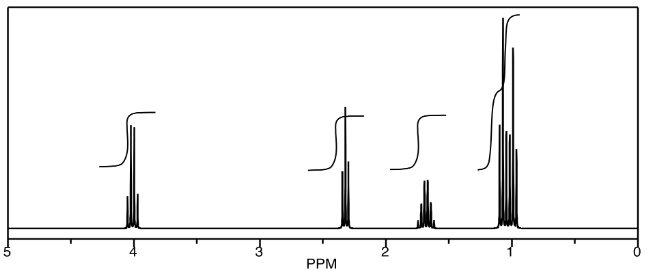
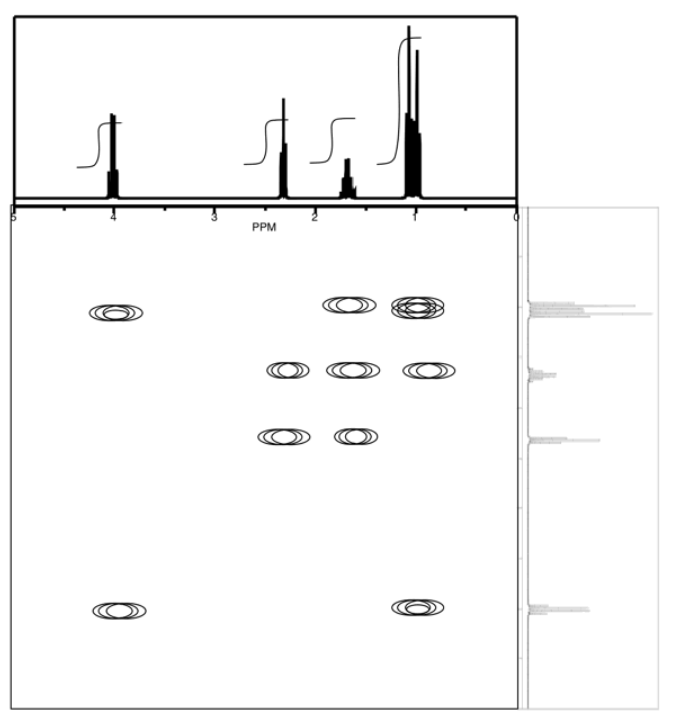
- Contestar
-
Butanoato de etilo
Ejercicio\(\PageIndex{2}\)
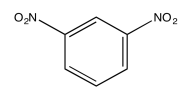
El siguiente espectro COSY es para un isómero de dinitrobenceno. ¿Qué isómero es?
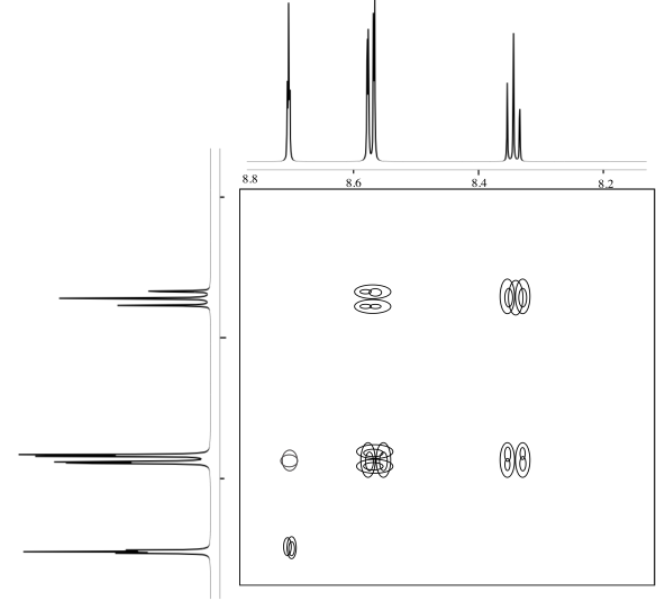
- Contestar
-
Ejercicio\(\PageIndex{3}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
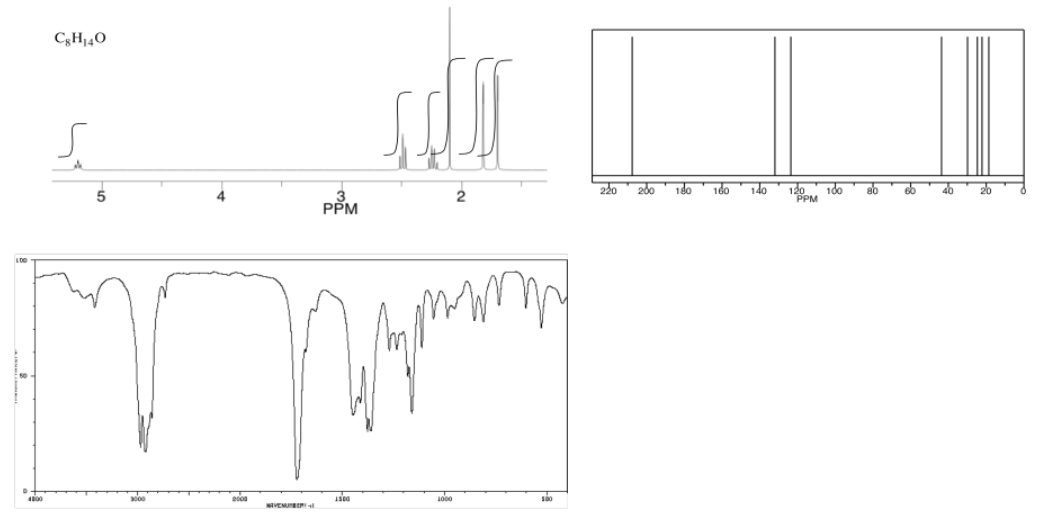
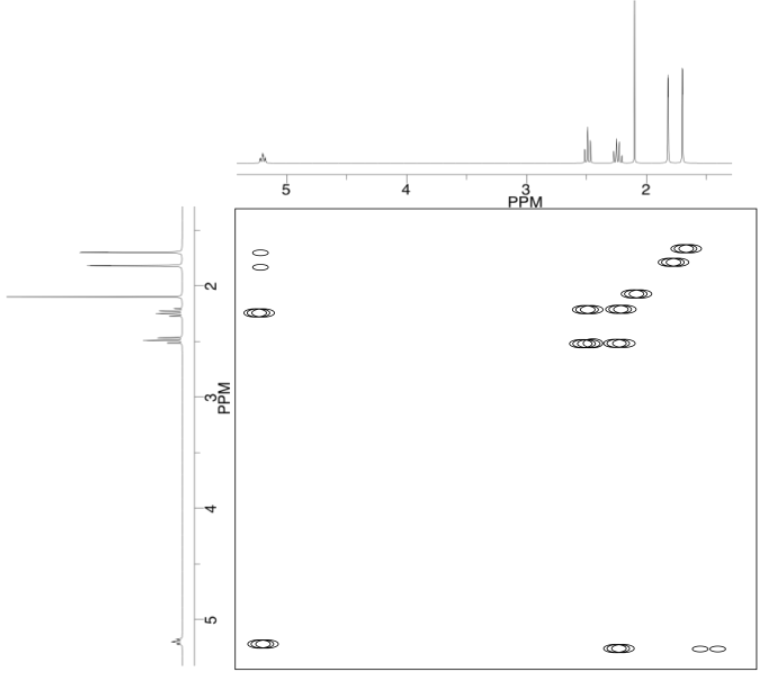
- Contestar
-
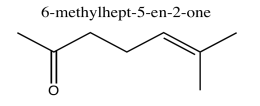
Ejercicio\(\PageIndex{4}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
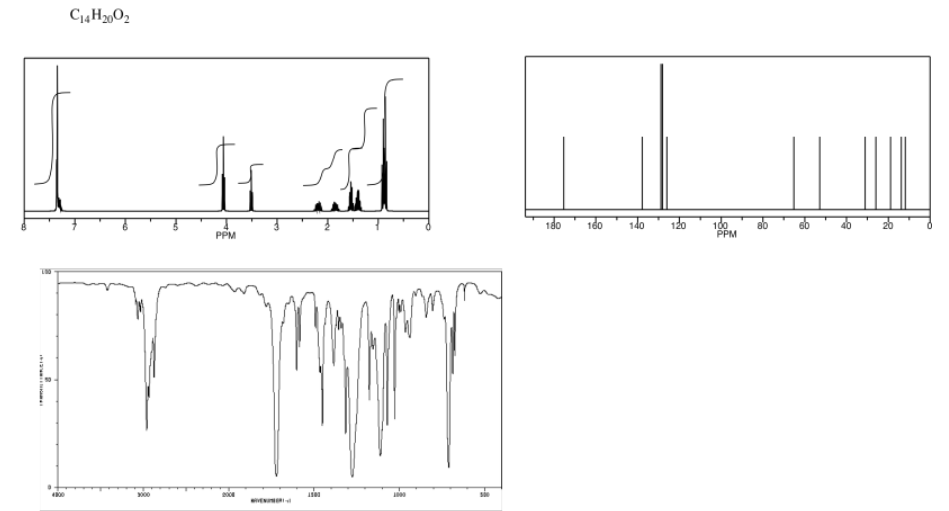
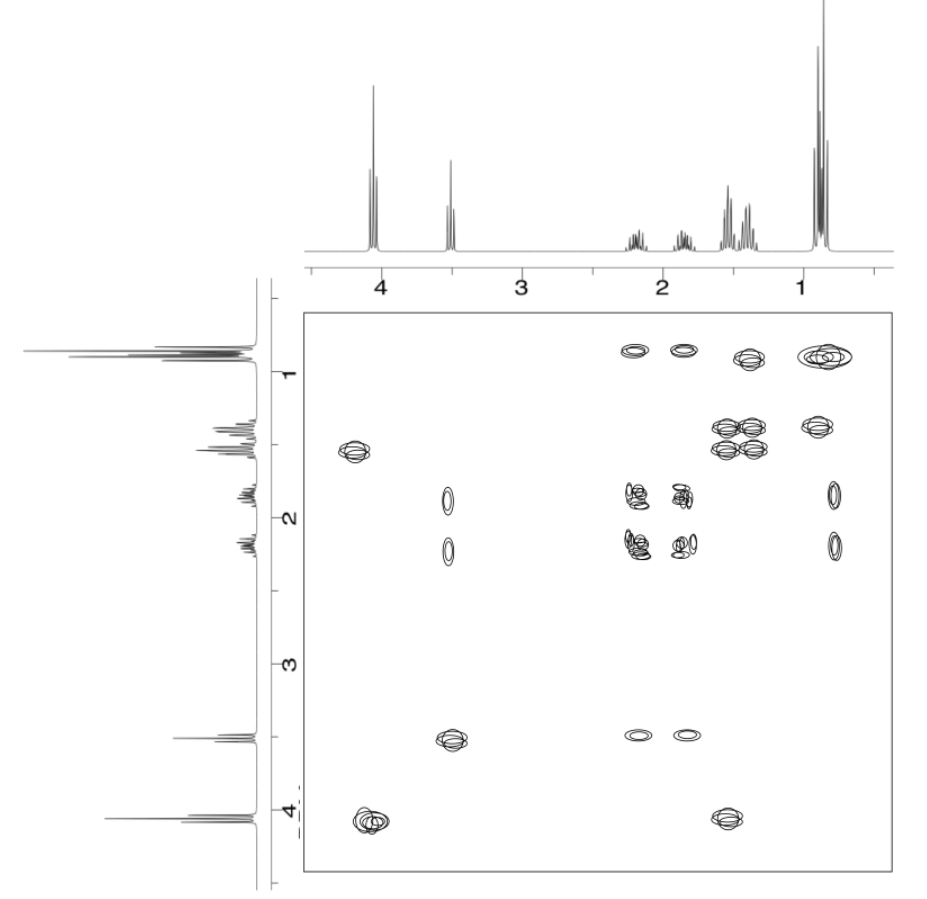
- Contestar
-
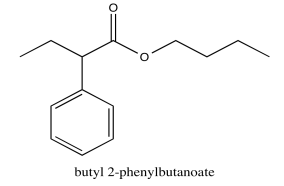
Ejercicio\(\PageIndex{5}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
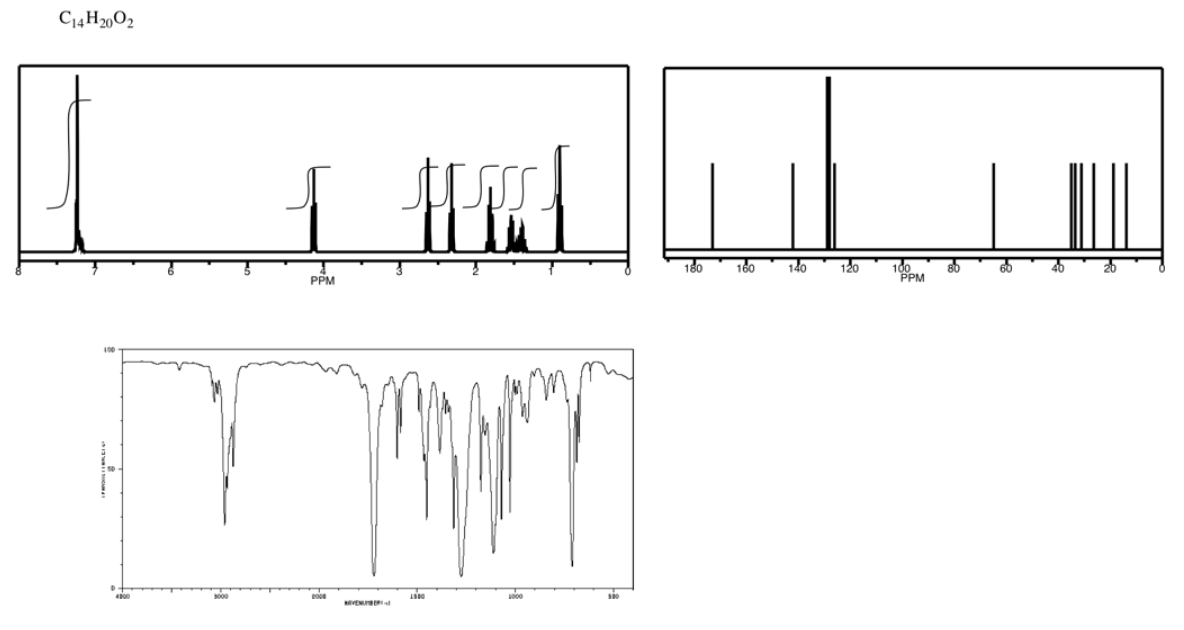

- Contestar
-
Ejercicio\(\PageIndex{6}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
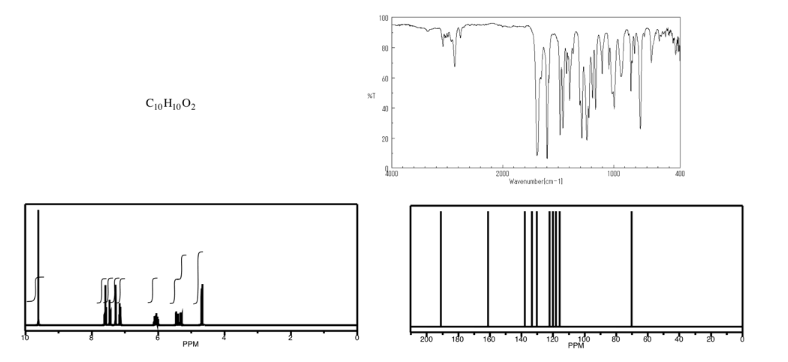
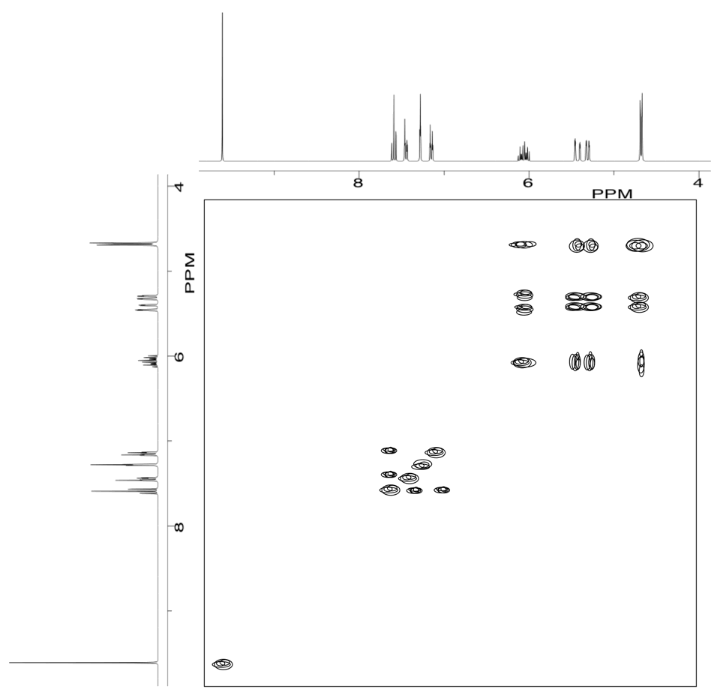
- Contestar
-
Ejercicio\(\PageIndex{7}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
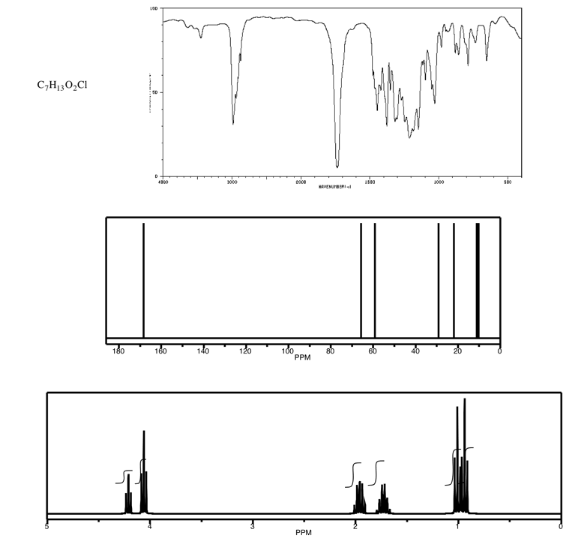
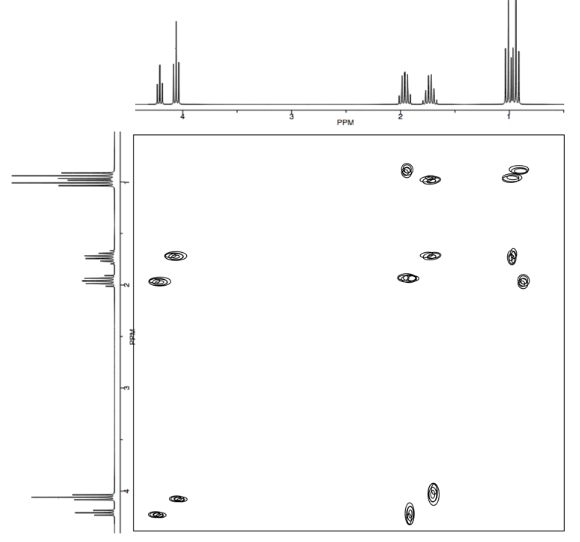
- Contestar
-
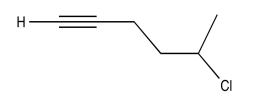
Ejercicio\(\PageIndex{8}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
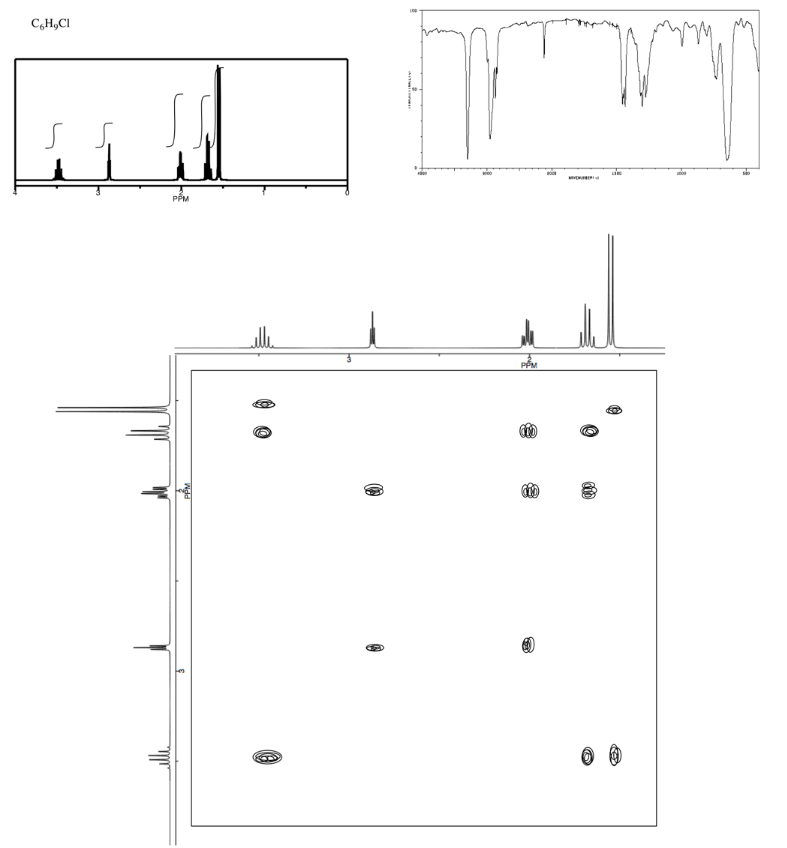
- Contestar
-
Ejercicio\(\PageIndex{9}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
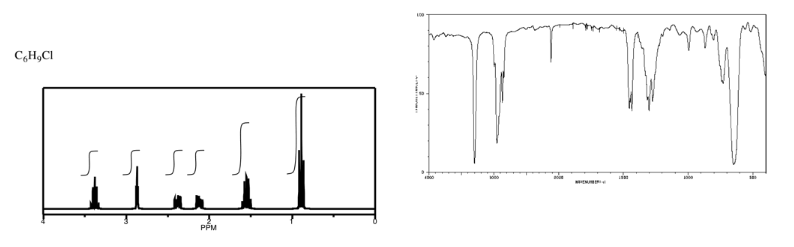
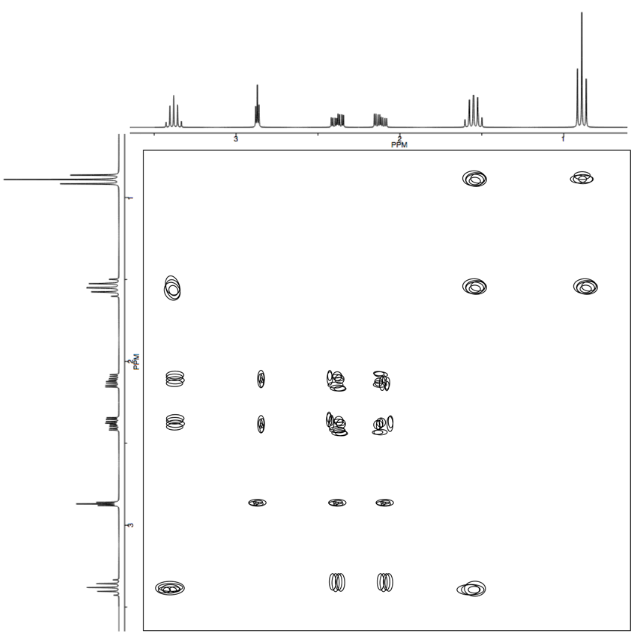
- Contestar
-
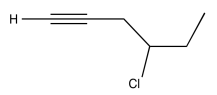
Ejercicio\(\PageIndex{10}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
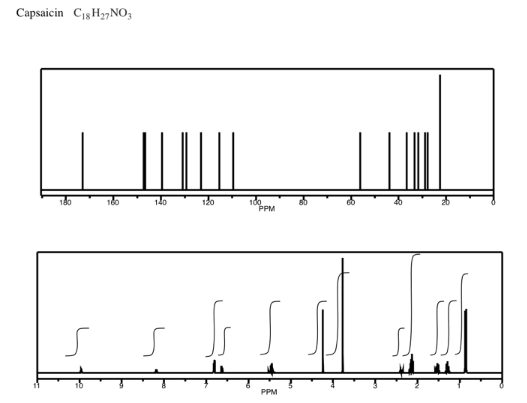

- Contestar
-
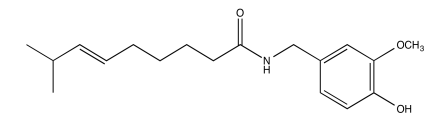
Ejercicio\(\PageIndex{11}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
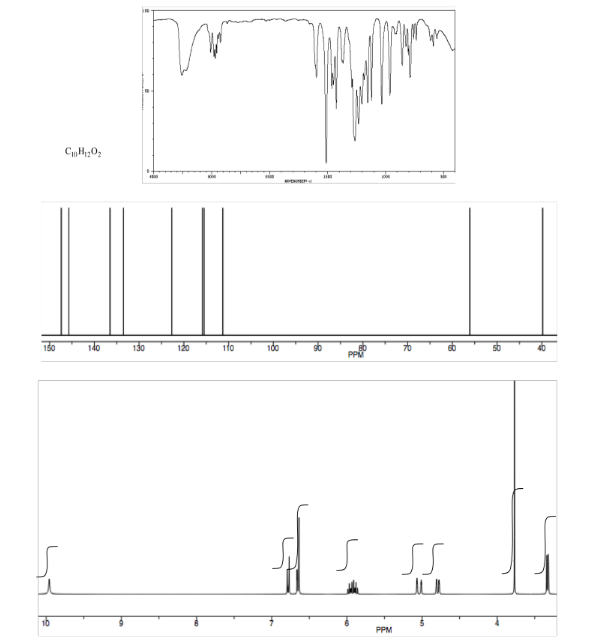
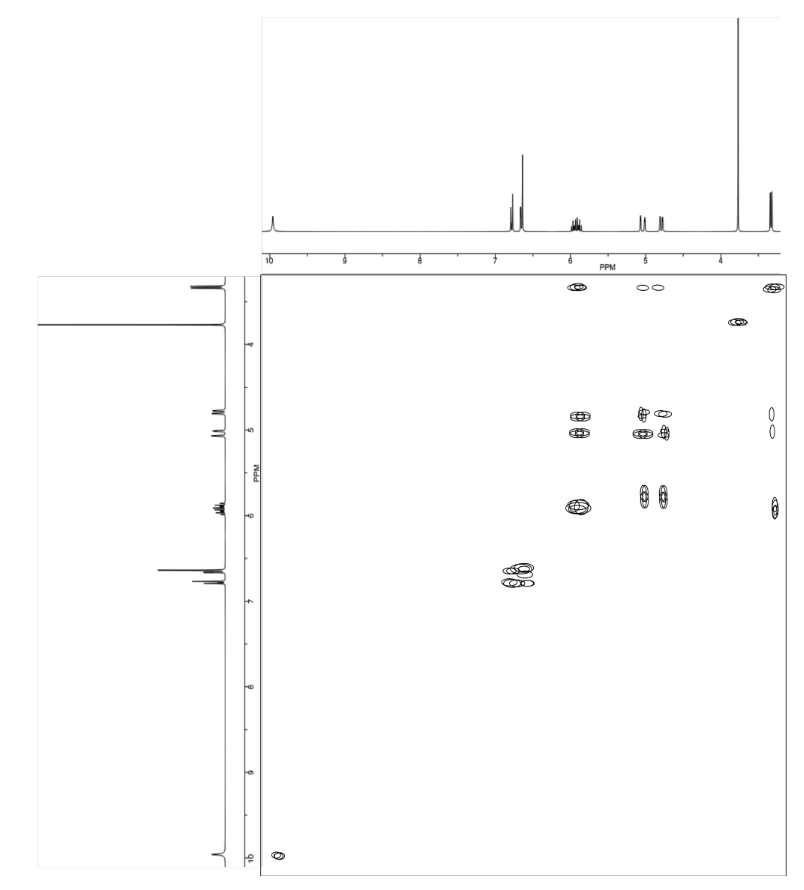
- Contestar
-
Ejercicio\(\PageIndex{12}\)
Analizar los datos en los siguientes espectros y proponer una estructura para el compuesto.
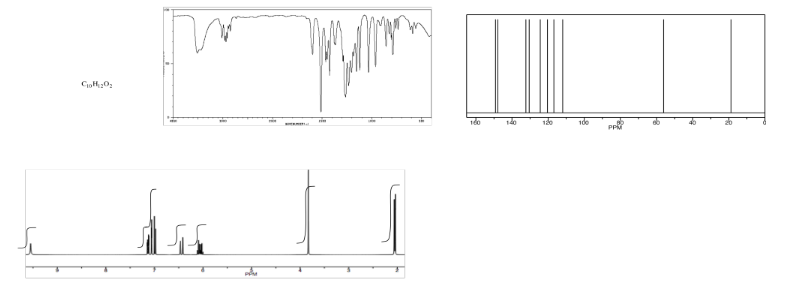
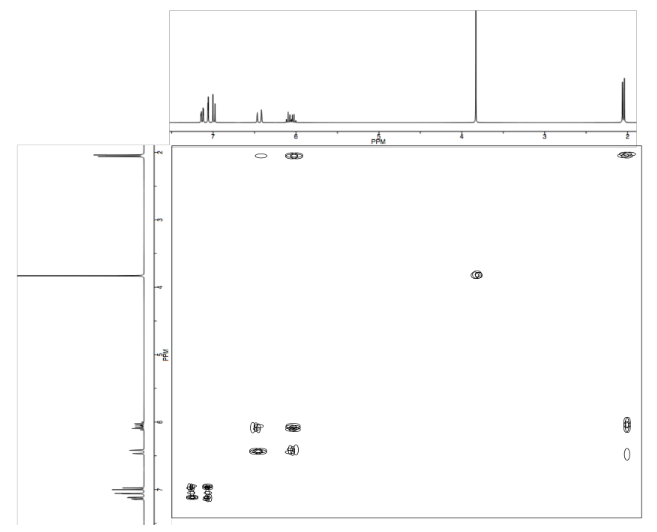
- Contestar
-
* Fuentes:
Espectros de RMN IR y 13 C seleccionados de SDBS (Instituto Nacional de Ciencia y Tecnología Industrial Avanzada, Japón, Base de datos espectral para compuestos orgánicos, http://sdbs.db.aist.go.jp/sdbs/cgi-bin/cre_index.cgi, consultado en diciembre de 2015).
Espectros de RMN 1H y COSY simulados.

