3.5: Compuestos de organosilicio y organogermanio
- Page ID
- 69266
Objetivos de aprendizaje
En esta conferencia aprenderás lo siguiente
- Compuestos organosilícicos y organogermanio.
- Compuestos con enlaces Si=Si y Ge=Ge.
Compuestos organosilícicos y organogermanio
Los compuestos organosilícicos son ampliamente estudiados debido a la amplia gama de aplicaciones comerciales como repelentes de agua, lubricantes y selladores. Se pueden sintetizar muchos compuestos organosilícicos con puente oxo. ej. (CH 3) 3 Si—O-Si (CH 3) 3 que es resistente a la humedad y al aire.
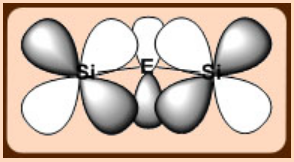
Los pares solitarios en O se deslocalizan parcialmente en orbitales σ*- vacantes de Si, como resultado la direccionalidad del enlace Si-O se reduce haciendo la estructura más flexible.
Esta flexibilidad permite que los elastómeros de silicona permanezcan como caucho hasta temperaturas muy bajas.
La deslocalización también explica la baja basicidad de un átomo de O unido al silicio, ya que los electrones necesarios para que el átomo de O actúe como base se eliminan parcialmente.
La planaridad de N (SiH 3) 3 también se explica por la deslocalización del par solitario en N lo que lo hace muy débilmente básico.
\[\ce{nMeCl + Si/Cu -> Me_{n}SiCl_{4-n}}\]
\[\ce{SiCl4 + 4RLi -> R4Si}\]
\[\ce{SiCl4 + RLi -> RSiCl3}\]
\[\ce{SiCl4 + 2RMgCl -> R2SiCl2 + 2MgCl2}\]
\ [\ ce {Me2SiCl2 + tBuBi -> TBuMe2SiCl + LiCl} |]
Los enlaces Si-C son relativamente fuertes (la entalpía del enlace es 318 kJ mol -1) y los derivados de R 4 Si poseen altas estabilidades térmicas. Et 4 Si en la cloración da (ClCH 2 CH 2) 4 Si, en contraste con la cloración de R 4 Ge o R 4 Sn que produce R n GecL 4-n o R n SnCl 4-n.
Me 2 SiCl 2 en hidrólisis producir siliconas.
\[\ce{Me3SiCl + NaCp -> (η^{1}-Cp)SiHMe3}\]
(η 1 -C 5 Me 5) 2 SiBr 2 en tratamiento con antraceno/potasio da Cp* 2 Si
La estructura en estado sólido de Cp* 2 Si consiste en dos moléculas independientes que difieren en las orientaciones relativas de los anillos Cp.
En una molécula, son paralelas y escalonadas mientras que en la otra, están inclinadas con un ángulo de 167°en Si.
La reacción entre R 2 SiCl 2 y naftalidas de metales alcalinos o alcalinos da ciclo- (R 2 Si) n por pérdida de formación de enlaces Cl - y Si-Si.
Los grupos R voluminosos favorecen los anillos pequeños [por ejemplo, (2,6-Me 2 C 6 H 3) 6 Si 3 y t Bu 6 Si 3] mientras que los grupos R más pequeños fomentan la formación de anillos grandes [Me 12 Si 6, Me 14 Si 7 y Me 32 Si 16]
\[\ce[Ph2SiCl2 + Li(SiPh2)5Li -> cyclo-Ph12Si6 + 2LiCl}\]
Los sustituyentes voluminosos estabilizan los compuestos R2 Si=SiR 2. La demanda estérica 2,4,6- i Pr 3 C 6 H 2 proporcionó el primer ejemplo de compuesto que contenía enlaces Si=Si conjugados.
Tiene configuración s-cis tanto en solución como en estado sólido.
También se conocen compuestos similares de germanio
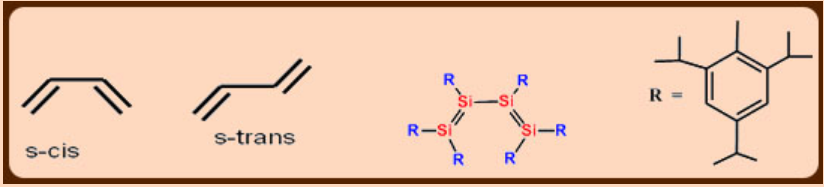
* La disposición espacial de dos dobles enlaces conjugados alrededor del enlace sencillo intermedio se describe como s- cis si es sinperiplanar y s-trans si es antiperiplanar.


