1.2: Química inorgánica vs orgánica
- Page ID
- 80985
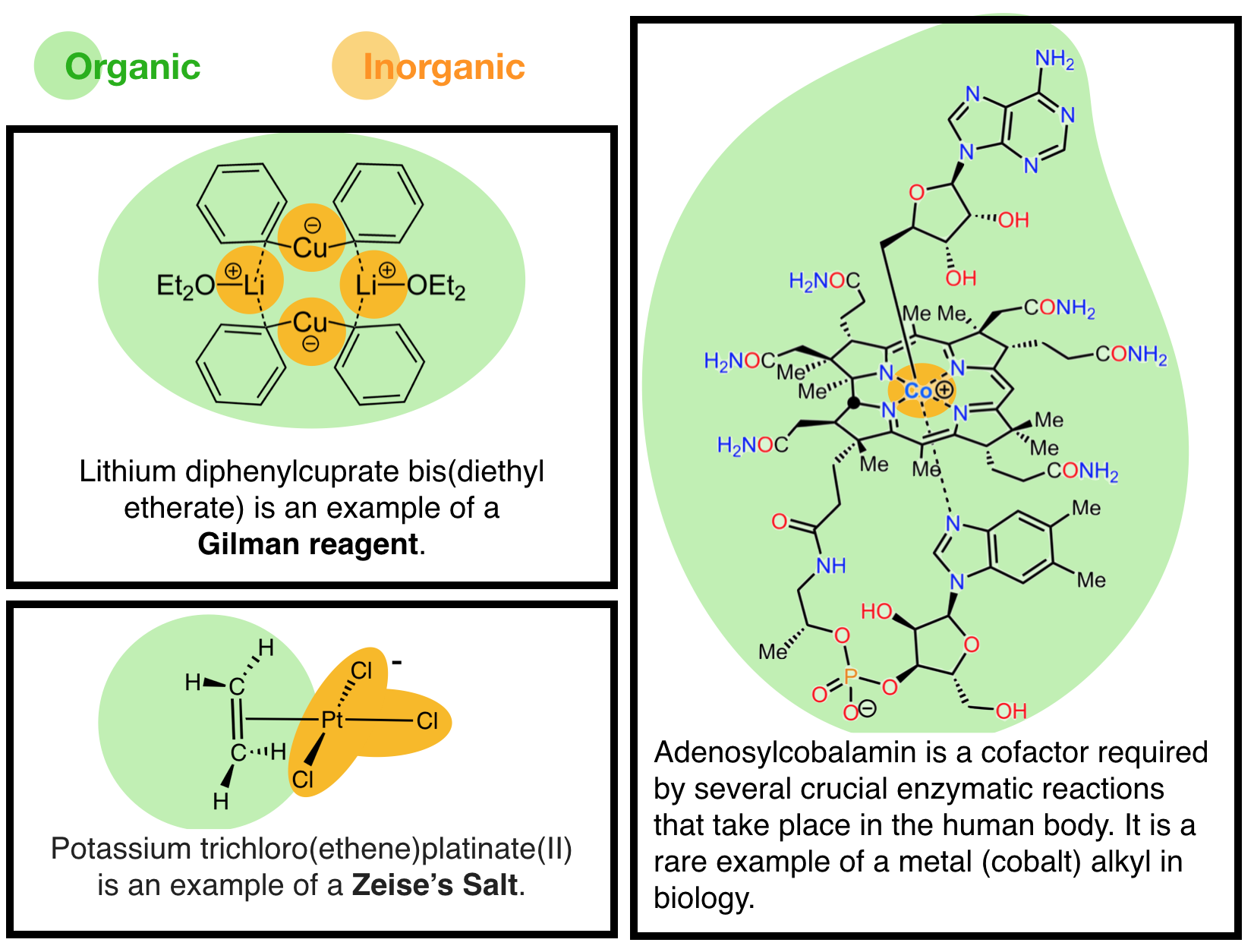
La división entre los campos de la química inorgánica y orgánica se ha vuelto borrosa. Por ejemplo, veamos una de las principales clases de catalizadores utilizados para las reacciones de síntesis orgánica: los catalizadores organometálicos (Figura\(\PageIndex{1}\)). Los catalizadores organometálicos como estos, y todos los compuestos organometálicos, contienen metales que están unidos a carbono o moléculas que contienen carbono. Entonces, ¿son “inorgánicos” porque contienen metales, o “orgánicos” porque contienen carbono? Estos ilustran que no existen claras divisiones entre química orgánica e inorgánica. Además, los iones metálicos son comunes en biología y por lo tanto la idea de que los metales son “inorgánicos” y por lo tanto se califican como “no vivos o no biológicos” es incorrecta. Un ejemplo canónico es el catalizador organometálico adenosilcobalbúmina, el cual es un importante cofactor biológico que contiene un ion cobalto (Co) (Figura\(\PageIndex{1}\), derecha) y un enlace cobalto-carbono.
Algunos de los subcampos de la Química Inorgánica se centran en la conductividad eléctrica de materiales inorgánicos (es decir, conducción, superconducción y semiconducción) y en el estudio de las propiedades ópticas y electrónicas de nanomateriales inorgánicos. La conductividad eléctrica es una propiedad canónica de los metales, pero los materiales a base de carbono también demuestran conductividad eléctrica. Por ejemplo, los nanotubos de carbono conducen la electricidad a través de sus\(\pi\) sistemas conjugados extendidos. Los fullerenos, de los cuales el más famoso es Buckminsterfullerene, o Buckeyball (C 60), demuestran propiedades interesantes que son similares a las nanopartículas, y cuando se combinan con metales y cristalizan pueden demostrar superconductividad.
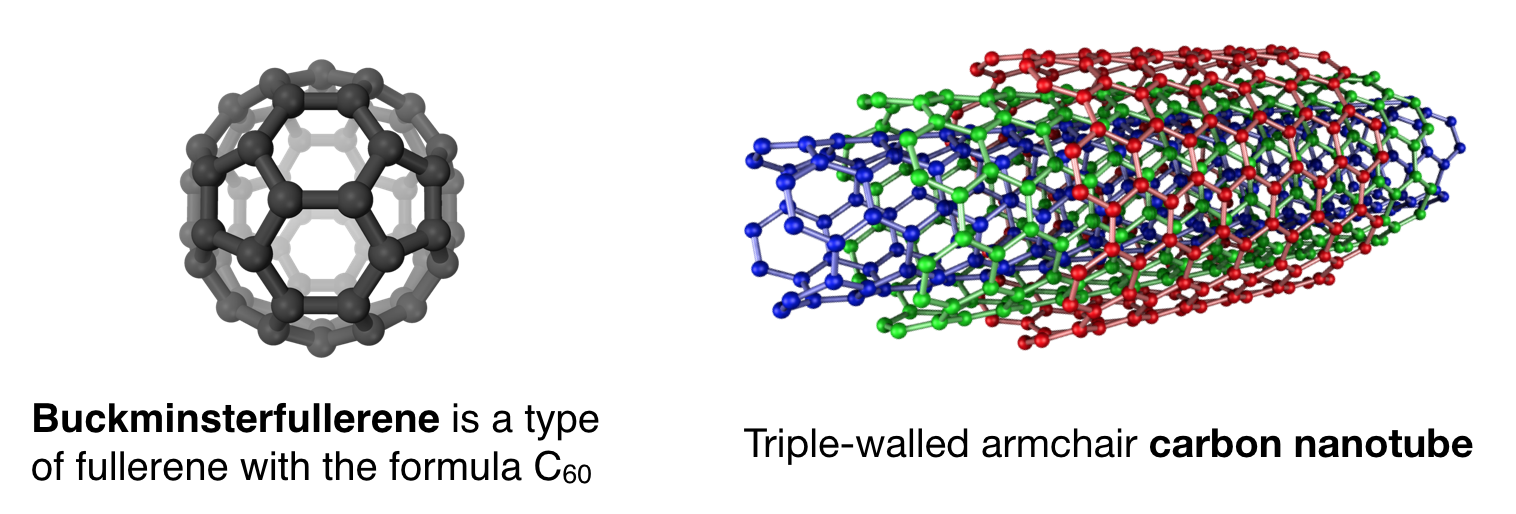
Aunque los nanotubos de carbono y los fullerenos son alótropos de carbono, sus propiedades materiales son algo ajenas a muchos químicos orgánicos, quienes tradicionalmente se han centrado en moléculas orgánicas más pequeñas que tienen propiedades muy diferentes. Sin embargo, estas propiedades son familiares para los químicos inorgánicos. Así, los químicos inorgánicos han abrazado estas moléculas como “inorgánicas” debido a que se comportan más como materiales inorgánicos que a moléculas orgánicas más pequeñas. Esta clase de moléculas basadas en carbono sirve como otro ejemplo de moléculas que no coinciden perfectamente con las definiciones tradicionales de química “orgánica” e “inorgánica”. Ciertamente, el futuro albergará cada vez más ejemplos de moléculas que no encajan en las disciplinas tradicionales de la química.


