7.7.4: La ecuación de Born-Lande'
- Page ID
- 81202
La ecuación Born-Landé es un concepto formulado originalmente en 1918 por los científicos Born y Landé y se utiliza para calcular la energía reticular (medida de la fuerza de los enlaces) de un compuesto. Esta expresión toma en cuenta tanto las interacciones Born como las atracciones de Coulomb.
Introducción
Debido a su alta simplicidad y facilidad, la ecuación de Born-Landé es comúnmente utilizada por los químicos a la hora de resolver la energía de celosía. Esta ecuación propuesta por Max Born y Alfred Landé establece que la energía reticular puede derivarse de la red iónica basada en el potencial electrostático y la energía potencial debida a la repulsión. Para resolver la ecuación Born-Landé, debes tener una comprensión básica de la energía de celosía:
- La energía de celosía disminuye a medida que desciende de un grupo (a medida que los radios atómicos suben, la energía de celosía baja).
- Al pasar por la tabla periódica, los radios atómicos disminuyen, por lo tanto, aumenta la energía de la red.
La ecuación de Born-Landé se derivó de estas dos ecuaciones siguientes. la primera es la energía potencial electrostática:
\[ \Delta U = - \dfrac{N_A M\left | Z^+ \right | \left | Z^- \right |e^2}{4\pi\epsilon_o r} \label{1} \]
con
- \(M_A\)es la constante de Avogadro (\(6.022 \times 10^{23}\))
- \(M\)es la Constante de Madelung (una constante que varía para diferentes estructuras)
- \(e\)es la carga de un electrón (\(1.6022 \times 10^{-19}\)C)
- \(Z^+\)es la carga catiónica
- \(Z^-\)es la carga aniónica
- \(\epsilon_o\)es la permitividad del espacio libre
La segunda ecuación es la interacción repulsiva:
\[ \Delta U = \dfrac{N_A B}{r^n} \label{2}\]
con
- \(B\)es el coeficiente de repulsión y
- \(n\)es el Exponente Born (típicamente oscila entre 5-12) que se utiliza para medir cuánto comprime un sólido
Estas ecuaciones se combinan para formar:
\[ \Delta U (0K) = \dfrac{N_A M\left | Z^+ \right | \left | Z^- \right |e^2}{4\pi\epsilon_or_o} \left ( 1- \dfrac{1}{n} \right) \label{3}\]
con
- \(r_0\)es la distancia iónica más cercana
Calcular energía de celosía
La energía de celosía, basada en la ecuación de arriba, depende de múltiples factores. Vemos que la carga de iones es proporcional al incremento de la energía reticular. Además, a medida que los iones entran en contacto más cercano, la energía de la red también aumenta.
¿Qué compuesto tiene la mayor energía de celosía?
- AlF 3
- NaCl
- LiF
- CaCl 2
Solución
Esta pregunta requiere conocimientos básicos de la energía de celosía. Dado que F 3 le da al compuesto una carga positiva +3 y el Al le da al compuesto una carga negativa -1, el compuesto tiene una gran atracción electrostática. Cuanto mayor es la atracción electrostática, mayor es la energía de la red.
¿Cuál es la energía reticular del NaCl? (Pista: debe buscar los valores de las constantes para este compuesto)
Solución
-756 kJ/mol (nuevamente, este valor se encuentra en una tabla de constantes)
Calcular la energía reticular de NaCl.
Solución
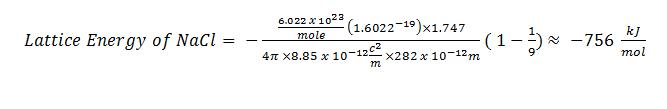
Referencias
- Johnson, D. A. Metales y Cambio Químico. Cambridge: Real Sociedad de Química, 2002.
- Cotton, F. Albert y F. Albert Cotton. Química Inorgánica Avanzada. Nueva York: Wiley, 1999.

