8.3: Vida media de los radioisótopos
- Page ID
- 77336
La vida media (t 1/2) de un radioisótopo es el tiempo que tarda la mitad de la muestra en descomponerse.
Cuenta la tasa de desintegración del radioisótopo: cuanto más rápida es la tasa de descomposición, cuanto más corta es la vida media.
Características generales de la vida media
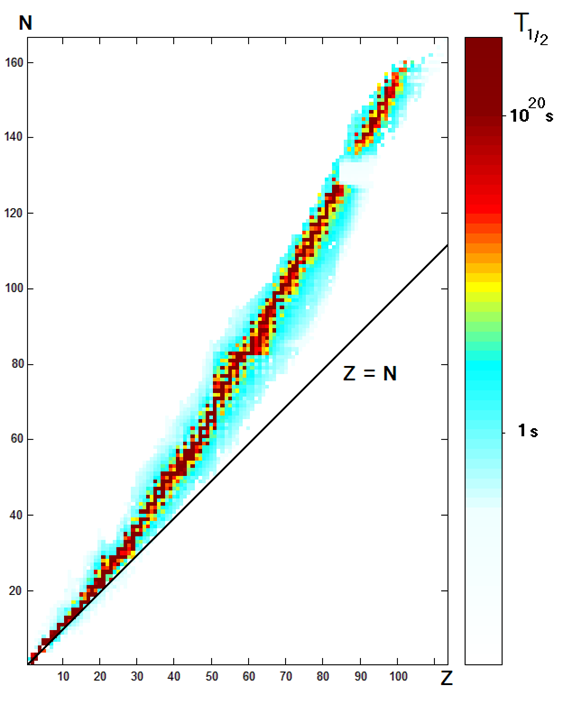
- La semivida es diferente para diferentes nucleoides, como se muestra en la Fig. 8.3.1, y en el Cuadro 1. Varía de una fracción de segundo a más de 10 20 s, es decir, más de 3 billones de años.
- Cuanto más lejos esté un nucleoide del nucleoide estable (mostrado por puntos negros en la Fig. 8.3.1), menos estable es y más rápido decae.
- La vida media es independiente de la concentración, temperatura y presión, es decir, la t 1/2 es una constante característica de un radioisótopo.
- Los isótopos radiactivos naturales suelen tener una vida media más larga, por ejemplo, t 1/2 carbono-14 es de 5730 años y el uranio-235 es de 7.0 x 10 8 años.
- Los radioisótopos utilizados para la imagen y el tratamiento en ciencias médicas suelen ser sintetizados y tienen una vida media corta para que no persistan en el cuerpo por un tiempo innecesariamente largo. Por ejemplo, el fósforo-32, el yodo-131 y el tecnecio-99m tienen vidas medias de 14.3 días, 8.1 días y 6.0 horas, respectivamente.
|
Radioisótopo |
Símbolo |
Vida media |
Uso |
|---|---|---|---|
|
Carbono-14 |
\(\ce{_6^14C}\) |
5730 años |
Datación por radioisótopos |
|
Hidrogeno-3 |
\(\ce{_1^3H}\) |
12.3 años |
Datación por radioisótopos |
|
Potasio-40 |
\(\ce{_19^40K}\) |
1.3 x 10 9 años |
Datación por radioisótopos |
|
Renio-187 |
\(\ce{_75^187Re}\) |
4.3 x 10 años |
Datación por radioisótopos |
|
Uranio-238 |
\(\ce{_92^238U}\) |
4.5 x 10 9 años |
Datación por radioisótopos |
|
Uranio-235 |
\(\ce{_92^235U}\) |
7.0 x 10 8 años |
Combustible para reactores nucleares |
|
Cobalto-60 |
\(\ce{_27^60Co}\) |
5.3 años |
Médico (fuente de radiación externa) |
|
Yodo-131 |
\(\ce{_53^131I}\) |
8.1 días |
Médico |
|
Plancha-59 |
\(\ce{_26^59Fe}\) |
45 días |
Médico |
|
Modeno-99 |
\(\ce{_42^99Mo}\) |
67 horas |
Médico |
|
Sodio-24 |
\(\ce{_11^24Na}\) |
15 horas |
Médico |
|
Tecnecio-99m |
\(\ce{_43^{99m}Te}\) |
6 horas |
Médico |
|
Fósforos-32 |
\(\ce{_15^32P}\) |
14.3 dsys |
Médico |
Curva de decaimiento de radioisótopos
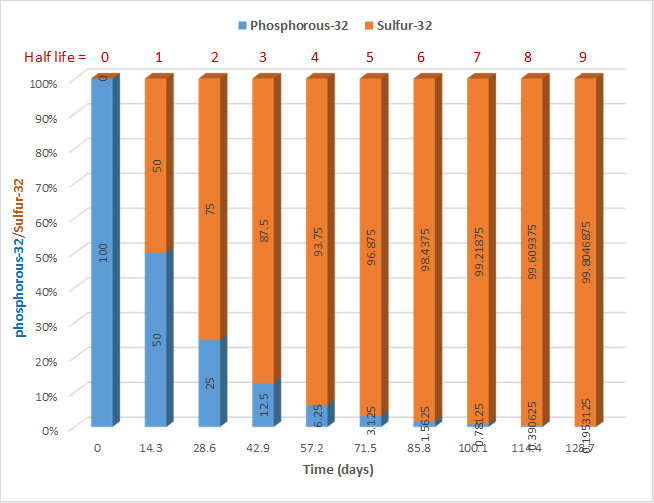
Durante cada semivida sucesiva, la mitad de la cantidad inicial se desintegrará radiactivamente, como se ilustra en la Fig. 8.3.2. para el caso del fósforo-32 que decae con una semivida de 14.3 días por la siguiente reacción nuclear
\[\ce{_15^32P -> _16^32S + _{-1}^{0}{e}}\nonumber\]
Supongamos que al principio hay 100 mg del fósforo-32; 50 mg quedarán atrás después de 14.3 días, es decir, después de 1 semivida; y 25 mg quedarán después de 28.6 días, es decir, después de 2 semividas. Una cantidad insignificante del isótopo parental fósforo-32 queda después de 9 semividas.
La cantidad de un radioisótopo restante después del tiempo dado se puede calcular a partir de la cantidad inicial conocida y el tiempo empleado, mediante la siguiente fórmula:
\[m_{f}=m_{i}(0.5)^{n}\nonumber\]
donde m i es la cantidad inicial, m f es la cantidad final, y n es el número de vidas medias pasadas. La fórmula funciona aunque el número de vidas medias no sea un número entero.
Si se inyectaron 50.0 mg de yodo-131 para tratamiento médico, ¿cuántos miligramos quedarán después de 40.5 días? (La vida media del yodo-131 es de 8.1 días)
Solución
Dado: m i = 50.0 mg, Tiempo = 40.5 días, ¿Deseado? m f
La igualdad: 1 medio vivo = 8.1 días, da los siguientes factores de conversión. \[\frac{1 \text { half-life }}{8.1 \text { days }} \quad\text{and}\quad \frac{8.1 \text { days }}{1 \text { half-life }}\nonumber\]
Para calcular las vidas medias, se multiplica el tiempo dado con el factor de conversión que cancela el tiempo:
\[n=40.5 \cancel{\text { days }} \times \frac{1 \text { half-life }}{8.1 \cancel{\text { days }}}=5 \text { half-lives }\nonumber\]
Para calcular la cantidad restante, ingrese los valores en la fórmula:
\[m_{f}=m_{i}(0.5)^{n}=50.0 \mathrm{mg}(0.5)^{5}=1.56 \mathrm{~mg}\nonumber\]
Datación por radioisótopos
La radiactividad natural se utiliza para establecer la edad de los objetos de interés arqueológico, antropológico o histórico. Todos los objetos vivos tienen carbono en su composición. El carbono-14 es un isótopo radiactivo de carbono con una vida media de 5730 años. El carbono-14 es producido por la transmutación de nitrógeno-14 tras el bombardeo de neutrones por rayos cósmicos, como se ilustra en la Fig. 8.3.3. Su concentración en una fuente de carbono para el organismo vivo permanece casi constante porque su descomposición contrarresta su producción por rayos cósmicos. Los organismos vivos repone continuamente el carbono, por lo que la concentración de carbono-14 permanece casi constante mientras el objeto esté vivo. Después de que el objeto muere, el carbono-14 disminuye con el tiempo, reduciéndose a la mitad después de una vida media. El isótopo carbono-12 no es radiactivo, por lo que su concentración se mantiene constante. La medición de la relación carbono-14/carbono-12 permite calcular la edad del objeto después de su muerte. La edad de las primeras civilizaciones, como los ejemplos de civilización del valle del Indo mostrados en la Fig. 8.3.4, fueron determinados por el método de datación por carbono-14.

Debido a que el carbono-14 disminuye con el tiempo, al objeto mayor de 20,000 años de edad no le queda suficiente carbono-14 para determinar su edad con precisión. Otros radioisótopos con una vida media más larga, por ejemplo, uranio-238 con una semivida de 4.5 x 10 9 años, se utilizan para determinar la edad de los objetos antiguos. Por ejemplo, la edad de las muestras de roca de la luna, como se muestra en la Fig. 8.3.5, se determinó mediante la datación por radioisótopos de uranio-238.



