3.9: Nombrar compuestos iónicos
- Page ID
- 72846
Objetivos de aprendizaje
- Escriba los nombres de los compuestos iónicos reconociendo y nombrando los iones en la unidad de fórmula.
Los compuestos iónicos se nombran usando la unidad de fórmula y siguiendo algunas convenciones importantes. Primero, el nombre del catión se escribe primero seguido del nombre del anión. Debido a que la mayoría de los metales forman cationes y la mayoría de los no metales forman aniones, las fórmulas suelen enumerar primero el metal y luego el no metal. Segundo, los cargos no están incluidos en el nombre (o la fórmula). Recuerde que en un compuesto iónico, las especies componentes son iones, no átomos neutros, aunque la fórmula no contenga cargas. La fórmula adecuada para un compuesto iónico mostrará cuántos de cada ion se necesitan para equilibrar las cargas positivas y negativas totales; el nombre no necesita incluir indicación de esta relación.
Existen dos tipos principales de compuestos iónicos con diferentes reglas de nomenclatura para cada uno; Tipo I: compuestos que contienen cationes de elementos del grupo principal y Tipo II: compuestos que contienen cationes de carga variable (generalmente metales de transición). A continuación veremos ejemplos de cada tipo para conocer las reglas para nombrar.
Compuestos Iónicos Tipo I
Los cationes de los elementos del grupo principal no tienen cargas variables y se nombran simplemente colocando primero el nombre del catión, seguido del nombre del anión, y dejando caer la palabra ion de ambas partes. Por ejemplo, ¿cuál es el nombre del compuesto cuya fórmula es\(\ce{Ba(NO3)2}\)?
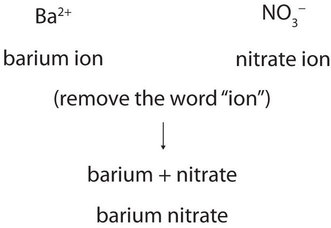
El nombre del compuesto no necesita indicar que hay dos iones nitrato por cada ion bario. Debe determinar la relación de iones en la unidad de fórmula equilibrando las cargas positivas y negativas.
Compuestos Iónicos Tipo II
Algunos metales pueden formar cationes con cargas variables. Al nombrar una fórmula para un compuesto iónico cuyo catión puede tener más de una posible carga, primero debe determinar la carga en el catión antes de identificar su nombre correcto. Por ejemplo, considere\(\ce{FeCl2}\) y\(\ce{FeCl3}\). En el primer compuesto, el ion hierro tiene una carga 2+ porque hay dos\(\ce{Cl^{−}}\) iones en la fórmula (1− carga en cada ion cloruro). En el segundo compuesto, el ion hierro tiene una carga 3+, como lo indican los tres\(\ce{Cl^{−}}\) iones en la fórmula. Estos son dos compuestos diferentes que necesitan dos nombres diferentes. Por el sistema de stock, los nombres son cloruro de hierro (II) y cloruro de hierro (III). Si usáramos los tallos y sufijos del sistema común, los nombres serían cloruro ferroso y cloruro férrico, respectivamente.
Todos los días te encuentras y usas una gran cantidad de compuestos iónicos. Algunos de estos compuestos, donde se encuentran, y para qué se utilizan se listan en la Tabla\(\PageIndex{1}\). Mira la etiqueta o lista de ingredientes de los diversos productos que usas durante los próximos días, y mira si te encuentras con alguno de los de esta tabla, o encuentras otros compuestos iónicos que ahora podrías nombrar o escribir como fórmula.
| Compuesto iónico | Nombre | Uso |
|---|---|---|
| NaCl | cloruro de sodio | sal de mesa ordinaria |
| KI | yoduro de potasio | agregado a la sal “yodada” para la salud de la tiroides |
| NaF | fluoruro de sodio | ingrediente en pasta de dientes |
| NaHCo 3 | bicarbonato de sodio | bicarbonato de sodio; utilizado en la cocina (y en antiácidos) |
| Na 2 CO 3 | carbonato de sodio | refresco de lavado; utilizado en agentes de limpieza |
| NaOCl | hipoclorito de sodio | ingrediente activo en lejía doméstica |
| CaCo 3 | carbonato de calcio | ingrediente en antiácidos |
| Mg (OH) 2 | hidróxido de magnesio | ingrediente en antiácidos |
| Al (OH) 3 | hidróxido de aluminio | ingrediente en antiácidos |
| NaOH | hidróxido de sodio | lejía; utilizado como limpiador de desagües |
| K 3 PO 4 | fosfato de potasio | aditivo alimentario (muchos propósitos) |
| MgSO 4 | sulfato de magnesio | añadido al agua purificada |
| Na 2 HPO 4 | hidrogenofosfato de sodio | agente antiapelmazante; utilizado en productos en polvo |
| Na 2 SO 3 | sulfito de sodio | conservante |
A medida que practiques nombrar compuestos, usa Figura\(\PageIndex{1}\) como guía.
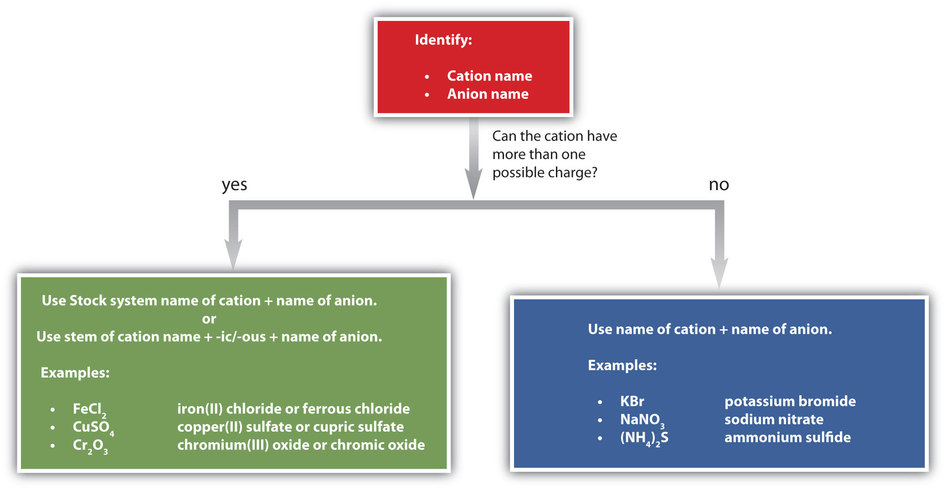
Ejemplo\(\PageIndex{3}\)
Nombrar cada compuesto iónico, utilizando ambos sistemas Stock y comunes si es necesario.
- Ca 3 (PO 4) 2
- (NH 4) 2 Cr 2 O 7
- KCl
- CuCl
- SnF 2
- Contestar a
-
fosfato de calcio
- Respuesta b
-
dicromato de amonio (el prefijo di - es parte del nombre del anión)
- Respuesta c
-
cloruro de potasio
- Respuesta d
-
cloruro de cobre (I) o cloruro cuproso
- Respuesta e
-
fluoruro de estaño (II) o fluoruro estannoso
Ejercicio\(\PageIndex{3}\)
Nombrar cada compuesto iónico, utilizando ambos sistemas Stock y comunes si es necesario.
- ZnBr 2
- Fe (NO 3) 3
- Al 2 O 3
- CuF 2
- AgF
- Contestar a
-
bromuro de zinc
- Respuesta b
-
nitrato de hierro (III) o nitrato férrico
- Respuesta c
-
óxido de aluminio
- Respuesta d
-
fluoruro de cobre (II) o fluoruro cúprico
- Respuesta e
-
fluoruro de plata


