14.9: Compuestos que contienen halógeno
- Page ID
- 73426
- Identificar y nombrar un haluro de alquilo simple.
La presencia de un átomo de halógeno (F, Cl, Br o I; además, X se usa para representar cualquier átomo de halógeno) es uno de los grupos funcionales más simples. Los compuestos orgánicos que contienen un átomo de halógeno se denominan haluros de alquilo. Ya hemos visto algunos ejemplos de haluros de alquilo cuando se introdujo la adición de halógenos a través de dobles y triples enlaces en la Sección 16.3 - “Hidrocarburos Ramificados”; los productos de estas reacciones fueron haluros de alquilo.
Un haluro de alquilo simple puede denominarse como una sal iónica, primero indicando el nombre del alcano parental como grupo sustituyente (con el sufijo -yl) y luego el nombre del halógeno como si fuera el anión. Entonces CH 3 Cl tiene el nombre común de cloruro de metilo, mientras que CH 3 CH 2 Br es bromuro de etilo y CH 3 CH 2 CH 2 I es yoduro de propilo. Sin embargo, este sistema no es ideal para haluros de alquilo más complicados.
La forma sistemática de nombrar haluros de alquilo es nombrar al halógeno como sustituyente, al igual que un grupo alquilo, y usar números para indicar la posición del átomo de halógeno en la cadena principal. El nombre del halógeno como sustituyente proviene del tallo del nombre del elemento más el final -o, por lo que los nombres de los sustituyentes son fluoro -, cloro -, bromo - y iodo -. Si hay más de uno de un determinado halógeno, utilizamos prefijos numéricos para indicar el número de cada tipo, al igual que con los grupos alquilo. Por ejemplo, esta molécula
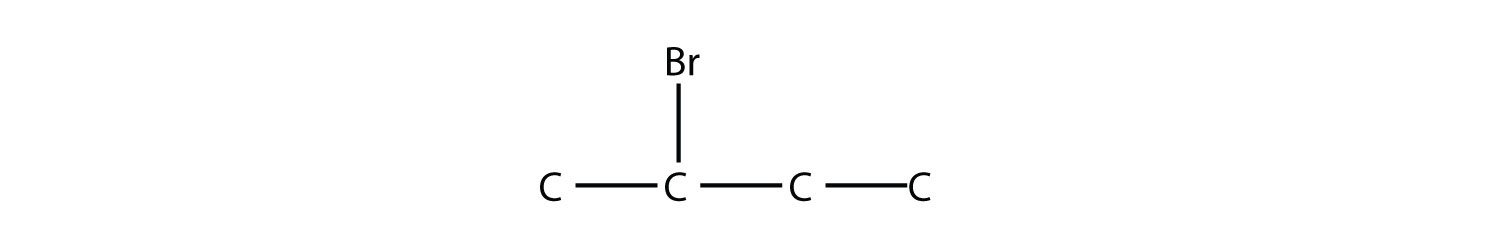
es 2-bromobutano, mientras que esta molécula
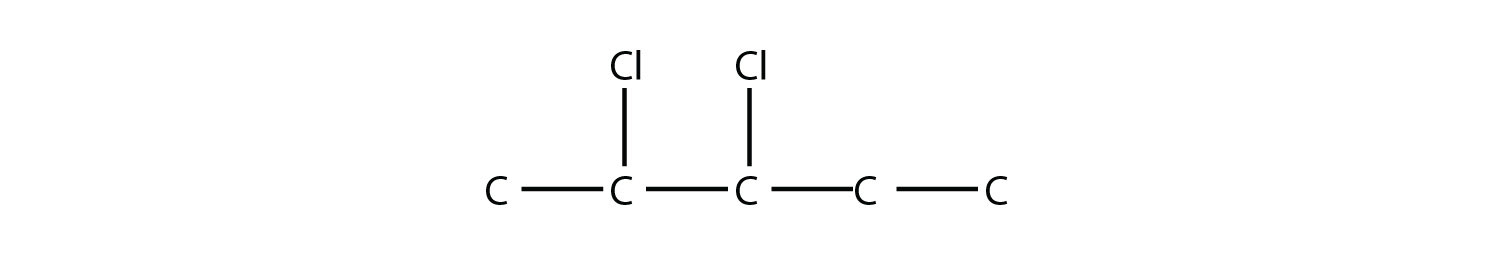
es 2,3-dicloropentano. Si están presentes grupos alquilo, los sustituyentes se enumeran alfabéticamente. Los prefijos numéricos se ignoran al determinar el orden alfabético de los grupos sustituyentes.
Nombra esta molécula.
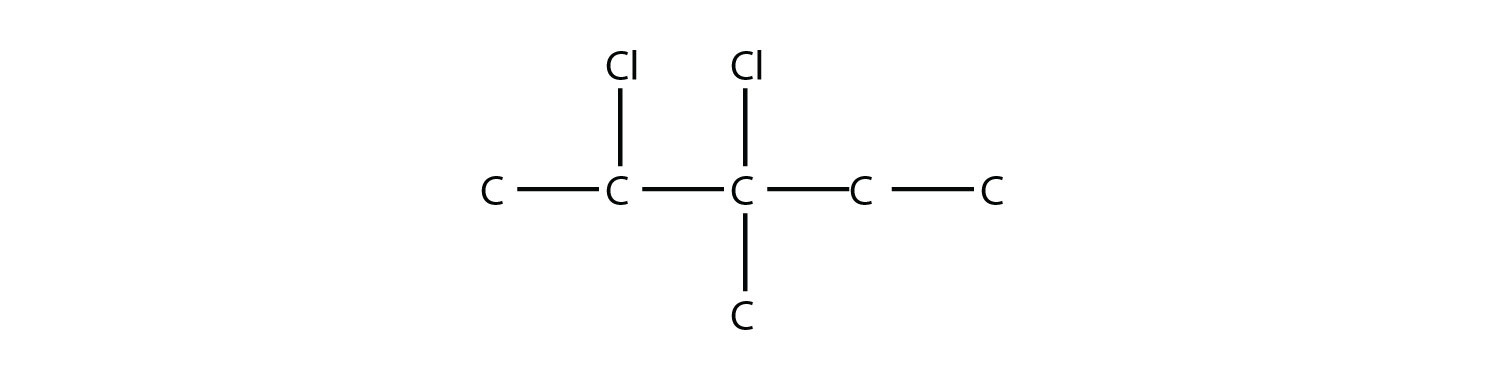
Solución
La cadena de carbono más larga tiene cinco átomos de C, por lo que la molécula es un pentano. Hay dos sustituyentes de cloro ubicados en el segundo y tercer átomos de C, con un grupo metilo de un carbono en el tercer átomo de C también. El nombre correcto para esta molécula es 2,3-dicloro-3-metilpentano.
Nombra esta molécula.
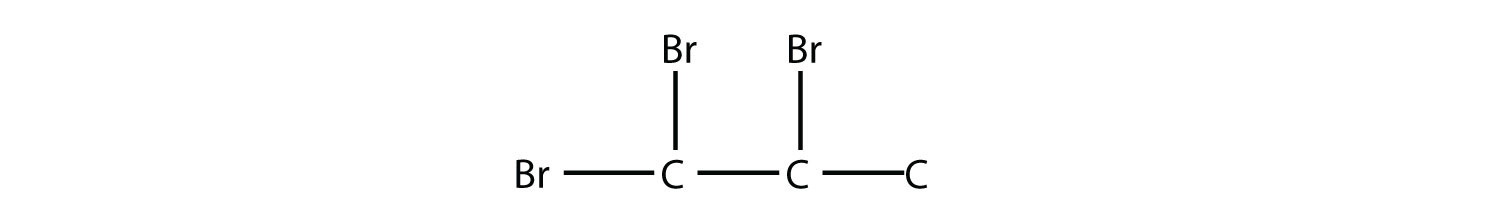
- Contestar
-
1,1,2-tribromopropano
La mayoría de los haluros de alquilo son insolubles en H 2 O. Los alcoholes más pequeños, sin embargo, son muy solubles en H 2 O porque estas moléculas pueden participar en enlaces de hidrógeno con moléculas de H 2 O. Para moléculas más grandes, sin embargo, el grupo OH polar está abrumado por la parte alquílica no polar de la molécula. Mientras que el metanol es soluble en H 2 O en todas las proporciones, solo aproximadamente 2.6 g de pentanol se disolverán en 100 g de H 2 O. Los alcoholes más grandes tienen una solubilidad aún menor en H 2 O.
Una reacción común a los alcoholes y haluros de alquilo es la eliminación, la eliminación del grupo funcional (ya sea X u OH) y un átomo de H de un carbono adyacente. La reacción general se puede escribir de la siguiente manera:
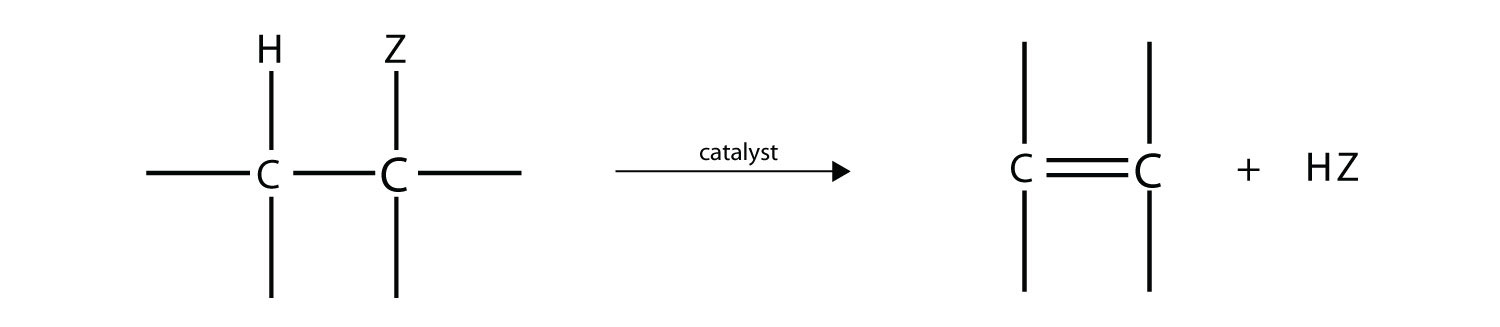
donde Z representa el grupo X o el grupo OH. La mayor diferencia entre la eliminación en haluros de alquilo y la eliminación en alcoholes es la identidad del catalizador: para los haluros de alquilo, el catalizador es una base fuerte; para los alcoholes, el catalizador es un ácido fuerte. Para los compuestos en los que hay átomos de H en más de un carbono adyacente, resulta una mezcla de productos.
Predecir el/los producto (s) orgánico (s) de esta reacción.
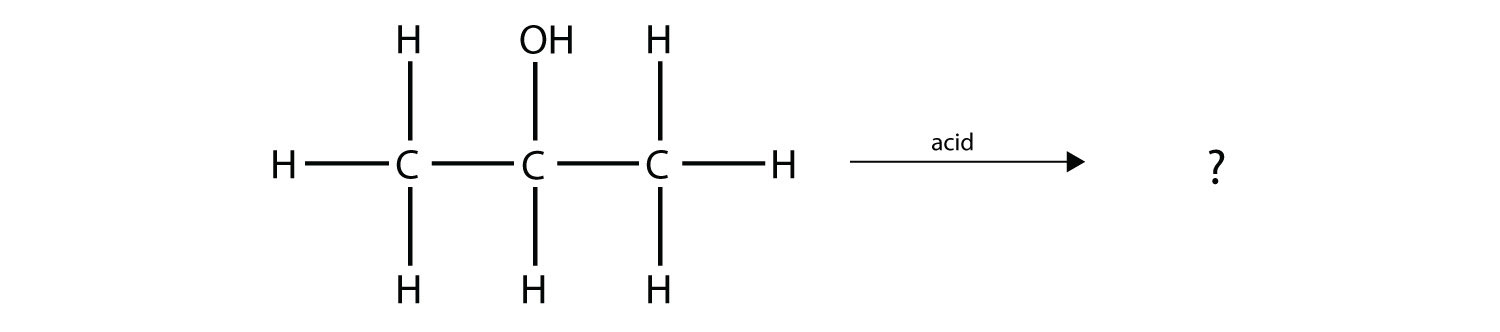
Solución
Bajo estas condiciones, se eliminará una molécula de HOH (también conocida como H 2 O) y se formará un alqueno. No importa qué carbono adyacente pierde el átomo de H; en cualquier caso el producto será
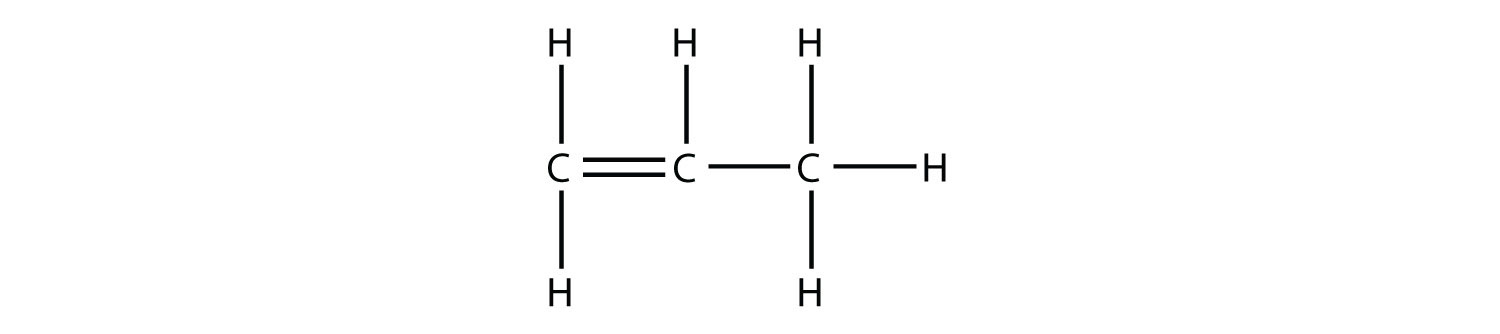
que es propeno.
Predecir el/los producto (s) orgánico (s) de esta reacción.
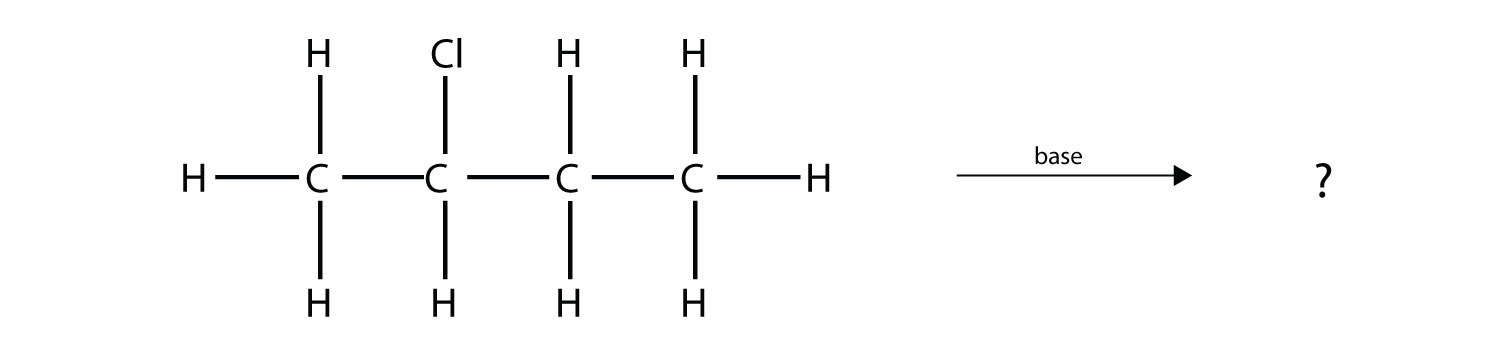
- Contestar
-
1-buteno y 2-buteno
Claves para llevar
- Los haluros de alquilo tienen un átomo de halógeno como grupo funcional.
- Los alcoholes tienen un grupo OH como grupo funcional.
- Las reglas de nomenclatura nos permiten nombrar haluros y alcoholes de alquilo.
- En una reacción de eliminación, se forma un doble enlace a medida que se elimina un HX o una molécula HOH.

