16.5: Basicidad de las aminas
- Page ID
- 73084
- Nombrar las reacciones típicas que tienen lugar con aminas.
- Describir aminas heterocíclicas
Recordemos que el amoníaco (NH 3) actúa como base porque el átomo de nitrógeno tiene un par solitario de electrones que pueden aceptar un protón. Las aminas también tienen un par de electrones solitarios en sus átomos de nitrógeno y pueden aceptar un protón del agua para formar iones amonio sustituido (NH 4 +) e iones hidróxido (OH -):
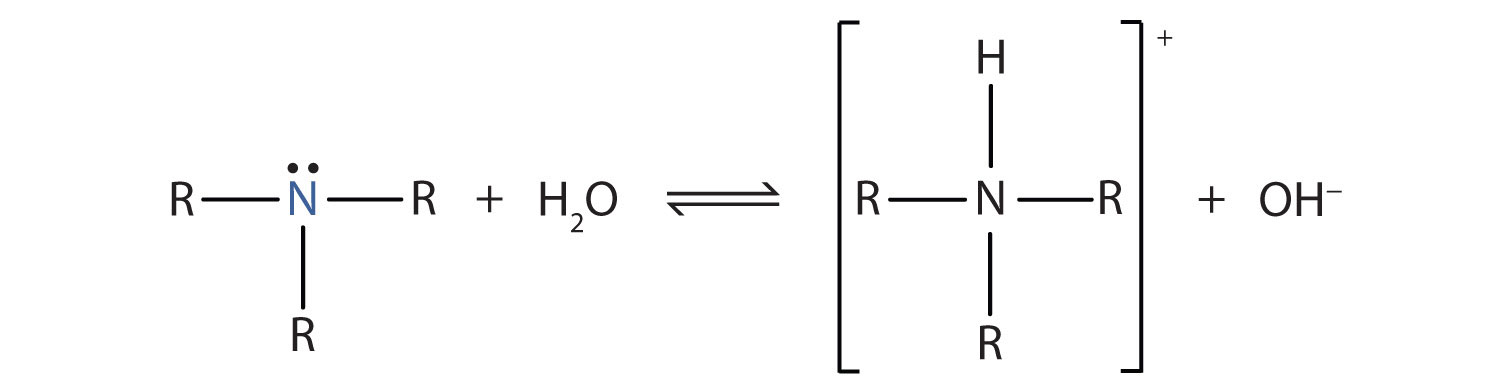
Como ejemplo específico, la metilamina reacciona con el agua para formar el ion metilamonio y el ion OH −.
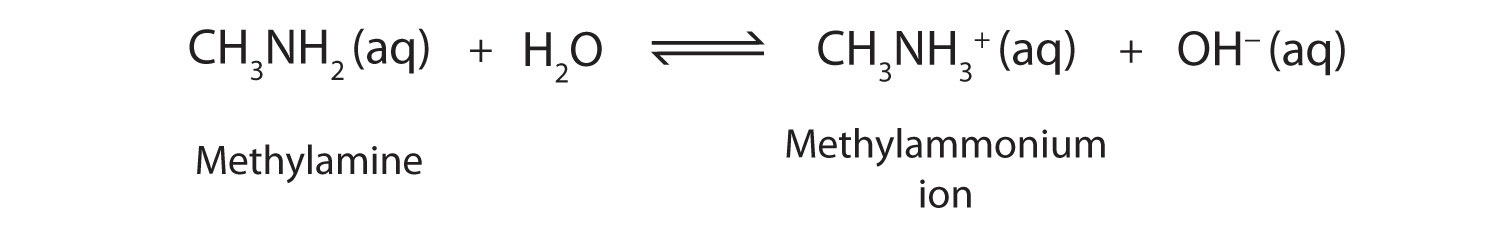
Casi todas las aminas, incluidas las que no son muy solubles en agua, reaccionarán con ácidos fuertes para formar sales solubles en agua.
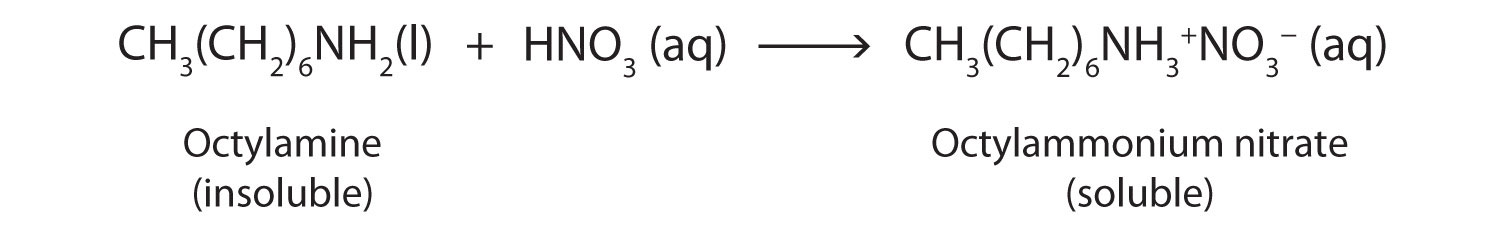
Las sales de amina se denominan como otras sales: el nombre del catión va seguido del nombre del anión.
¿Cuáles son las fórmulas del ácido y base que reaccionan para formar [CH 3 NH 2 CH 2 CH 3] + CH 3 COO −?
Solución
El catión tiene dos grupos —metilo y etilo— unidos al átomo de nitrógeno. Proviene de etilmetilamina (CH 3 NHCH 2 CH 3). El anión es el ion acetato. Proviene del ácido acético (CH 3 COOH).
¿Cuáles son las fórmulas del ácido y base que reaccionan para formar (CH 3 CH 2 CH 2) 3 NH + I −?
Las sales de anilina se denominan propiamente como compuestos de anilinio, pero un sistema más antiguo, aún en uso para nombrar medicamentos, identifica la sal de anilina y ácido clorhídrico como “clorhidrato de anilina”. Estos compuestos son iónicos, son sales, y las propiedades de los compuestos (solubilidad, por ejemplo) son las características de las sales. Muchos fármacos que son aminas se convierten en sales hidrocloruro para aumentar su solubilidad en solución acuosa.

