6.22: Tendencias Periódicas - Carácter Metálico y No Metálico
- Page ID
- 70523
¿Qué comemos como nación?
La gráfica anterior indica algunas tendencias en la dieta estadounidense durante un periodo de treinta años. Al observar la dirección en la que van nuestros hábitos alimenticios, se pueden tomar medidas para ayudar a prevenir los malos hábitos alimenticios y disminuir problemas como la presión arterial alta y los ataques cardíacos.
El desarrollo de la tabla periódica ha ayudado a organizar la información química de muchas maneras. Ahora podemos ver tendencias entre propiedades de diferentes átomos y hacer predicciones sobre el comportamiento de materiales específicos.
Carácter Metálico y No Metálico
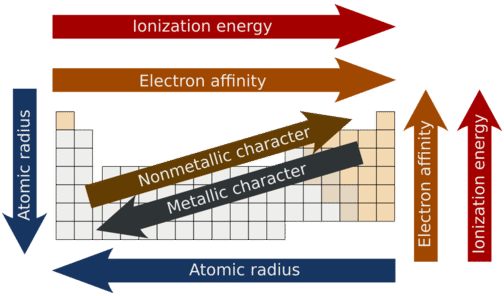
Carácter metálico se refiere al nivel de reactividad de un metal. Los metales tienden a perder electrones en las reacciones químicas, como lo indican sus bajas energías de ionización. Dentro de un compuesto, los átomos metálicos tienen una atracción relativamente baja para los electrones, como lo indican sus bajas electronegatividades. Al seguir el resumen de tendencias en la siguiente figura, se puede ver que los metales más reactivos residirían en la parte inferior izquierda de la tabla periódica. El metal más reactivo es el cesio, el cual no se encuentra en la naturaleza como elemento libre. Reacciona explosivamente con el agua y se encenderá espontáneamente en el aire. El francio está por debajo del cesio en el grupo de los metales alcalinos, pero es tan raro que la mayoría de sus propiedades nunca se han observado.
La reactividad de los metales se basa en procesos como la formación de compuestos halogenuros con halógenos, y la facilidad con la que el elemento desplaza el hidrógeno de los ácidos diluidos.
El carácter metálico aumenta a medida que bajas un grupo. Dado que la energía de ionización disminuye bajando un grupo (o aumenta subiendo un grupo), la mayor capacidad para que los metales más bajos en un grupo pierdan electrones los hace más reactivos. Además, el radio atómico aumenta bajando un grupo, colocando los electrones externos más lejos del núcleo y haciendo que ese electrón sea menos atraído por el núcleo.
Los no metales tienden a ganar electrones en las reacciones químicas, y tienen una alta atracción para los electrones dentro de un compuesto. Los no metales más reactivos residen en la parte superior derecha de la tabla periódica. Dado que los gases nobles son un grupo especial por su falta de reactividad, el elemento flúor es el no metálico más reactivo. No se encuentra en la naturaleza como elemento libre. El gas flúor reacciona explosivamente con muchos otros elementos y compuestos, y es considerado como una de las sustancias conocidas más peligrosas.
Tenga en cuenta que no existe una división clara entre el carácter metálico y el no metálico. A medida que avanzamos a través de la tabla periódica, hay una tendencia creciente a aceptar electrones (no metálicos) y una disminución en la posibilidad de que un átomo renuncie a uno o más electrones.
Resumen
- Carácter metálico se refiere al nivel de reactividad de un metal.
- El carácter no metálico se relaciona con la tendencia a aceptar electrones durante las reacciones químicas.
- La tendencia metálica aumenta bajando un grupo.
- La tendencia no metálica aumenta de izquierda a derecha a través de la tabla periódica.
Revisar
- Define “carácter metálico”.
- Define “carácter no metálico”.
- Describir la tendencia en carácter metálico bajando un grupo.
- Describir la tendencia en el carácter no metálico recorriendo la tabla periódica.
- ¿Por qué aumenta el carácter metálico a medida que bajas un grupo?


