13.7: Evaporación
- Page ID
- 70447
¿Cuál es la caja en el techo de la casa?
En el techo de la casa que se muestra a continuación hay un dispositivo conocido como “enfriador de pantano”. Esta pieza de equipo remonta su origen a los antiguos egipcios, quienes colgaron mantas mojadas a través de las puertas de sus hogares. A medida que el aire caliente pasaba por las mantas, el agua se evaporaría y enfriaría el aire. La realeza fue un paso más allá, e hizo que los sirvientes abanicaran paños mojados sobre jarras de agua para obtener más evaporación y enfriamiento.
Se desconoce el origen del término “enfriador de pantano”; ciertamente no funcionan en un pantano. Las mejores condiciones para el enfriamiento incluyen una temperatura alta (sobre\(80^\text{o} \text{F}\)) y una humedad baja (preferiblemente menor que\(30\%\)). Estos refrigeradores funcionan bien en zonas desérticas, pero no proporcionan ningún enfriamiento en las zonas húmedas del país.
Evaporación
Un charco de agua que queda intacto finalmente desaparece. Las moléculas líquidas escapan a la fase gaseosa, convirtiéndose en vapor de agua. La vaporización es el proceso en el que un líquido se convierte en un gas. La evaporación es la conversión de un líquido a su vapor por debajo de la temperatura de ebullición del líquido. Si el agua se mantiene en un recipiente cerrado, las moléculas de vapor de agua no tienen oportunidad de escapar a los alrededores, por lo que el nivel del agua no cambia. A medida que algunas moléculas de agua se convierten en vapor, un número igual de moléculas de vapor de agua se condensan de nuevo al estado líquido. La condensación es el cambio de estado de un gas a un líquido.
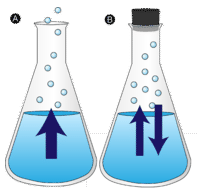
Para que una molécula líquida escape al estado gaseoso, la molécula debe tener suficiente energía cinética para superar las fuerzas de atracción intermoleculares en el líquido. Recordemos que una muestra líquida dada tendrá moléculas con un amplio rango de energías cinéticas. Las moléculas líquidas que tienen este cierto umbral de energía cinética escapan de la superficie y se convierten en vapor. Como resultado, las moléculas líquidas que quedan ahora tienen menor energía cinética. A medida que se produce la evaporación, la temperatura del líquido restante disminuye. Se han observado los efectos del enfriamiento evaporativo. En un día caluroso, las moléculas de agua en tu transpiración absorben el calor corporal y se evaporan de la superficie de tu piel. El proceso de evaporación deja la transpiración restante más fría, que a su vez absorbe más calor de tu cuerpo.
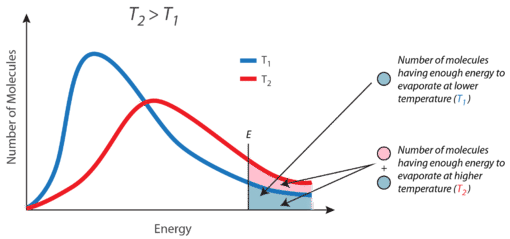
Un líquido dado se evaporará más rápidamente cuando se caliente. Esto se debe a que el proceso de calentamiento da como resultado que una mayor fracción de las moléculas del líquido tenga la energía cinética necesaria para escapar de la superficie del líquido. La siguiente figura muestra la distribución de energía cinética de moléculas líquidas a dos temperaturas. Los números de moléculas que tienen la energía cinética requerida para evaporarse se muestran en el área sombreada bajo la curva a la derecha. El líquido de mayor temperatura\(\left( T_2 \right)\) tiene más moléculas que son capaces de escapar a la fase de vapor que el líquido de menor temperatura\(\left( T_1 \right)\).
Explore cómo el calor y la temperatura se relacionan con el cambio de fase en esta simulación:
Resumen
- La evaporación es la conversión de un líquido a su vapor por debajo de la temperatura de ebullición del líquido.
- La condensación es el cambio de estado de un gas a un líquido.
- A medida que aumenta la temperatura, aumenta la velocidad de evaporación.
Revisar
- Definir vaporización.
- Definir evaporación.
- Definir condensación.
- ¿Cómo afecta la temperatura a la velocidad de evaporación?


