29.4: Fuerzas entre Cadenas de Polímero
- Page ID
- 73193
Los polímeros se producen a escala industrial principalmente, aunque no exclusivamente, para su uso como materiales estructurales. Sus propiedades físicas son particularmente importantes para determinar su utilidad, ya sea como llantas de goma, revestimientos para edificios o combustibles sólidos para cohetes.
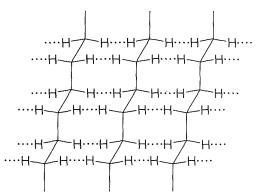
Los polímeros que no están altamente reticulados tienen propiedades que dependen en gran medida de las fuerzas que actúan entre las cadenas. A modo de ejemplo, consideremos un polímero como el polietileno que, en una muestra comercial normal, estará conformado por moléculas que tengan de 1000 a 2000\(\ce{CH_2}\) grupos en cadenas continuas. Debido a que el material es una mezcla de diferentes moléculas, no se espera que cristalice de manera convencional. \(^2\)Sin embargo, la difracción de rayos X muestra que el polietileno tiene un carácter cristalino muy considerable, existiendo regiones tan grandes como varios cientos de unidades angstrom de longitud, las cuales tienen cadenas ordenadas de\(\ce{CH_2}\) grupos orientados entre sí como las cadenas en cristales de bajo peso molecular. hidrocarburos en peso. Estas regiones cristalinas se denominan cristalitos (Figura 29-3). Entre los cristalitos de polieteno se encuentran regiones amorfas, no cristalinas en las que las cadenas poliméricas están esencialmente ordenadas aleatoriamente entre sí (Figura 29-4). Estas regiones constituían defectos cristalinos.
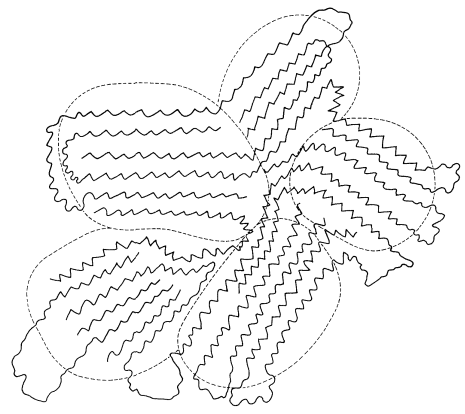
Las fuerzas entre las cadenas en los cristalitos de polieteno son las llamadas fuerzas de van der Waals o de dispersión, que son las mismas fuerzas que actúan entre las moléculas de hidrocarburos en los estados líquido y sólido, y, en menor medida, en el estado vapor. Estas fuerzas son relativamente débiles y surgen a través de la sincronización de los movimientos de los electrones en los átomos separados a medida que se acercan entre sí. La fuerza atractiva que resulta es rápidamente superada por fuerzas repulsivas cuando los átomos se acercan mucho entre sí (ver Figura 12-9, que muestra cómo la energía potencial entre un par de átomos varía con la distancia internuclear). Las fuerzas intermoleculares atractivas entre pares de hidrógenos en los cristalitos de polieteno son solo aproximadamente\(0.1\) -\(0.2 \: \text{kcal mol}^{-1}\) por par, pero para un segmento cristalino de 1000\(\ce{CH_2}\) unidades, la suma de estas interacciones bien podría ser mayor que las resistencias de\(\ce{C-C}\) unión. Así, cuando una muestra del polímero cristalino se somete a tensión hasta el punto en que se fractura, se rompen los enlaces carbono-carbono y se generan radicales que pueden detectarse por espectroscopía esr (Sección 27-9).
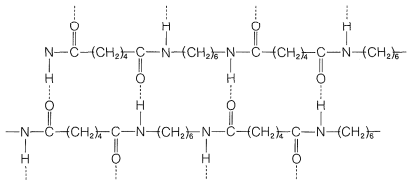
En otros tipos de polímeros, se pueden producir fuerzas intermoleculares aún más fuertes mediante enlaces de hidrógeno. Esto es especialmente importante en las poliamidas, como los nylons, de los cuales el nylon 66 es el más utilizado (Figura 29-5).
El efecto de la temperatura sobre las propiedades físicas de los polímeros es muy importante para sus usos prácticos. A bajas temperaturas, los polímeros se vuelven duros y vítreos porque los movimientos de los segmentos de las cadenas poliméricas con relación entre sí son lentos. La temperatura aproximada por debajo de la cual el comportamiento vítreo es aparente se llama temperatura del vidrio y se simboliza por\(T_g\). Cuando se calienta un polímero que contiene cristalitos, los cristalitos finalmente se funden, y esta temperatura generalmente se llama temperatura de fusión y se simboliza como\(T_m\). Por lo general, la temperatura de moldeo estará por encima\(T_m\) y la resistencia mecánica del polímero disminuirá rápidamente a medida que se aproxime la temperatura\(T_m\).
Otra temperatura de gran importancia en el uso práctico de polímeros es la temperatura a la que se produce la descomposición térmica de las cadenas poliméricas. Las temperaturas de descomposición obviamente serán sensibles a las impurezas, como el oxígeno, y estarán fuertemente influenciadas por la presencia de inhibidores, antioxidantes, etc. Sin embargo, habrá una temperatura (generalmente bastante alta,\(200^\text{o}\) a\(400^\text{o}\)) a la que la escisión no catalizada de los enlaces en una cadena se llevará a cabo a una velocidad apreciable y, en general, no se puede esperar que este tipo de reacción provoque la degradación del polímero. Claramente, si esta temperatura de degradación es comparable a\(T_m\), como lo es para el polipropenonitrilo (poliacrilonitrilo), se esperan dificultades en el moldeo térmico simple del plástico. Esta dificultad se supera en la fabricación de fibras de polipropenonitrilo (Orlon) disolviendo el polímero en\(\ce{N}\)\(\ce{N}\) dimetilmetanamida y forzando la solución a través de orificios finos hacia un espacio de aire caliente donde se evapora el disolvente.
Las propiedades físicas como la resistencia a la tracción, el patrón de difracción de rayos X, la resistencia al flujo de plástico, el punto de reblandecimiento y la elasticidad de la mayoría de los polímeros se pueden entender de manera general en términos de cristalitos, regiones amorfas, el grado de flexibilidad de las cadenas, reticulaciones y la resistencia de las fuerzas actuando entre las cadenas (fuerzas de dispersión, enlaces de hidrógeno, etc.). Una buena manera de apreciar la interacción entre las propiedades físicas y la estructura es comenzar con una clasificación aproximada de las propiedades de los polímeros sólidos de acuerdo con la forma en que las cadenas están dispuestas entre sí.
- Un polímero amorfo es uno sin cristalitos. Si las fuerzas de atracción entre las cadenas son débiles y si los movimientos de la cadena no están de alguna manera severamente restringidos como por reticulación o grandes barreras rotacionales, se esperaría que dicho polímero tuviera baja resistencia a la tracción y cuando se tensa sufra un flujo plástico en el que las cadenas se deslizan por una otro.
- Un polímero cristalino no orientado es uno que está considerablemente cristalizado pero tiene los cristalitos esencialmente orientados aleatoriamente uno con respecto al otro, como en la Figura 29-4. Cuando dichos polímeros se calientan suelen mostrar\(T_m\) puntos bastante afilados, que corresponden a la fusión de los cristalitos. Arriba\(T_m\), estos polímeros son amorfos y experimentan flujo plástico, lo que les permite ser moldeados. Al igual que otras cosas, esperamos\(T_m\) ser mayores para polímeros con cadenas rígidas (barreras altas a la rotación interna).
- Un polímero cristalino orientado es aquel en el que los cristalitos están orientados uno con respecto al otro, generalmente como resultado de un proceso de estirado en frío. Consideremos un polímero como el nylon, que tiene fuertes fuerzas intermoleculares y, cuando se prepara por primera vez, se encuentra en un estado desorientado como el representado por la Figura 29-4. Cuando el material es sometido a fuertes esfuerzos en una dirección, generalmente arriba para que\(T_g\) pueda ocurrir algo de flujo plástico, el material se alarga y los cristalitos son estirados juntos y orientados a lo largo de la dirección de la tensión aplicada (Figura 29-6).
Un polímero cristalino orientado generalmente tiene una resistencia a la tracción mucho mayor que el polímero no orientado. El estirado en frío es un paso importante en la producción de fibras sintéticas.
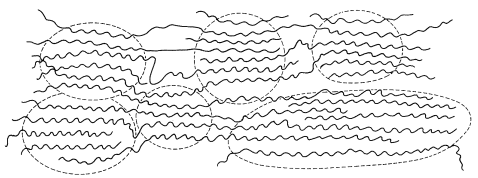
- Los elastómeros suelen ser polímeros amorfos. La clave del comportamiento elástico es tener cadenas altamente flexibles con fuerzas suficientemente débiles entre las cadenas o una estructura suficientemente irregular para ser inestables en el estado cristalino. La tendencia de las cadenas a cristalizar a menudo se puede reducir considerablemente mediante la introducción aleatoria de grupos metilo, que por impedimento estérico inhiben el orden de las cadenas. Un elastómero útil necesita tener algún tipo de región reticulada para evitar el flujo de plástico y cadenas lo suficientemente flexibles como para tener una baja\(T_g\). La estructura de un polímero de este tipo se muestra esquemáticamente en la Figura 29-7; la diferencia importante entre este elastómero y el polímero cristalino de la Figura 29-4 es el tamaño de las regiones amorfas. Cuando se aplica tensión y el material se alarga, las cadenas en las regiones amorfas se enderezan y se vuelven más casi paralelas. En el límite elástico, se alcanza un estado semicristalino, el cual es diferente al producido por estirado en frío de un polímero cristalino en que es estable solo mientras está bajo tensión. Las fuerzas entre las cadenas son demasiado débiles para mantener el estado cristalino en ausencia de tensión. Así, cuando se libera la tensión, se produce la contracción y se produce el polímero amorfo original. La entropía (Sección 4-4B) de las cadenas es más favorable en el estado relajado que en el estado estirado.
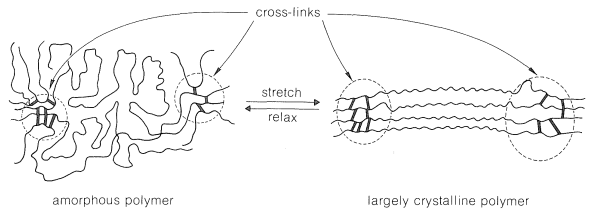
Un buen elastómero no debe sufrir flujo plástico ni en el estado estirado ni relajado, y cuando se estira debe tener un “recuerdo” de su estado relajado. Estas condiciones se logran mejor con caucho natural (cis-poli-2-metil-1,3-butadieno, cis-poliisopreno; Sección 13-4) curando (vulcanizando) con azufre. El caucho natural es pegajoso y experimenta flujo de plástico con bastante facilidad, pero cuando se calienta con\(1\) - en\(8\%\) peso de azufre elemental en presencia de un acelerador, se introducen reticulaciones de azufre entre las cadenas. Estas reticulaciones reducen el flujo de plástico y proporcionan un marco de referencia para que el polímero estirado regrese cuando se le permite relajarse. Demasiado azufre destruye completamente las propiedades elásticas y produce caucho duro del tipo utilizado en estuches para baterías de almacenamiento.
La química de la vulcanización del caucho es compleja. La reacción del caucho con el azufre se ve notablemente acelerada por sustancias llamadas aceleradores, de las cuales los comúnmente conocidos como mercaptobenzotiazol y disulfuro de tetrametiltiuram son ejemplos:
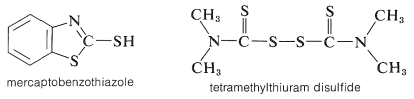
Claramente, los dobles enlaces en el caucho natural son esenciales para la vulcanización porque el caucho hidrogenado (“hidrorcaucho”) no está vulcanizado por azufre. El grado de insaturación disminuye durante la vulcanización, aunque la disminución es mucho menor que un doble enlace por átomo de azufre introducido. Existe evidencia de que el ataque ocurre tanto en el doble enlace como en el hidrógeno adyacente (de manera similar a algunas halogenaciones; Sección 14-3A) dando reticulaciones posiblemente de los siguientes tipos:
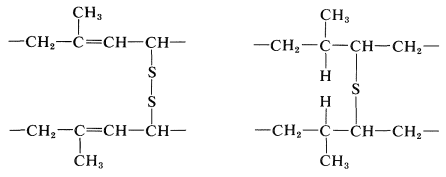
Los aceleradores probablemente funcionan actuando como portadores de azufre desde el azufre elemental hasta los sitios del polímero donde se forman las reticulaciones.
\(^2\)Se han formado cristales de tipo placa bastante buenos, aproximadamente\(100 \: \text{Å}\) gruesos, a partir de soluciones diluidas de polietileno. En estos cristales,\(\ce{CH_2}\) cadenas en la anti conformación (Sección 5-2) discurren entre las grandes superficies de las placas. Sin embargo, la evidencia es fuerte de que cuando las\(\ce{CH_2}\) cadenas alcanzan la superficie del cristal no se pliegan ordenadamente y vuelven a bajar a la otra superficie. En cambio, las partes de una cadena dada que están en los segmentos cristalinos parecen estar conectadas en los extremos de los cristalitos por bucles aleatorios de\(\ce{CH_2}\) secuencias desordenadas, algo así como una centralita telefónica anticuada.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


