1.5: Ácidos fosfóricos quirales (PA)
- Page ID
- 73339
Los ácidos fosfóricos quirales (PA) derivados de BINOL ópticamente activo que portan sustituyentes 3,3'-se han utilizado como catalizadores quirales eficaces para diversas transformaciones orgánicas. Los ácidos fosfóricos actúan como catalizadores bifuncionales que llevan tanto el sitio ácido de Brønsted como un sitio básico de Lewis y los sustituyentes 3,3'-juegan un papel crucial en la obtención de una alta estereoinducción mediante el control de las propiedades estructurales y electrónicas.
Catálisis Asimétrica Dirigida por Conterión (ACDC)
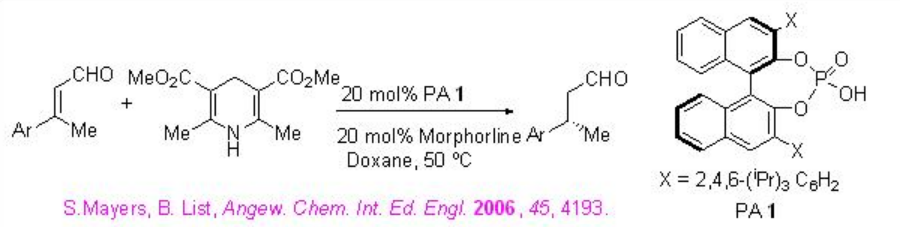
ACDC es un nuevo concepto de síntesis enantioselectiva. En 2006, el grupo List reportó por primera vez el concepto de ACDC para la 1,4-hidrogenación de aldehídos α, β -insaturados usando la combinación de morfolina y PA 1 a temperatura moderada (Esquema\(\PageIndex{1}\)). En esta reacción, el PA 1 reacciona con morfolina para dar la sal morfolina del anión quiral PA 1 que cataliza la reacción. La reacción tiene lugar a través de la formación de sal de iminio, donde se cree que el anión fosfato protege eficazmente uno de los enantioface de la sal de iminio.
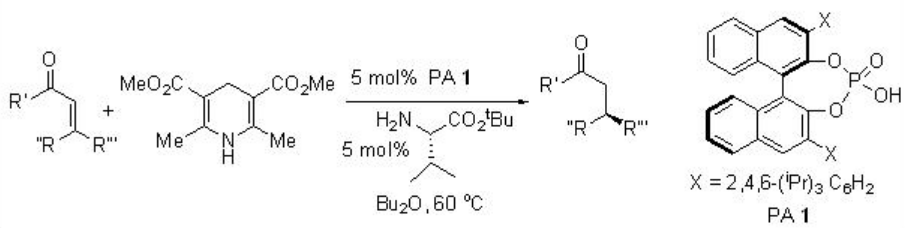
Este método ha sido posteriormente utilizado para la reducción de cetonas α, β -insaturadas (Esquema\(\PageIndex{2}\)). En el que tanto catión como anión son quirales que catalizan con alta enantioselectividad.
Ejemplos:
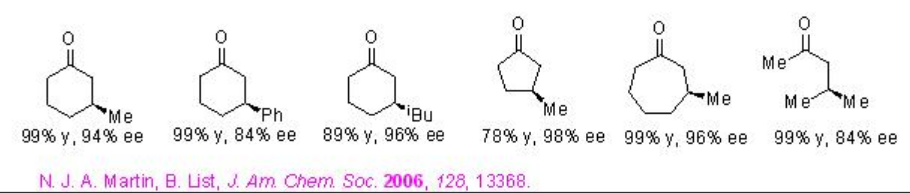
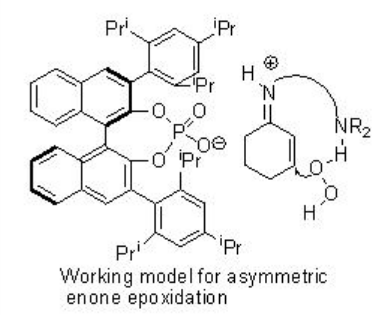
El PA 2 se ha utilizado adicionalmente para la epoxidación asimétrica de aldehídos α, β -insaturados en presencia de t-BuOOH (Esquema\(\PageIndex{3}\)). El ciclo catalítico propuesto se muestra en el Esquema 12. El producto de adición inicial es aquiral y la posterior ciclación a ión iminio conduce al centro estereogénico.
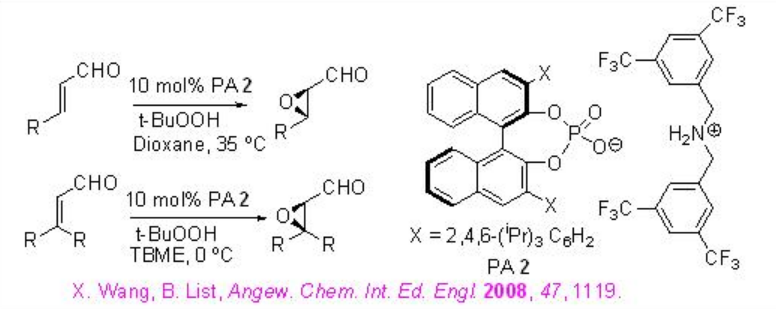
Esta metodología se ha ampliado aún más para la epoxidación de cetonas α, β -insaturadas (Esquema\(\PageIndex{5}\)). En este sistema, la sal de diamina puede servir como catalizador bifuncional para activar posiblemente el sustrato de enona a través de la formación de iones iminio y peróxido de hidrógeno mediante catálisis básica general como se muestra en el Esquema\(\PageIndex{6}\).
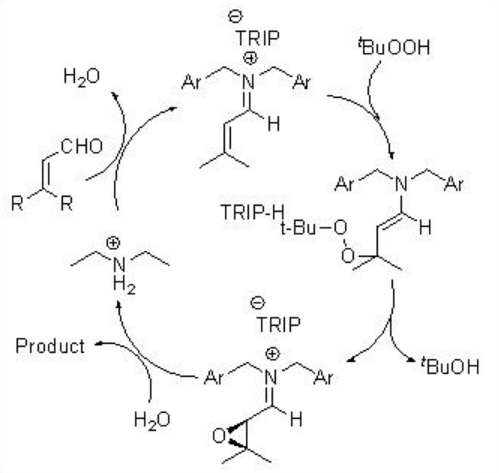
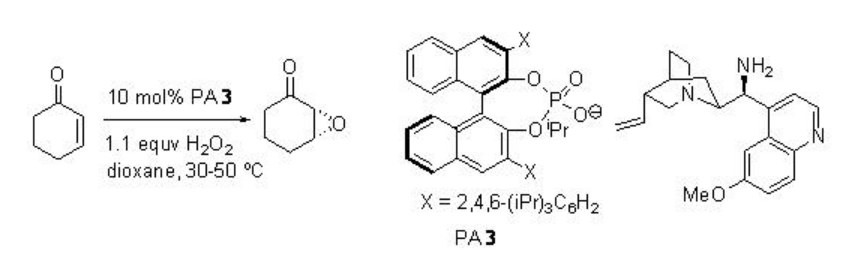
Ejemplos:
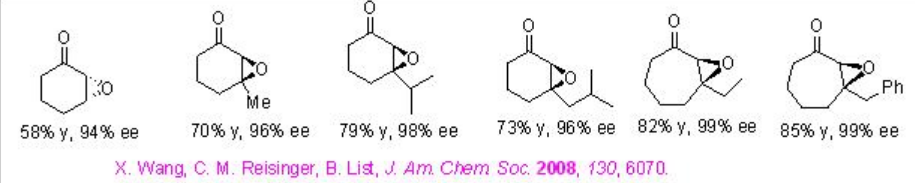
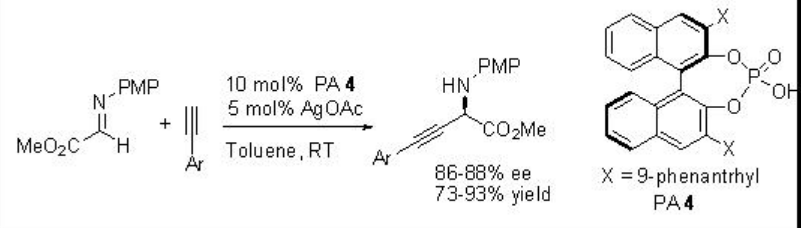
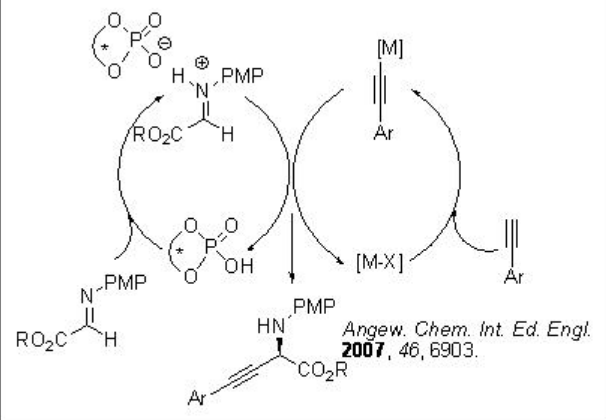
Se ha desarrollado un procedimiento catalítico dual para la activación enantioselectiva de iminas por un ácido de Brønsted combinado con complejo BINOL fosfato que da como resultado una nueva reacción catalizada por metales en la que el contraión quiral induce la enantioselectividad (Esquema 15).
Adiciones nucleofílicas de aldiminas
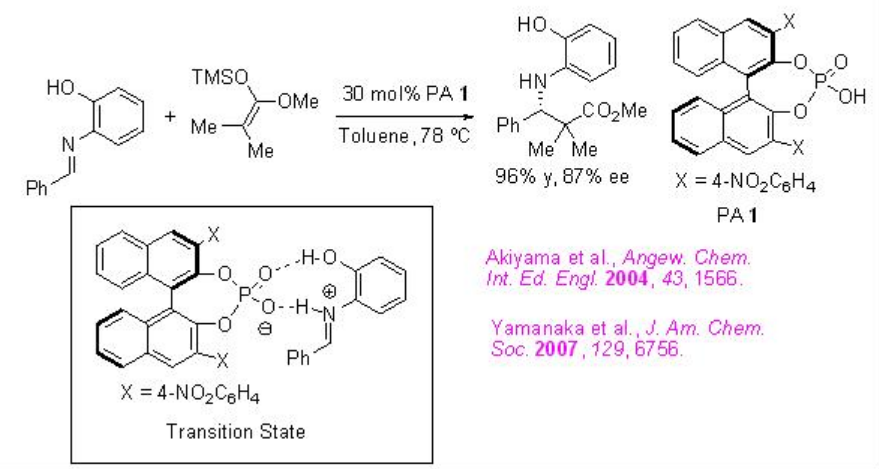
Los ácidos fosfóricos quirales (PA) han sido investigados como catalizadores efectivos para reacciones de tipo Mannich. Por ejemplo, se ha estudiado la reacción de iminas con ceteno silil acetales usando PA 1 en el que la introducción de sustituyentes 4-nitrofenilo en posiciones 3,3'-tiene un efecto beneficioso en la obtención de la alta enantioselectividad (Esquema\(\PageIndex{8}\)). Con base en cálculos de DFT, se ha propuesto un estado de transición zwitteriónica de nueve miembros para explicar la estereoinducción.
La reacción de acetilacetona con iminas N-boc-protegidas ha sido reportada posteriormente empleando 2 mol% PA 2 con excelente rendimiento y enantioselectivitos (Esquema\(\PageIndex{9}\)). El procedimiento es compatible con una serie de sustratos para proporcionar productos diana en altas enantioselectividades.
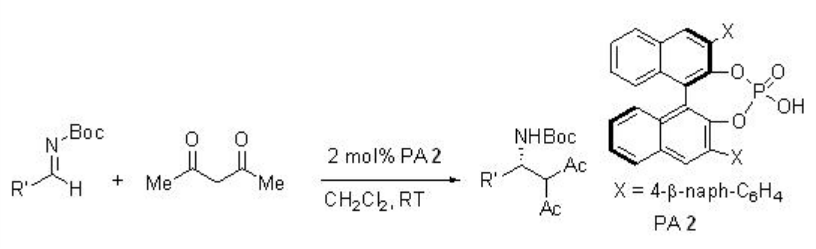
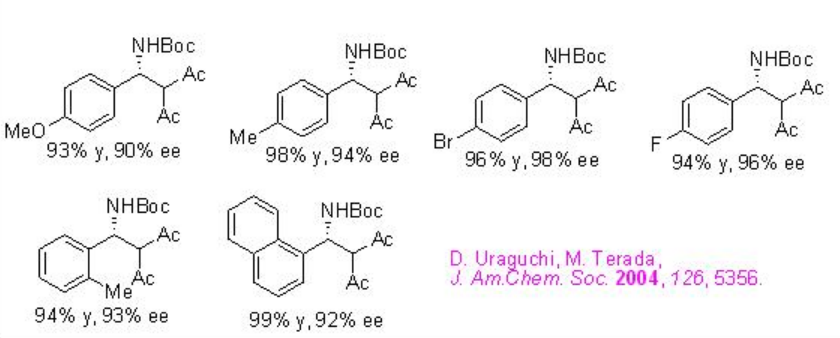
Ejemplos:
El ácido fosfórico PA 3 derivado del derivado H 8-BINOL ha sido estudiado adicionalmente para las reacciones directas de Mannich entre N - aril iminas y cetonas generadas in situ (Esquema\(\PageIndex{10}\)). Los autores han propuesto TS-1 para la enolización de la cetona promovida por ácido y su adición a la aldimina protonada.
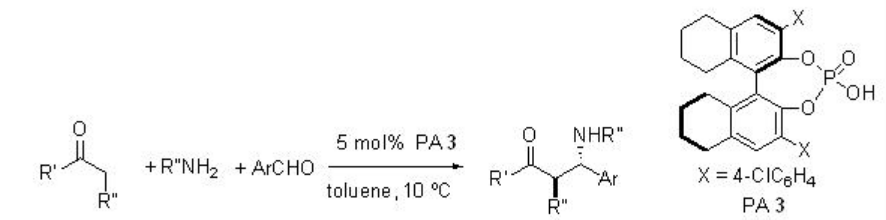
Ejemplos:
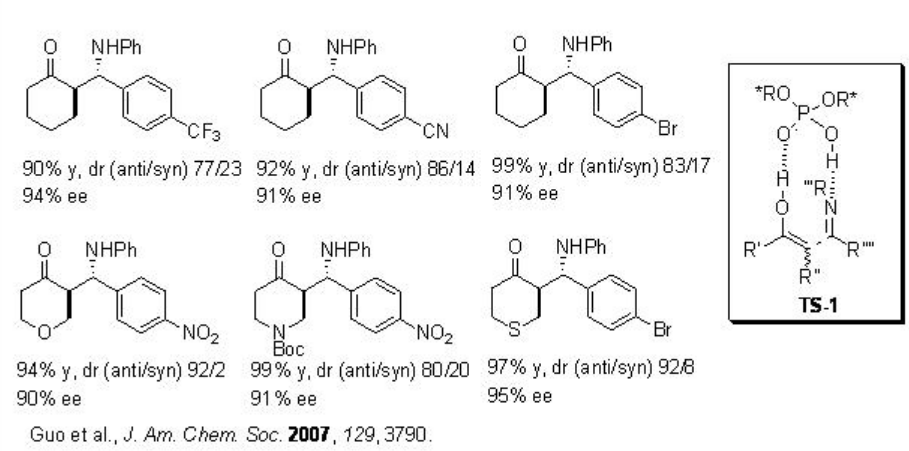
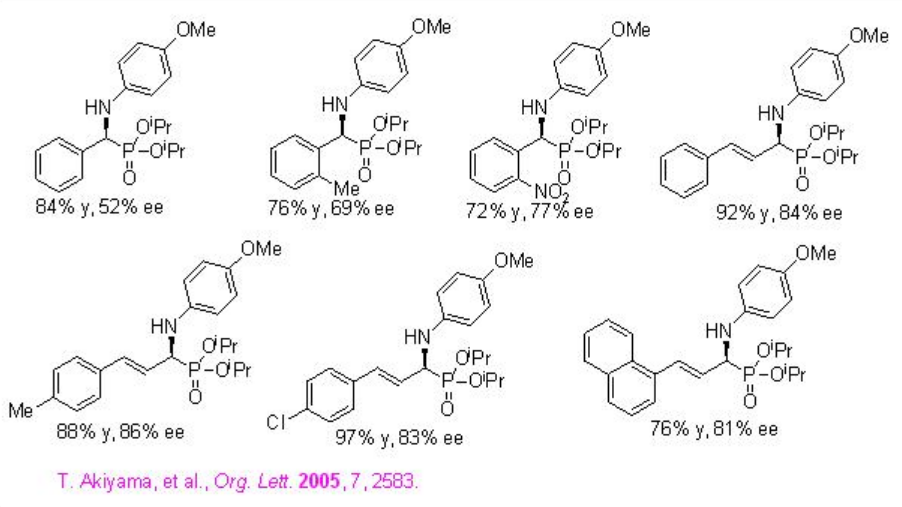
La hidrofosforilación de aldiminas con fosfato de dialquilo se ha estudiado usando PA 4 para proporcionar α-amino fosfonatos ópticamente activos con rendimientos buenos a altos y enantioselectividades (Esquema\(\PageIndex{11}\)). El estado de transición propuesto se muestra en TS-2, donde PA 4 actúa como catalizador bifuncional: el OH en ácido fosfórico activa la aldimina como ácido de Brønsted y el oxígeno fosforílico activa al nucleófilo como base de Lewis, orientando así tanto al nucleófilo como al electrófilo.
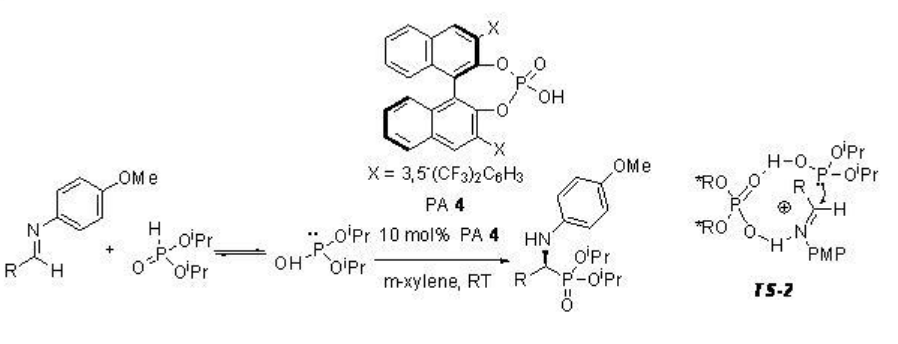
Ejemplos:
Aza-Friedel-Crafts Reacciones
La primera reacción organocatalítica de Aza-Friedel-Crafts de aldiminas se ha logrado usando PA 5 (Esquema\(\PageIndex{12}\)). Es importante señalar que las aril iminas N-boc-protegidas que tienen grupos donadores o —retiradores de electrones en las posiciones orto -, meta - o para - son compatibles con la condición de reacción.
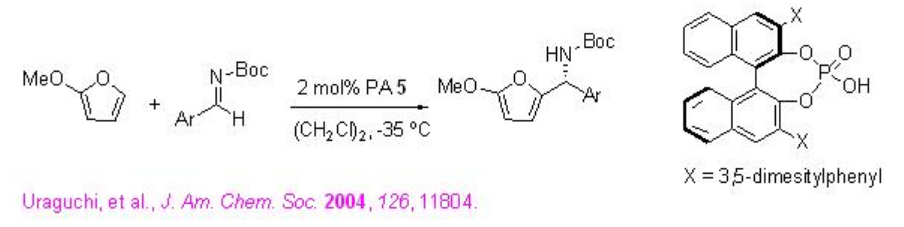
Ejemplos:
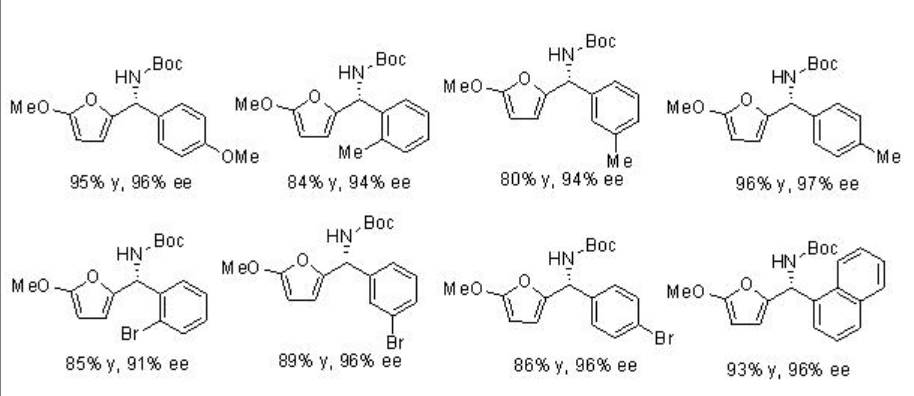
La reacción de indoles con enecarbamatos se ha logrado exitosamente en presencia
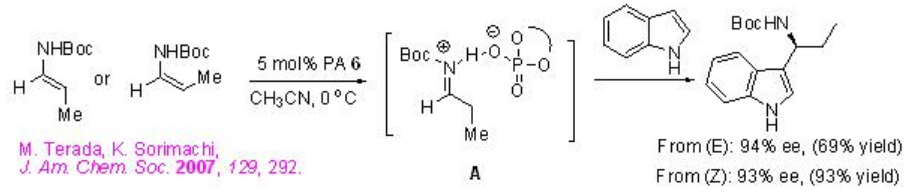
Ejemplos:
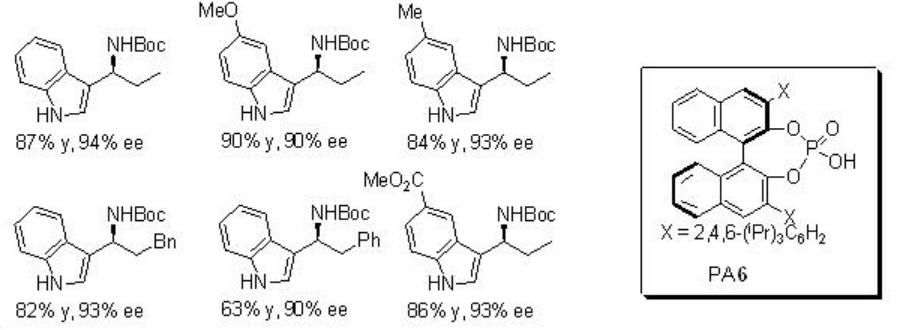
de PA 6 (Esquema\(\PageIndex{13}\)). El uso de regioisómeros puros (E) o (Z) -enecarbamato da el mismo producto con enantioselectividades similares. Así, se cree que la reacción tiene lugar a través de un intermedio común A que podría generarse por la protonación de los enecarbamatos.
Las reacciones del indol con una amplia gama de iminas, derivadas de aldehídos aromáticos, se han demostrado utilizando PA 7 con excelentes enantioselectividades (Esquema\(\PageIndex{14}\)).
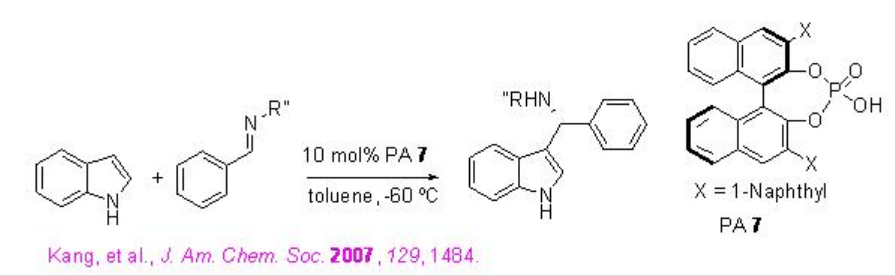
Ejemplos:
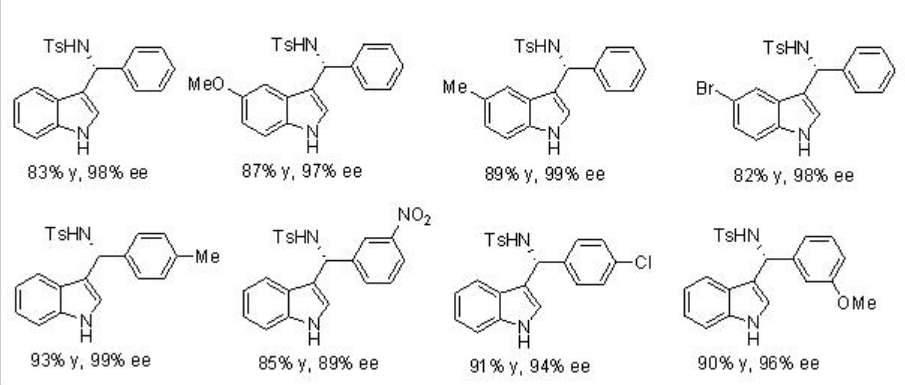
La reacción de Pictet-Spengler de N-tritilsulfenil-triptaminas con diversos aldehídos alfáticos y aromáticos se ha logrado usando PA 7 (Esquema\(\PageIndex{15}\)). El sustituyente sulfenilo estabiliza el ion iminio intermedio y favorece la ciclación de Pictet-Spengler en comparación con la formación indeseada de enamina.
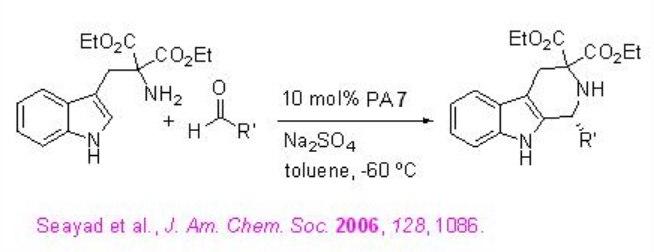
Ejemplos:
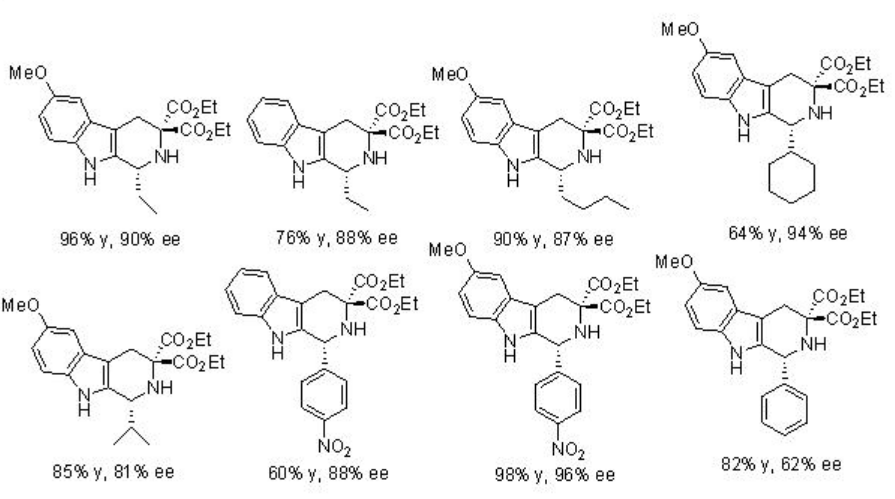
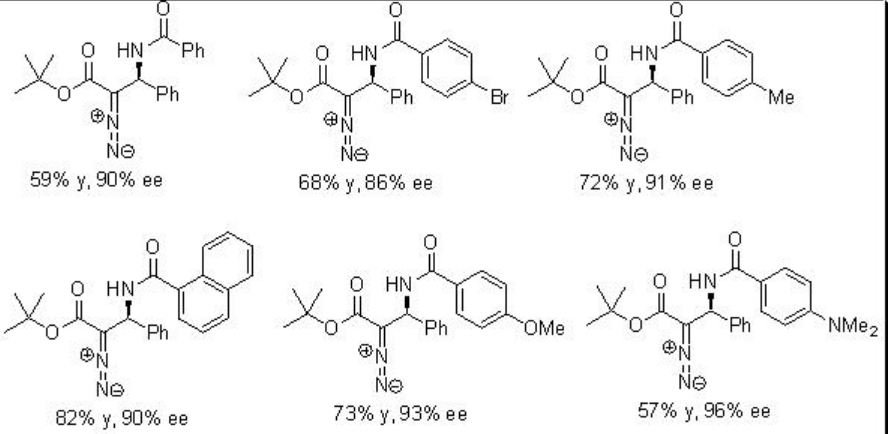
La interesante alquilación de α-diazoésteres con N-acil-iminas se ha demostrado utilizando PA 8 con altas enantioselectividades (Esquema\(\PageIndex{16}\)). El diazoacetato se usa generalmente en la formación de aziridina en presencia de condiciones ácidas de Lewis y Brønsted. Bajo estas condiciones, la formación competitiva de aziridina se ha eliminado al disminuir la nucleofilia de los intermedios amínicos resultantes y así, el aducto de Friedel-Crafts podría formarse a través de la escisión del enlace C-H por el oxígeno fosforílico del ácido fosfórico.
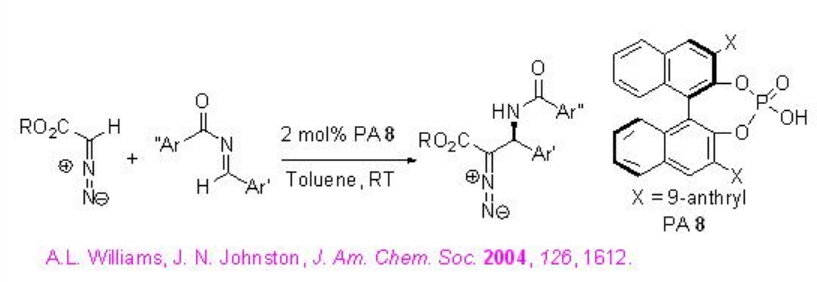
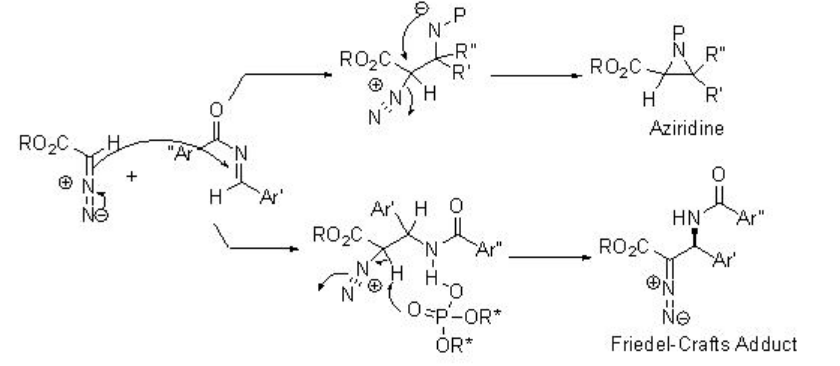
Ejemplos:
1.4.4: Reacción Diels-Aliso
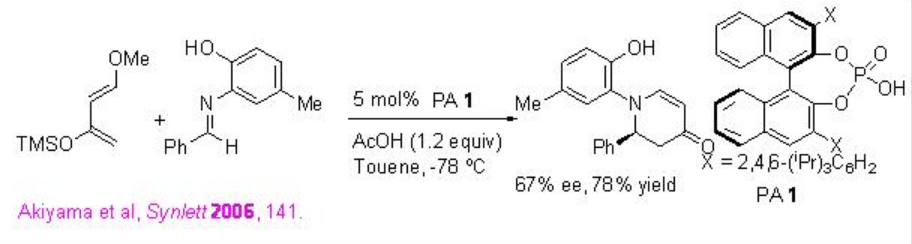
Los ácidos fosfóricos quirales (PA) son excelentes catalizadores para la reacción de Diels-Alder. Por ejemplo, la reacción aza- Diels Alder del dieno de Danishefsky con aldiminas es efectiva usando PA 1 con buenas enantioselectividades (Esquema\(\PageIndex{17}\)). La adición de ácido acético conduce a incrementar significativamente el rendimiento y enantioselectividades.
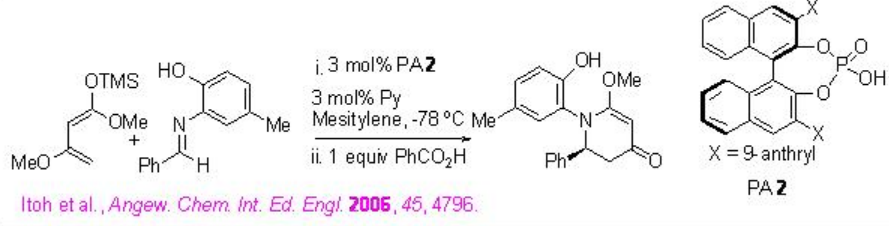
Aunque la reacción aza-Diels Alder del dieno de Brassard usando un ácido de Brønsted es rara debido a la labilidad del dieno en presencia de un ácido fuerte de Brønsted, PA 2 se ha encontrado que es un catalizador efectivo para la reacción aza-Diels Alder del dieno de Brassard (Esquema\(\PageIndex{18}\)). El rendimiento del producto se pudo mejorar usando la sal de piridinio del ácido fosfórico como catalizador.
También se ha encontrado que el PA 2 es efectivo para la reacción inversa de electron-demand aza-Diels Alder de alquenos ricos en electrones con 2-aza dienos con excelentes enantioselectividades (Esquema\(\PageIndex{19}\)). La presencia del grupo OH es crucial para la selectividad cis en los productos.
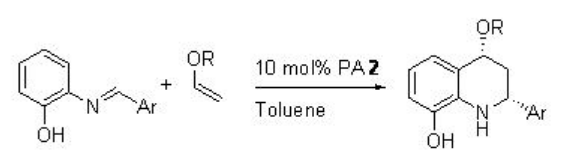
Ejemplos:
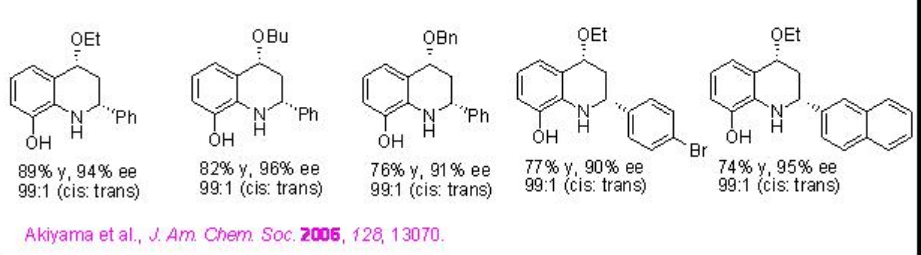
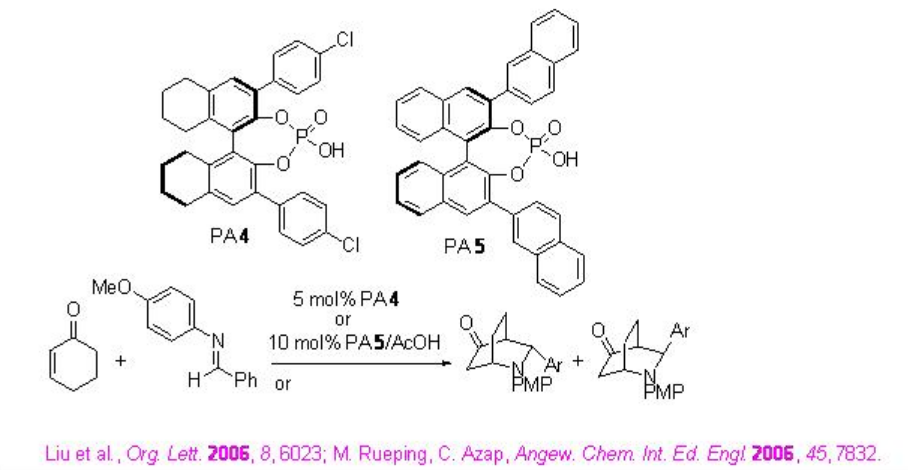
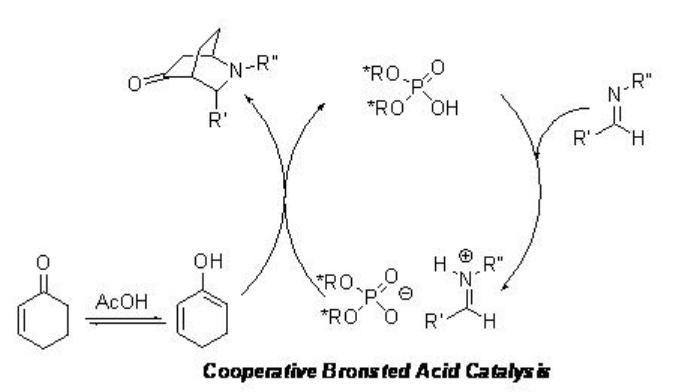
La reacción aza-Diels Alder de aldiminas con ciclohexenona se ha logrado usando PA 4 o PA 5 /AcOH (Esquema\(\PageIndex{20}\)). Se propone un catalizador cooperativo para la reacción usando PA 5 /AcOH, donde se lleva a cabo cooperativamente tanto la activación de un electrófilo como de un nucleófilo (Esquema\(\PageIndex{21}\)).
Hidrogenación por Transferencia
Los ácidos fosfóricos quirales (PA) son catalizadores efectivos para la hidrogenación biomimética usando éster de Hantzsch como fuente de hidruro. Por ejemplo, la reducción de cetiminas usando éster de Hantzsch se puede lograr usando PA 6 con buen rendimiento y enantioselectividades (Esquema\(\PageIndex{22}\)). PA 1 rodamiento voluminoso 2,4,6- (i - Pr) 3 C 6 H 3 en las posiciones 3,3'-de BINOL se encuentra superior a PA 6 para este propósito.

Ejemplos:
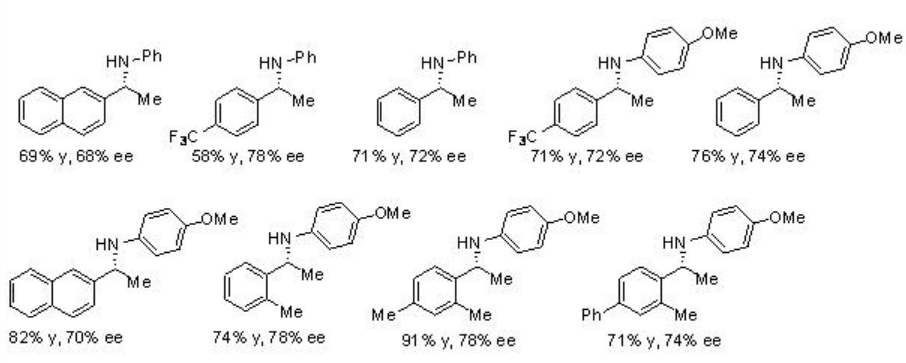
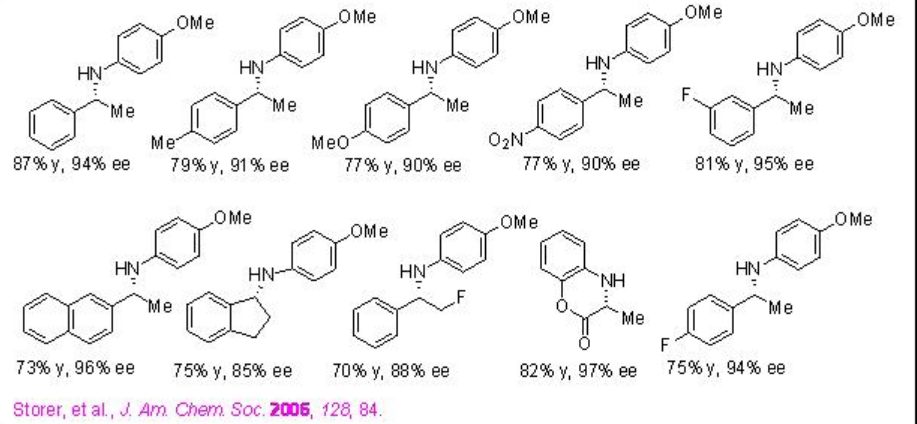
Se pueden realizar reacciones de aminación reductora de tres componentes a partir de cetonas, aminas y éster de Hantzsch usando PA 7 con excelente rendimiento y enantioselectividades (Esquema\(\PageIndex{23}\)). Este método también es compatible para las reacciones de metil fenil cetonas así como metil alquil cetonas.
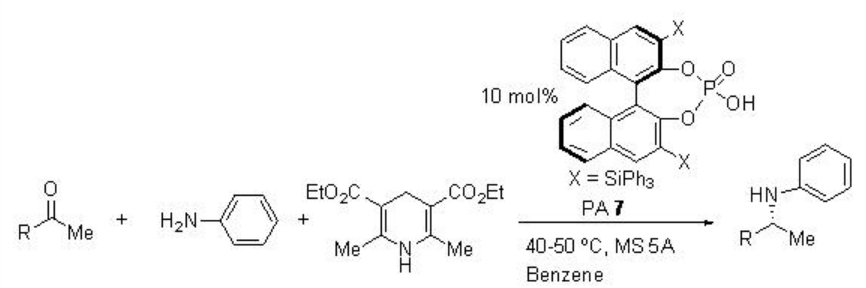
Ejemplos:
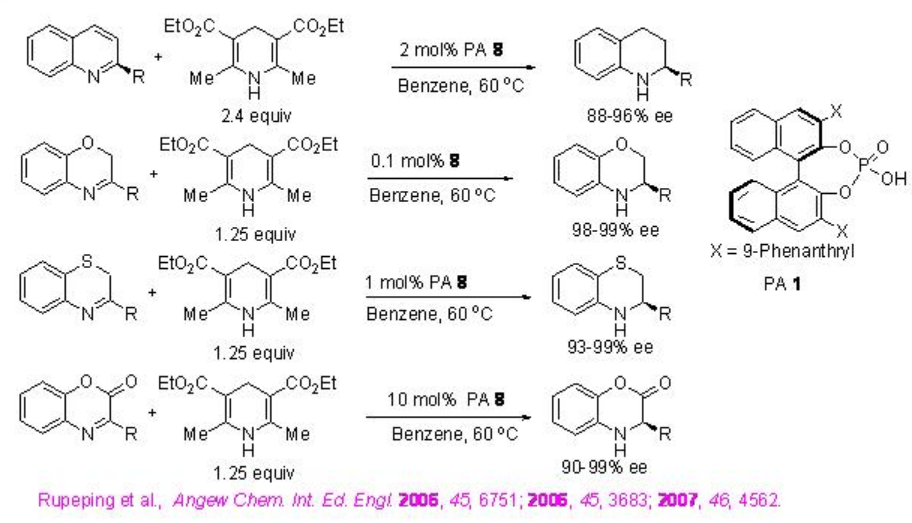
Después de estos estudios iniciales, se ha explorado la reducción de una amplia gama de heterociclos. Por ejemplo, la reducción de una serie de quinonlinas, benzoxazinas, benzotiazinas y benzoxazinonas sustituidas se puede lograr usando PA 8 con excelentes enantioselectividades (Esquema\(\PageIndex{24}\)).
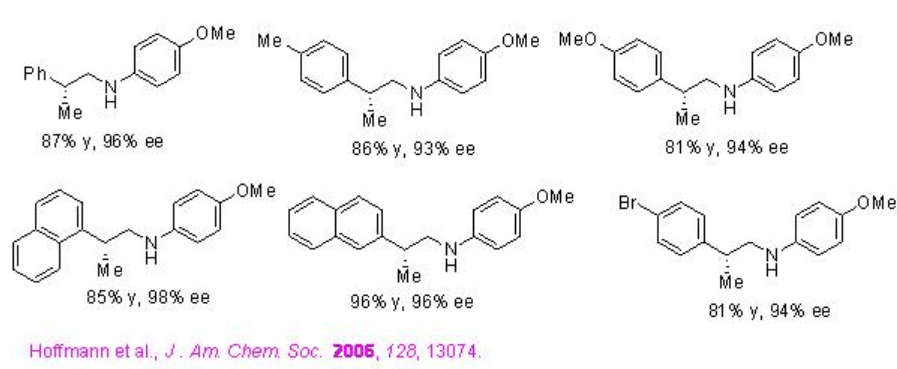
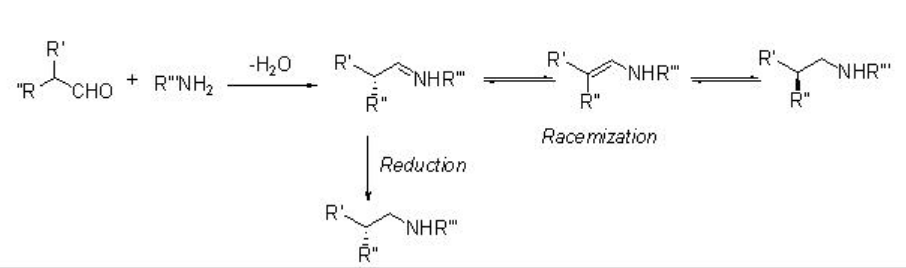
La aminación reductora asimétrica de aldehídos ramificados α y p-anisidina con éster de Hantzch se puede realizar empleando PA 1 con altas enantioselectividades (Esquema\(\PageIndex{25}\)). Los resultados observados sugieren que la reacción procede a través de una resolución cinética dinámica (Esquema\(\PageIndex{26}\)).
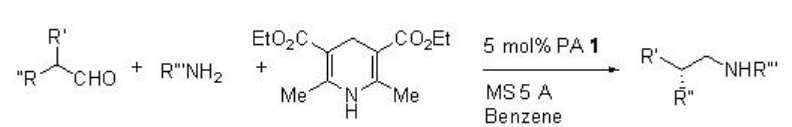
Ejemplos:
Mecanismo propuesto
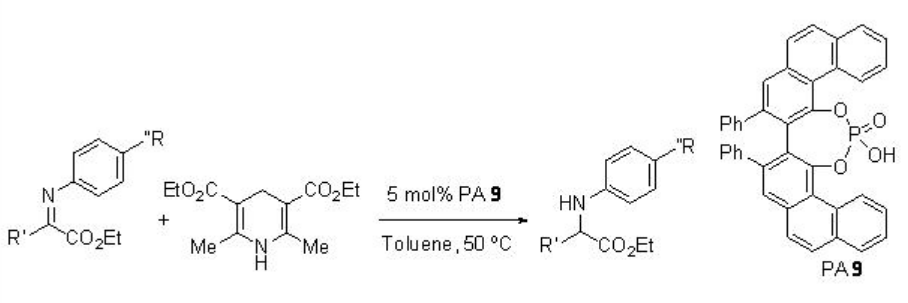
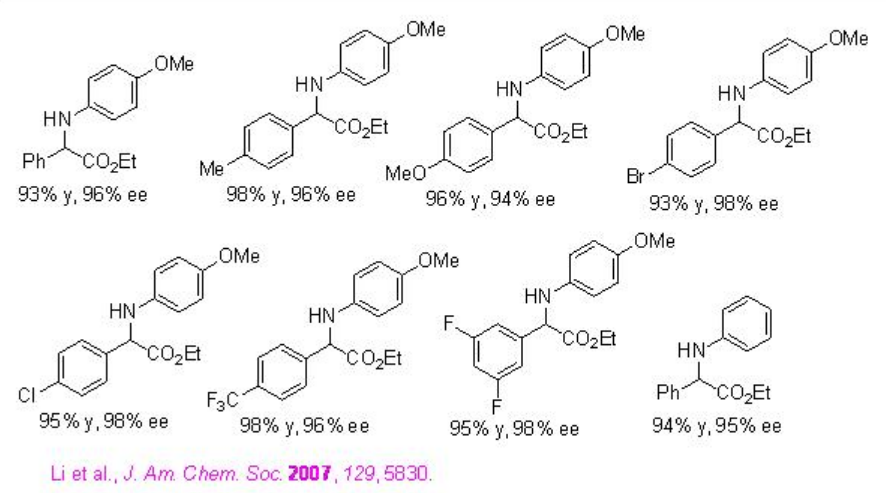
Se encuentra que el ácido fosfórico quiral PA 9 derivado de (S) -VAPOL es superior a los PA derivados de BINOL para la reducción de α-imino ésteres usando éster de Hantzsh para proporcionar α-amino ésteres con mayores enantioselectividades (Esquema\(\PageIndex{27}\)).
Ejemplos:
Reacción de tipo Mannich
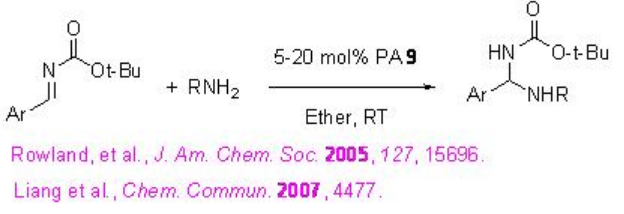
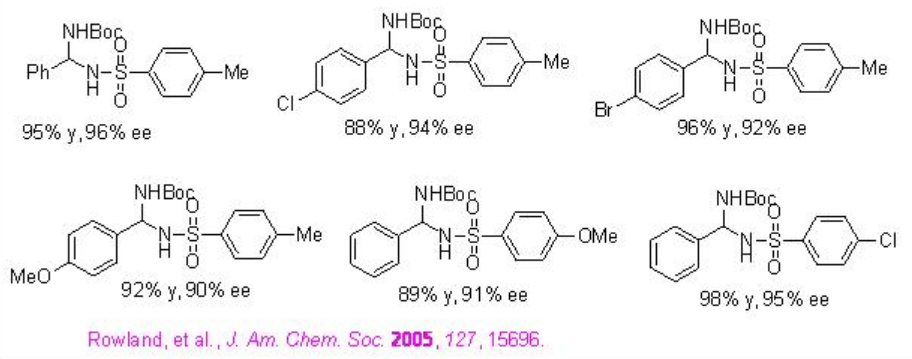
La utilidad del PA 9 se ha extendido aún más como excelente catalizador para la adición de nucleófilos nitrogenados tales como sulfonamidas e imidas a iminas para dar aminales protegidos (Esquema\(\PageIndex{28}\)). El procedimiento tiene un amplio alcance de sustrato para dar a los productos objetivo en 73-99% ee y 80-99% de rendimiento.
Ejemplos:
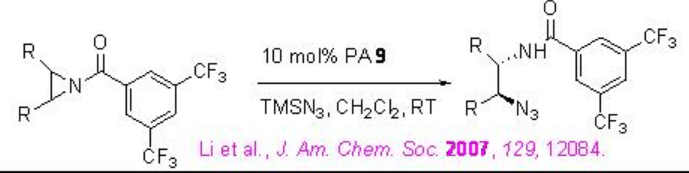
Desymmetrización asimétrica de meso-aziridinas
La aplicación de PA 9 se ha extendido aún más a la apertura del anillo de meso-piridinas. Este es el primer ejemplo de desimetrización organocatalíica de meso-aziridinas. Los sustratos que tienen grupos protectores aceptores de electrones sobre el nitrógeno proceden a la reacción con rendimientos mejorados y enantioselectividad de los productos (Esquema\(\PageIndex{29}\)).
Ejemplos:
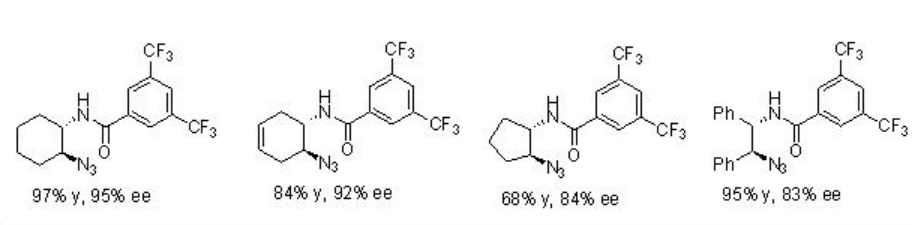
Mecanismo propuesto
El ácido fosfórico reacciona primero con TMSN 3 para dar ácido fosfórico sililado como catalizador activo (Esquema\(\PageIndex{30}\)). Este último activa la aziridina por coordinación de su grupo carbonilo, y el posterior ataque de azida proporciona el precursor del producto y regeneración del ácido fosfórico.