4.1: Reacciones de sustitución alílica
- Page ID
- 73240
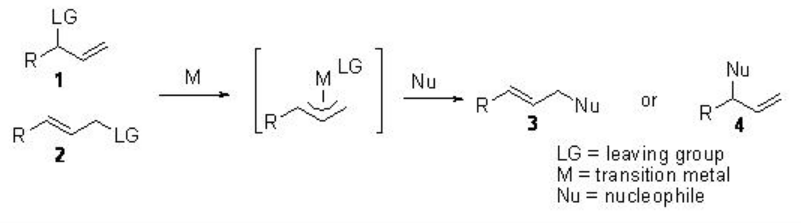
Se ha dedicado mucho esfuerzo a controlar la regioselectividad y enantioselectividad en la sustitución alílica de sustratos 1 o 2 (Esquema\(\PageIndex{1}\)). La sustitución alílica catalizada por paladio es versátil, sin embargo, a menudo se forma el producto (E) -lineal 3. Así, el control de la regioselectividad ha sido recientemente el foco principal para proporcionar el producto 4.
4.1.1 Aminación alílica y Eterificación de Derivados de Alcohol Alílico
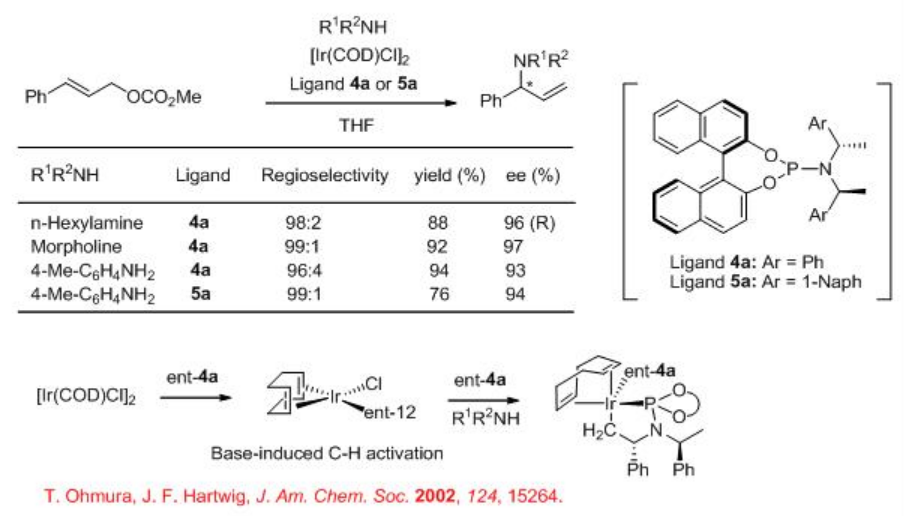
Se ha demostrado que el complejo quiral de iridio que tiene fosforamidato 4a o 5a cataliza la aminación alílica del carbonato para dar un producto ramificado con excelente enantioselectividad (Esquema\(\PageIndex{2}\)). Se ha identificado una forma activada del complejo de iridio mediante la activación in situ de C-H en el grupo CH 3 de un ligando impedido 4a.
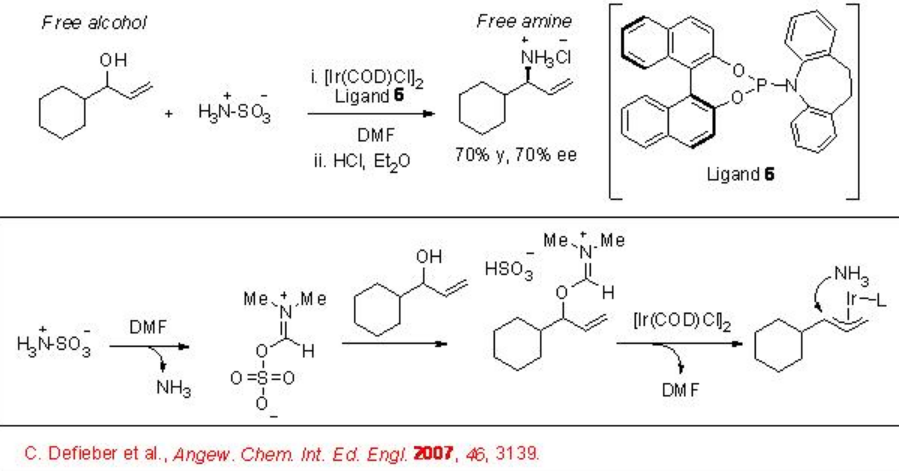
Se ha estudiado la reacción directa de alcoholes alílicos para dar aminas alílicas en presencia de complejo quiral de iridio derivado de [Ir (COD) Cl] 2 y ligando 6 (Esquema\(\PageIndex{3}\)). En esta reacción, el ácido sulfámico sirve no sólo como fuente de nitrógeno sino también como activador in situ del grupo hidroxilo del alcohol alílico.
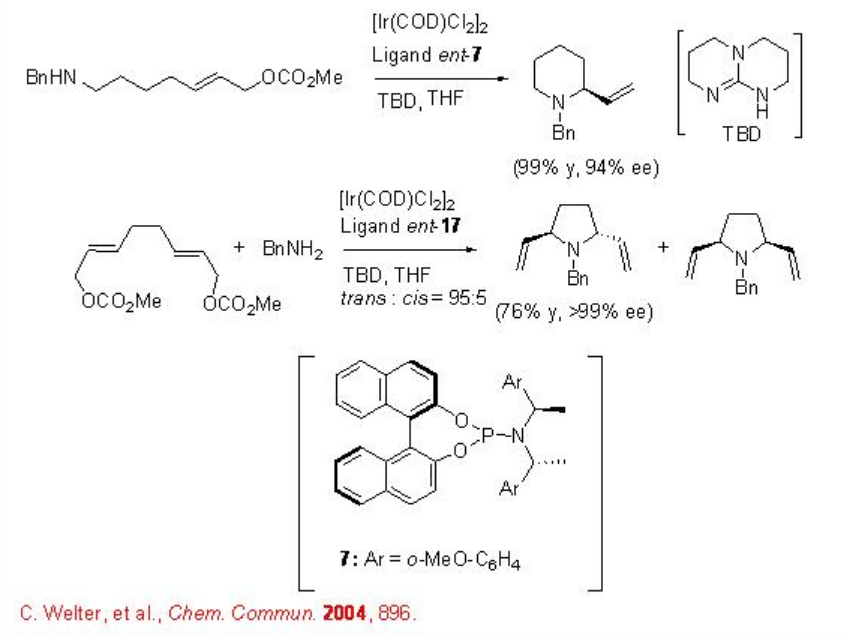
La aminación alílica es importante para la construcción de compuestos heterocíclicos a base de nitrógeno (Esquema\(\PageIndex{4}\)). La aminación enantioselectiva intramolecular alílica se ha logrado utilizando complejo quiral de iridio derivado de [Ir (CDD) Cl 2] 2 y ligando 7. Se ha obtenido buena enantioselectividad tras la activación utilizando 1,5,7-triazabicilo [4.4.0] undec-5-eno (TBD) como base. El sistema catalítico también se ha utilizado para las aminaciones secuenciales de carbonato bis alílico a través de una reacción inter- seguida de una intramolecular.
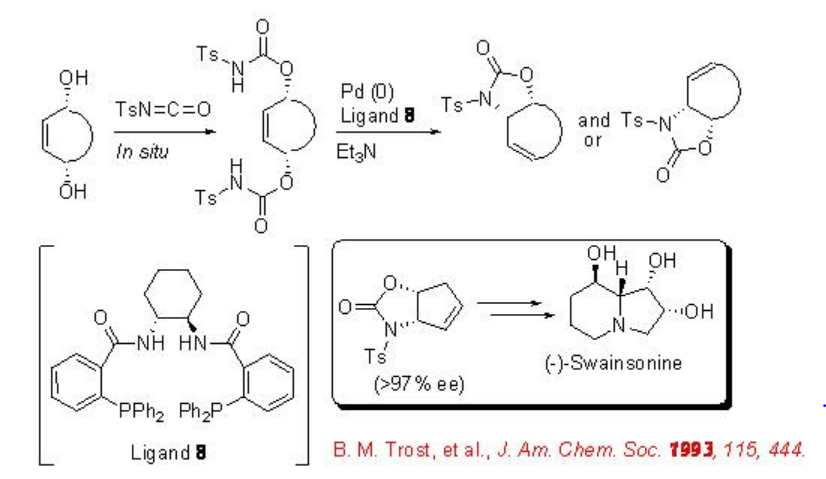
La aminación alílica enantioselectiva es también una poderosa herramienta para la construcción de productos naturales. Por ejemplo, la desimmetrización asimétrica de meso -diol con p-tosilisocianato usando complejo quiral de paladio da fácil acceso a heterociclos quirales sustituidos con nitrógeno que son precursores para la síntesis de (-) -swainsonina (Esquema\(\PageIndex{5}\)).
La aminación alílica enantioselectiva catalizada con paladio quiral también se ha utilizado para la síntesis total de (-) -tubifolina, (-) -deshidrotubifolina y (-) -estricnina (Esquema\(\PageIndex{6}\)).
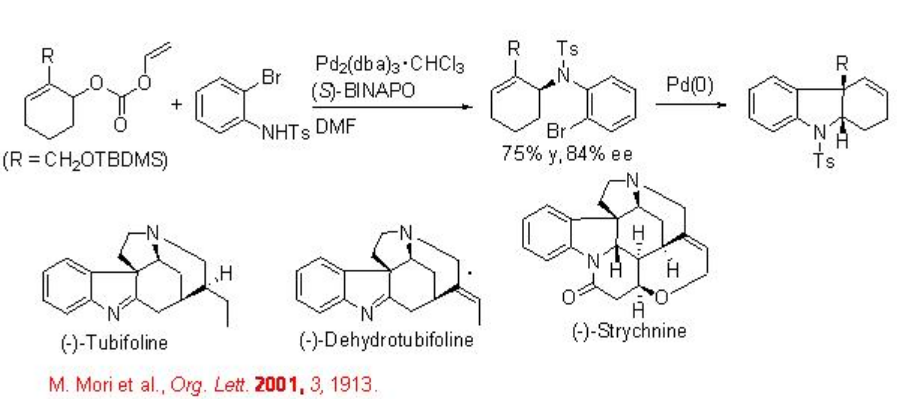
La síntesis enantioselectiva de azaciclo en un solo recipiente se ha mostrado usando una adición de eno-ino catalizada por rutenio seguida de una aminación alílica asimétrica catalizada por paladio (Esquema\(\PageIndex{7}\)).
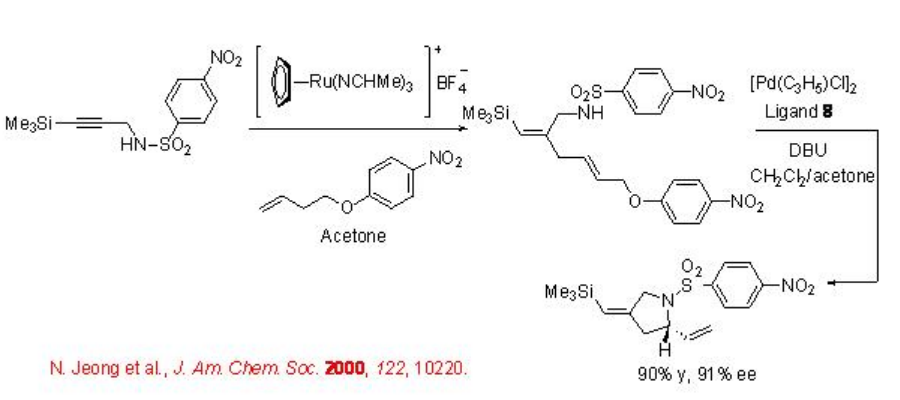
La eterificación alílica regio- y enantioselectiva ha sido estudiada utilizando el complejo quiral de rutenio. Por ejemplo, el complejo de ciclopentadienil rutenio planar-quiral 9 cataliza de manera eficiente la reacción del cloruro de cinamoílo con 3-metilfenol con alta enantioselectividad y rendimiento (Esquema\(\PageIndex{8}\)).
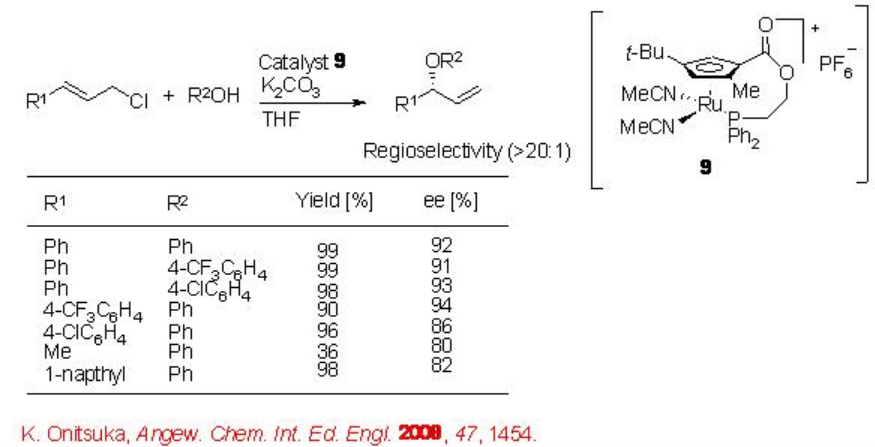
Se han demostrado sustituciones alílicas enantioselectivas de carbonatos con un diboro usando catalizadores a base de cobre (I). Por ejemplo, se ha demostrado que el complejo de Cu (I) -fosfina generado in situ a partir de Cu (O-t-Bu) con el ligando 10 cataliza la reacción de alilboronato con carbonato en excelente regioselectividad y enantioselectividad (Esquema\(\PageIndex{9}\)). Se ha sugerido un mecanismo de adición-eliminación que tiene la generación de complejo Cu alqueno π e intermedio de borilalquilcobre.
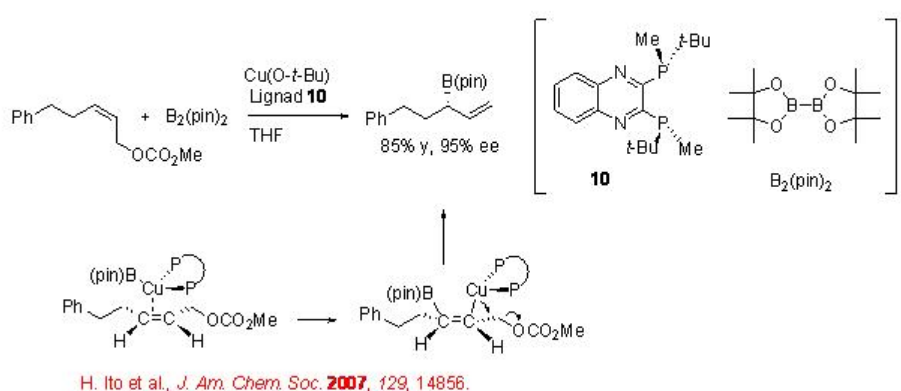
4.1.2 Reacción de los intermedios de π -alilo
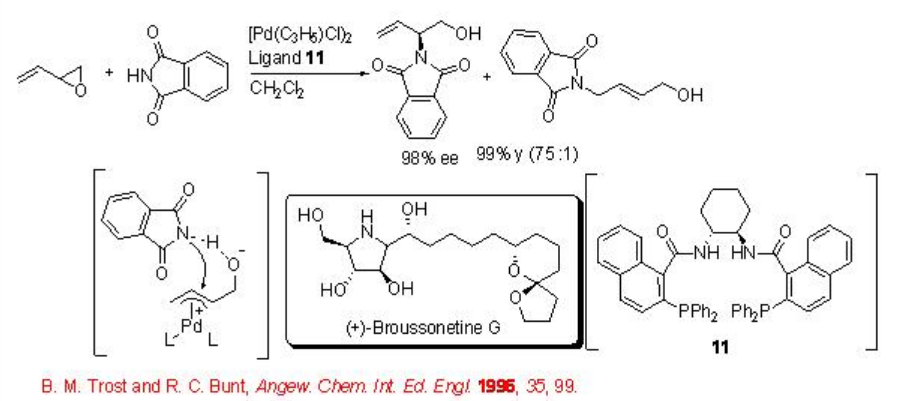
El ataque nucleofílico de una amina a un intermedio π- alilo puede proporcionar un derivado de amina alílica. Por ejemplo, el complejo de paladio derivado de [Pd (C 3 H 5) Cl] 2 y el ligando 11 cataliza la reacción de viniloxirano racémico con ftalimida en rendimiento casi cuantitativo (Esquema\(\PageIndex{10}\)). Se propone la implicación del enlace de hidrógeno del nucleófilo al grupo de salida de oxígeno para entregar el nucleófilo al carbono adyacente para proporcionar la molécula diana. El proceso ha sido utilizado para la síntesis de (+) -broussonetina G.
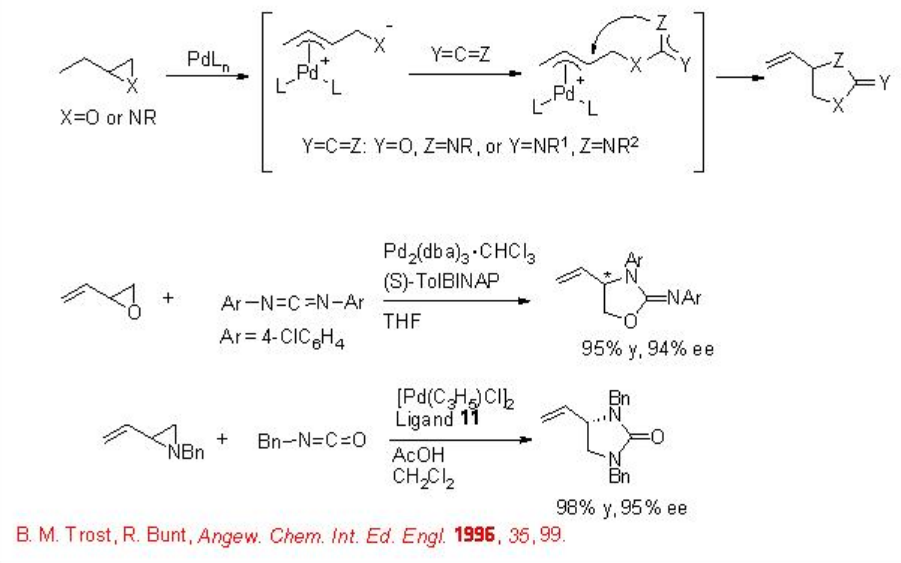
También se han utilizado sistemas basados en paladio para la reacción de cicloadición de epóxidos y aziridinas con heterocumulenos (Esquema\(\PageIndex{11}\)).
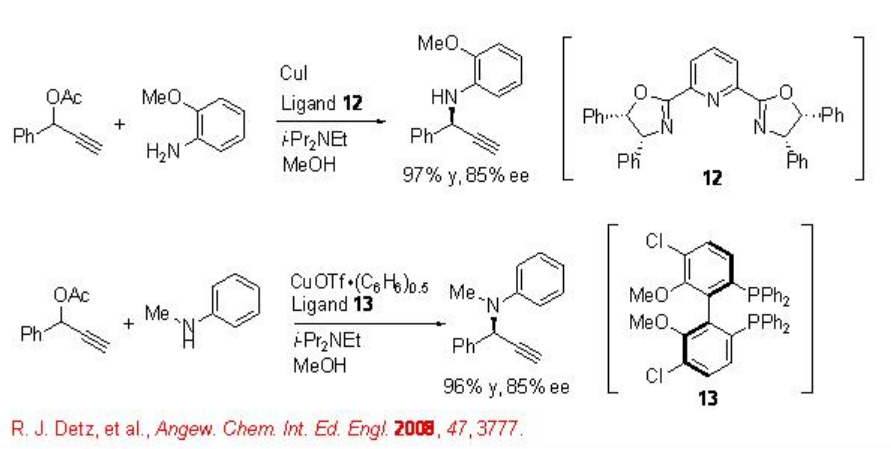
Se han explorado reacciones enantioselectivas de sustitución catalizadas por cobre (I) de acetatos propargílicos con aminas. Por ejemplo, los complejos de cobre derivados de sales de cobre (I) y ligandos 12 y 13 catalizan la reacción de aminación propargílica con 85% ee (Esquema\(\PageIndex{12}\)).